Мексидол при гастрите
Содержание
- Действующее вещество
- АТХ
- Фармакологические группы
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания препарата Мексидол®
- Противопоказания
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Способ применения и дозы
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения препарата Мексидол®
- Срок годности препарата Мексидол®
Действующее вещество
Этилметилгидроксипиридина сукцинат (Ethylmethylhydroxypyridine succinate)
АТХ
N07XX Прочие препараты для лечения заболеваний нервной системы
Фармакологические группы
- Антиоксидантное средство
- Антиоксидантное средство
Нозологическая классификация (МКБ-10)
список кодов МКБ-10
Состав
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
| действующее вещество: | |
| этилметилгидроксипиридина сукцинат | 125,0 мг |
| вспомогательные вещества: лактозы моногидрат; повидон К-30; магния стеарат | |
| оболочка пленочная: Opadry II белый (33G28435) (гипромеллоза, титана диоксид, лактозы моногидрат, макрогол, триацетин) |
Описание лекарственной формы
Круглые, двояковыпуклые таблетки, покрытые пленочной оболочкой от белого до белого с желтоватым оттенком цвета, допускается наличие характерного запаха.
Фармакологическое действие
Фармакологическое действие — антиоксидантное.
Фармакодинамика
Мексидол® является ингибитором свободнорадикальных процессов, мембранопротектором, обладающим антигипоксическим, стресспротективным, ноотропным, противосудорожным и анксиолитическим действием.
Препарат повышает резистентность организма к воздействию различных повреждающих факторов (шок, гипоксия и ишемия, нарушения мозгового кровообращения, интоксикация алкоголем и антипсихотическими средствами — нейролептиками).
Механизм действия препарата Мексидол® обусловлен его антиоксидантным, антигипоксантным и мембранопротекторным действием. Он ингибирует перекисное окисление липидов, повышает активность супероксиддисмутазы, повышает соотношение липид–белок, уменьшает вязкость мембраны, увеличивает ее текучесть.
Мексидол® модулирует активность мембраносвязанных ферментов (кальцийнезависимой ФДЭ, аденилатциклазы, ацетилхолинэстеразы), рецепторных комплексов (бензодиазепинового, ГАМК, ацетилхолинового), что усиливает их способность связывания с лигандами, способствует сохранению структурно-функциональной организации биомембран, транспорта нейромедиаторов и улучшению синаптической передачи.
Мексидол® повышает содержание в головном мозге дофамина. Вызывает усиление компенсаторной активации аэробного гликолиза и снижение степени угнетения окислительных процессов в цикле Кребса в условиях гипоксии с увеличением содержания АТФ и креатинфосфата, активацию энергосинтезирующих функций митохондрий, стабилизацию клеточных мембран.
Препарат улучшает метаболизм и кровоснабжение головного мозга, улучшает микроциркуляцию и реологические свойства крови, уменьшает агрегацию тромбоцитов.
Стабилизирует мембранные структуры клеток крови (эритроцитов и тромбоцитов) при гемолизе. Обладает гиполипидемическим действием, уменьшает содержание общего Хс и ЛПНП.
Антистрессорное действие проявляется в нормализации постстрессового поведения, соматовегетативных нарушений, восстановлении циклов сон– бодрствование, нарушенных процессов обучения и памяти, снижении дистрофических и морфологических изменений в различных структурах головного мозга.
Мексидол® обладает выраженным антитоксическим действием при абстинентном синдроме. Он устраняет неврологические и нейротоксические проявления острой алкогольной интоксикации, восстанавливает нарушения поведения, вегетативные функции, а также способен снимать когнитивные нарушения, вызванные длительным приемом этанола и его отменой.
Под влиянием препарата Мексидол® усиливается действие транквилизирующих, нейролептических, антидепрессивных, снотворных и противосудорожных средств, что позволяет снизить их дозы и уменьшить побочные эффекты.
Мексидол® улучшает функциональное состояние ишемизированного миокарда. В условиях коронарной недостаточности увеличивает коллатеральное кровоснабжение ишемизированного миокарда, способствует сохранению целостности кардимиоцитов и поддержанию их функциональной активности. Эффективно восстанавливает сократимость миокарда при обратимой сердечной дисфункции.
Фармакокинетика
Быстро всасывается при приеме внутрь. При приеме внутрь в дозах 400–500 мг Cmax составляет 3,5–4 мкг/мл. Быстро распределяется в органах и тканях. Среднее время удержания препарата в организме при приеме внутрь — 4,9–5,2 ч.
Метаболизируется в печени путем глюкуронконъюгирования. Идентифицировано 5 метаболитов: 3-оксипиридина фосфат — образуется в печени и при участии ЩФ распадается на фосфорную кислоту и 3-оксипиридин; 2-й метаболит — фармакологически активный, образуется в больших количествах и обнаруживается в моче на 1–2-е сут после введения; 3-й — выводится в больших количествах с мочой; 4-й и 5-й — глюкуронконъюгаты.
Т1/2 при приеме внутрь — 2–2,6 ч. Быстро выводится с мочой, в основном в виде метаболитов и в незначительном количестве в неизмененном виде. Наиболее интенсивно выводится в течение первых 4 ч после приема препарата. Показатели выведения с мочой неизмененного препарата и метаболитов имеют индивидуальную вариабельность.
Показания препарата Мексидол®
последствия острых нарушений мозгового кровообращения, в т.ч. после транзиторных ишемических атак, в фазе субкомпенсации в качестве профилактических курсов;
легкая черепно-мозговая травма, последствия черепно-мозговых травм;
энцефалопатии различного генеза (дисциркуляторные, дисметаболические, посттравматические, смешанные);
синдром вегетативной дистонии;
легкие когнитивные расстройства атеросклеротического генеза;
тревожные расстройства при невротических и неврозоподобных состояниях;
ишемическая болезнь сердца (в составе комплексной терапии);
купирование абстинентного синдрома при алкоголизме с преобладанием неврозоподобных и вегетативно-сосудистых расстройств, постабстинентные расстройства;
состояния после острой интоксикации антипсихотическими средствами;
астенические состояния, а также для профилактики развития соматических заболеваний под воздействием экстремальных факторов и нагрузок;
воздействие экстремальных (стрессорных) факторов.
Противопоказания
повышенная индивидуальная чувствительность к препарату и его компонентам;
острые нарушения функции печени и/или почек;
непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция;
беременность, грудное вскармливание (в связи с недостаточной изученностью действия препарата)
детский возраст (в связи с недостаточной изученностью действия препарата).
Применение при беременности и кормлении грудью
Препарат Мексидол® противопоказан при беременности и в период грудного вскармливания.
Побочные действия
Нарушения со стороны иммунной системы: очень редко — ангионевротический отек, крапивница.
Психические нарушения: очень редко — сонливость.
Нарушения со стороны нервной системы: очень редко — головная боль.
Желудочно-кишечные нарушения: очень редко — сухость во рту, тошнота, боль, жжение и дискомфорт в эпигастральной области, изжога, метеоризм, диарея.
Нарушения со стороны кожи и подкожных тканей: очень редко — сыпь, зуд, гиперемия.
Взаимодействие
Мексидол® сочетается со всеми препаратами, используемыми для лечения соматических заболеваний.
Усиливает действие бензодиазепиновых препаратов, антидепрессантов, анксиолитиков, противосудорожных, противопаркинсонических средств. Уменьшает токсические эффекты этилового спирта.
Способ применения и дозы
Внутрь, по 125–250 мг 3 раза в сутки; максимальная суточная доза — 800 мг (6 табл.).
Длительность лечения — 2–6 нед; для купирования алкогольной абстиненции — 5–7 дней. Лечение прекращают постепенно, уменьшая дозу в течение 2–3 дней.
Начальная доза — 125–250 мг (1–2 табл.) 1–2 раза в сутки с постепенным повышением до получения терапевтического эффекта; максимальная суточная доза — 800 мг (6 табл.).
Продолжительность курса терапии у больных ИБС — не менее 1,5–2 мес. Повторные курсы (по рекомендации врача), желательно проводить в весенне-осенние периоды.
Передозировка
Симптомы: сонливость, бессонница.
Лечение: в связи с низкой токсичностью передозировка маловероятна. Лечение, как правило, не требуется, симптомы исчезают самостоятельно в течение суток. При выраженных проявлениях проводится поддерживающее и симптоматическое лечение.
Особые указания
Влияние на способность управлять транспортными средствами или заниматься другими потенциально опасными видами деятельности. В период приема препарата следует соблюдать осторожность при работе, требующей быстроты психофизических реакций (в т.ч. управление транспортными средствами, механизмами).
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 125 мг. По 10 табл. в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой. По 1, 2, 3, 4, 5 контурных ячейковых упаковок вместе с инструкцией по применению помещают в пачку из картона.
Производитель
ЗАО «ЗиО-Здоровье», 142103, Россия, Московская обл., г. Подольск, ул. Железнодорожная, 2.
Владелец регистрационного удостоверения/организация, принимающая претензии: ООО «НПК «ФАРМАСОФТ», 115407, Россия, Москва, ул. Судостроительная, 41, этаж 1, пом. 12.
Тел./факс: (495) 626-47-55.
Условия отпуска из аптек
По рецепту.
Условия хранения препарата Мексидол®
В защищенном от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности препарата Мексидол®
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Регистрационные удостоверения Мексидол®
Следовательно, применение мексидола в сочетании с традиционной терапией позволяет эффективно воздействовать на панкреатогенную токсемию у больных острым панкреатитом.
Исходя из современных представлений косвенным показателем поражения поджелудочной железы может считаться глюкоземический профиль. Динамика показателя сахара крови была исследована у всех больных. В 48% наблюдений диагностирована гипергликемия. В обеих группах пациентов отмечены случаи сахарного диабета, преимущественно 2-го типа, их частота составила в среднем 16%. При поступлении в клинику больным, как правило, назначалась инсулинотерапия, которая в ряде наблюдений была малоэффективной.
Исследования динамики глюкоземического профиля показали, что после курса лечения мексидолом в основной группе отмечено снижение уровня сахара крови в более ранние сроки, чем в контрольной группе, что указывает на корригирующее воздействие препарата на углеводный обмен при остром панкреатите.
Влияние мексидола на выраженность синдрома эндогенной интоксикации при ОП
У пациентов ОП накопление в крови токсических метаболитов среднемолекулярной массы наряду с продуктами деструкции тканей и промежуточными метаболитами выше допустимых величин ведет к функциональной печеночно-почечной недостаточности, замыкая тем самым один из порочных кругов формирования эндогенной интоксикации.
Анализ уровня молекул средней массы (МСМ) у всех пациентов на момент поступления в клинику показал статистически достоверное увеличение их содержания в плазме крови и в моче.
В основной группе с тяжестью состояния пациентов 0-3 балла к концу курса лечения мексидолом произошло снижение уровня МСМ плазмы в 1,9 раза с полной нормализацией показателя, без последующего повышения. Тогда как в аналогичной контрольной подгруппе не только не произошло снижения уровня МСМ плазмы, но и отмечено некоторое его повышение: средние значения превышали норму в 2,5 раза (табл. 3).
Таблица 3. Динамика уровня МСМ плазмы
В основной группе больных с тяжестью состояния 4-7 баллов по окончании курса лечения мексидолом отмечено снижение среднего уровня МСМ плазмы в 1,6 раза с достижением уровня нормальных значений. В контрольной подгруппе отмечено снижение среднего уровня МСМ плазмы в 1,2 раза, который продолжал превышать нормальные значения в 2 раза. Такие повышенные значения показателя в контрольной подгруппе сохранялись на одном уровне длительный период времени без тенденции к снижению.
В подгруппах больных с тяжестью состояния 8-11 баллов не наблюдалось отчетливых положительных результатов. В основной группе отмечено снижение уровня МСМ плазмы в 1,5 раза, в контрольной — повышение в 1,3 раза. Такие результаты можно объяснить выраженной тяжестью течения патологического процесса у данной группы больных. Острый панкреатит у пациентов третьей подгруппы протекал с развитием панкреатогенного шока, распространенного перитонита и гнойных пара-панкреатических осложнений.
В подгруппах пациентов с тяжестью состояния 12 и более баллов к концу курса лечения отмечалось снижение уровня МСМ плазмы в 1,6 раза (в основной группе) и 1,9 раза (в контрольной).
Анализ динамики МСМ плазмы в контрольной и основной группах выявил различия в течении процесса во время и после окончания курса лечения мексидолом. Отмечено, что на фоне применения мексидола уменьшалась выраженность эндогенной интоксикации. Это подтверждалось тем, что у пациентов основной группы на протяжении всего курса лечения титр МСМ был ниже, чем в контрольной.
У больных ОП, как правило, начиная с первых суток заболевания наблюдался выраженный лейкоцитоз, который в последующем имел тенденцию к нарастанию. У всех пациентов установлен высокий уровень лейкоцитов крови в первые сутки нахождения в клинике — от 9,9х109/л до 25,9х109/л. При этом у 62% больных отмечено увеличение доли незрелых форм лейкоцитов выше 10%.
В основной группе с тяжестью состояния пациентов 0-3 балла к концу курса лечения мексидолом абсолютное количество лейкоцитов крови снизилось в 1,8 раза, при этом не отмечено ни одного случая с уровнем лейкоцитов выше 12×109/л или доли незрелых форм выше 10%. В контрольной группе изменения уровня лейкоцитов за период лечения не произошло и у 30% пациентов сохранялся значительный палочкоядерный сдвиг формулы крови (табл. 4).
Таблица 4. Динамика уровня лейкоцитов крови
В основной группе пациентов с 4-7 баллами по шкале ТФС, нормальный уровень лейкоцитов крови зарегистрирован уже на 5-е сутки лечения, к концу курса лечения мексидолом произошло снижение количества лейкоцитов в 1,7 раза. В этой группе только у одного пациента после курса лечения зарегистрирован сдвиг лейкоцитарной формулы крови влево до 12%. В контрольной группе на 8-е сутки наблюдалось снижение лейкоцитов в 1,2 раза, в дальнейшем без тенденции к снижению. У половины пациентов этой группы значения лейкоцитов крови на 8-е сутки были выше 12х109/л и у 40% сохранялась высокая доля незрелых форм лейкоцитов больше 10%.
В основной группе больных с тяжестью состояния 8-11 баллов на 8-е сутки отмечено снижение уровня лейкоцитов крови в 1,5 раза. Доля больных, имевших значительный палочкоядерный сдвиг формулы крови, к концу лечения уменьшилась в 2,5 раза. Тогда как в контрольной группе у больных с тяжестью состояния 8-11 баллов, наоборот, произошло увеличение среднего уровня лейкоцитов крови в 1,3 раза и существенных изменений формулы крови не отмечалось.
В основной группе пациентов с тяжестью состояния 12 и более баллов к концу курса лечения на 11-е сутки отмечено снижение средних значений показателя в 1,5 раза. Однако при этом у 4 пациентов зарегистрирована лейкопения (уровень лейкоцитов меньше 4х109/л), что является одним из неблагоприятных показателей проявления синдрома системной воспалительной реакции. В контрольной группе при тяжести состояния больных 12 и более баллов статистически значимых результатов по изменению абсолютного количества лейкоцитов крови не получено.
С учетом приведенных данных можно сделать вывод о противовоспалительном эффекте мексидола при лечении ОП. Применение мексидола позволяет быстрее купировать системные проявления синдрома системного воспаления у больных этой категории.
Влияние мексидола на функции печени и белков крови
Одним из решающих факторов, определяющих тяжесть течения и исход ОП, является выраженность функциональных нарушений печени. У ряда пациентов развивается токсический гепатит, нередко переходящий в токсическую дистрофию печени, влекущую за собой полиорганную недостаточность, что в свою очередь обусловливает неблагоприятные исходы заболевания.
С целью изучения функциональной недостаточности печени при ОП исследована динамика показателя билирубина плазмы крови (табл. 5).
Таблица 5. Динамика уровня билирубина
У пациентов с тяжестью состояния 0-3 балла средний уровень билирубина при поступлении находился в пределах нормы и его повышения в ходе лечения не отмечалось.
В основной группе больных с тяжестью состояния 4-7 баллов по шкале ТФС к концу курса лечения мексидолом уровень билирубина снизился в 4,5 раза. В контрольной подгруппе происходило медленное изменение показателя и за аналогичный период времени лечения средние значения уровня билирубина снизились в 1,5 раза, при этом превышали норму в 3,3 раза.
В основной группе больных с тяжестью состояния 8-11 баллов к концу курса лечения мексидолом средний уровень билирубина снизился 2,6 раза. В контрольной подгруппе к концу лечения отмечено снижение значений показателя в 1,6 раза.
В основной группе пациентов с тяжестью состояния 12 и более баллов к концу лечения средний уровень билирубина снизился в 4,3 раза. В контрольной подгруппе к концу лечения уровень билирубина повысился в 1,2 раза. Полученные результаты свидетельствуют о благоприятном воздействии мексидола на функциональное состояние печени, на что указывает динамика уровня билирубина у пациентов основной группы.
В настоящее время ведущим биохимическими маркером токсического печеночного цитолиза является АлАТ. Анализ результатов применения мексидола выявил, что у большинства больных основной группы произошло достоверное снижение уровня АлАТ на 6-11-е сутки в 1,7-3 раза (табл. 6). В контрольной группе к этому сроку во многих наблюдениях не только не произошло изменений, но и было отмечено повышение уровня изучаемого показателя.
Таблица 6. Динамика уровня АлАТ
| Подгруппы | Изменение уровня АЛАТ, е/л | |||
| основная группа | контрольная группа | |||
| до лечения | после лечения | до лечения | после лечения | |
| 1-я | 156 ± 18 1 | 60,2 ± 6 * 1 2 | 204 ± 19 1 | 148 ± 8 * 1 |
| 2-я | 301 ± 14 1 | 126 ± 17 * 1 2 | 225 ± 19 1 2 | 200 ± 12 1 |
| 3-я | 384 ± 14 1 | 126 ± 7 * 1 2 | 116 ± 8 1 2 | 155 ± 12 * 1 |
| 4-я | 358 ± 13 1 | 217 ± 10 * 1 | 496 ± 14 1 2 | 216,5 ± 16 * 1 |
Таким образом установлено, что использование в качестве гапатопротекторного средства мексидола выявило высокую эффективность корригирующего воздействия препарата при токсическом поражении печени у больных острым панкреатитом. В широкой клинической практике нет эффективных и доступных медикаментозных методов коррекции функционального состояния печени, поддерживающих на необходимом уровне ее защитные функции, а также повышающих детоксикационную способность печени.
В последние годы большое внимание клиницистов привлекает роль одного из основных белков плазмы альбумина в функции детоксикации и поддержании показателей гомеостаза. Альбумин является резервной системой депонирования токсинов, компонентом антиоксидантной защиты и регулятором протеолитической активности плазмы. При тяжелых эндотоксикозах, свойственных острому панкреатиту, происходит как снижение общей концентрации альбумина, так и изменение его физико-химических свойств. Это в свою очередь препятствует обмену токсинов между сосудистым руслом и тканями, снижает объем их транспорта к органам детоксикации. По современным представлениям динамика содержания альбумина в плазме крови является высокочувствительным маркером тяжести течения эндотоксикоза и заболевания в целом, а также высокоинформативным критерием прогноза исхода заболевания.
У большинства (92%) больных ОП на момент поступления в клинику отмечена достоверная гипопротеинемия со средними значениями общего белка 57±2,0 г/л, что было связано в том числе с нарушением альбуминсинтезирующей функции печени.
В основной группе пациентов с тяжестью состояния 0-3 балла после окончания курса лечения мексидолом отмечено повышение среднего уровня концентрации альбумина в 1,4 раза, тогда как в контрольной группе за аналогичный период произошло снижение исследуемого показателя в 1,2 раза (табл. 7).
Таблица 7. Динамика альбумина общей концентрации
В основной группе больных с 4-7 баллами по шкале ТФС к концу курса лечения отмечено повышение уровня концентрации альбумина в 1,2 раза. В контрольной группе к концу лечения, напротив, наблюдалось снижение уровня показателя в 1,4 раза.
В основной группе пациентов с тяжестью состояния 8-11 баллов к концу курса лечения мексидолом средние значения концентрации альбумина увеличились в 1,2 раза. В контрольной подгруппе за аналогичный период времени средний уровень исследуемого показателя уменьшился в 1,3 раза.
В подгруппах пациентов с 12 и более баллами по шкале ТФС существенных изменений уровня концентрации альбумина не было отмечено.
Таким образом, при лечении мексидолом отмечено повышение концентрации альбумина, что в свою очередь обусловливало повышение резерва связывания альбумина. Опосредованно при повышении белковообразовательной функции печени возрастает активность репаративных процессов в организме. Следует также отметить экономическую эффективность применения мексидола, так как в основной группе снизилось количество инфузий альбумина по сравнению с контрольной.
Клинические результаты использования мексидола в комплексном лечении ОП
В основной группе пациентов с тяжестью состояния 0-3 балла осложненное течение наблюдалось в 35% случаев (табл. 8). У больных этой подгруппы при проведении контрольного УЗИ на 6-е сутки от начала лечения мексидолом зафиксировано уменьшение размеров поджелудочной железы и неоднородности ее паренхимы, сглаженность контуров. 9 (64,3%) больных выписаны из стационара с выздоровлением на 10-14-е сутки. У 5 (36%) больных развились постнекротические панкреатогенные осложнения: перипанкреатический инфильтрат — у 2 (14%), абсцесс забрюшинного пространства — у 1 (8%), ложная киста хвоста поджелудочной железы — у 2 (14%). Положительная динамика в течении заболевания с отчетливым отграничением деструктивных процессов позволила ограничиться проведением миниинвазивных хирургических методов лечения. На 15-20-е сутки 3 (22%) больным были выполнены пункции и дренирование жидкостных образований под контролем УЗИ.
Таблица 8. Осложнения у больных основной и контрольной групп
| Показатель | Частота осложнений, % | |||||||
| основная группа | контрольная группа | |||||||
| 1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 | |
| Неосложненное течение | 65 | 82 | 42 | 8 | 43 | 19 | 0 | 0 |
| Осложненное течение | 35 | 18 | 58 | 92 | 57 | 81 | 100 | 100 |
| Перипанкреатический инфильтрат | 14 | 12 | 33 |   | 29 | 50 | 25 |   |
| Панкреатогенный абсцесс | 7 |   | 25 | 25 | 7 | 19 | 17 | 8 |
| Псевдокиста поджелудочной железы | 14 |   |   |   | 14 |   | 8 |   |
| Абактериальный асцит-перитонит |   |   |   | 8 | 7 | 6 |   | 42 |
| Гнойный перитонит |   |   |   | 17 |   |   | 8 | 25 |
| Флегмона забрюшинного пространства |   | 6 |   | 17 |   | 6 | 25 | 17 |
| Аррозивное кровотечение |   |   |   | 17 |   |   |   | 8 |
| Внутренний дегистивный свищ |   |   |   | 8 |   |   | 17 |   |
Примечание. 1, 2, 3, 4 — подгруппы больных.
В контрольной подгруппе пациентов с аналогичной тяжестью состояния осложненное течение заболевания имело место в 57% случаев. В этой подгруппе 6 (43%) больных были выписаны в среднем на 18-е сутки в удовлетворительном состоянии, без осложнений. По данным УЗИ, у 7 (50%) больных стабилизация деструктивных процессов наступила к 15-м суткам. У 1 (7%) больного как исход воспалительного процесса наблюдался абсцесс сальниковой сумки, который был дренирован под контролем УЗИ на 20-е стуки. У 2 (14%) больных на 20-е сутки были диагностированы ложные кисты головки и хвоста поджелудочной железы, последние были дренированы под контролем УЗИ. У 1 (7%) больного на 5-е сутки было произведено лапароскопическое дренирование брюшной полости по поводу развития ферментативного перитонита.
В основной группе больных с тяжестью состояния 4-7 балла по шкале ТФС осложненное течение заболевания наблюдалось в 18% случаев. В этой группе у 15 (94%) больных проведено консервативное лечение, они были выписаны из стационара в среднем на 19-е сутки с выздоровлением. У 2 (12%) из них при поступлении было отмечено наличие перипанкреатических инфильтратов, которые к концу лечения мексидолом, по данным УЗИ, не визуализировались. По поводу флегмоны забрюшинной клетчатки был оперирован 1 (6%) больной. Ему была произведена люмботомия, вскрытие полости гнойника и дренирование двумя встречными дренажами с последующим осуществлением проточной санации гнойного очага антисептическими растворами, подобранными в соответствии с чувствительностью к ним бактериальной микрофлоры. Послеоперационный период протекал гладко.
В контрольной подгруппе пациентов осложненное течение было зарегистрировано в 81% наблюдений. В среднем на 26-е сутки после консервативного лечения были выписаны из стационара 11 (69%) больных. У 8 (50%) из них в среднем на 5-е сутки базисной терапии отмечено осложненное течение заболевания с развитием перипанкреатического инфильтрата. На стадии гнойных осложнений были оперированы 5 (31%) больных. У 3 (19%) больных наблюдалось развитие абсцессов хвоста поджелудочной железы, у 1 (6%) больной развилась флегмона забрюшинного пространства. У 1 (6%) больной на 5-е сутки пребывания в стационаре развилась клиническая картина ферментативного перитонита, по поводу которого была произведена санационная лапароскопия с дренированием сальниковой сумки и брюшной полости.
В основной подгруппе пациентов с тяжестью состояния 8-11 баллов осложненное течение заболевания отмечено в 58% случаев. В данной подгруппе 8 (67%) больных были выписаны из стационара в среднем на 33-е сутки, после консервативного лечения без развития панкреатогенных осложнений. У 4 (33%) больных отмечено осложненное течение заболевания — развитие перипанкреатических инфильтратов, которые имели абортивное течение на фоне лечения мексидолом к 15-20-м суткам. У 3 (25%) больных на 15-е сутки наблюдалось развитие абсцесса хвоста поджелудочной железы и множественных абсцессов забрюшинного пространства. Больным были произведены люмботомии со вскрытием и дренированием гнойных полостей, с установкой проточно-промывной системы. Послеоперационный период протекал гладко.
В контрольной подгруппе осложненное течение заболевания наблюдалось в 100% случаев. В 1 (8%) наблюдении зарегистрирован летальный исход в послеоперационном периоде, на фоне прогрессирующего синдрома эндогенной интоксикации с развитием полиорганной недостаточности. У 3 (25%) больных этой подгруппы наблюдалось развитие перипанкреатических инфильтратов в среднем на 12-е сутки. Эти пациенты получали консервативное лечение с положительным эффектом и были выписаны в среднем на 46-е сутки. Осложнения в виде абсцесса хвоста поджелудочной железы были выявлены у 2 (17%) больных на 18-е сутки пребывания в стационаре. Этим пациентам были произведены люмботомии с санацией и дренированием полости абсцесса. У 1 (8%) больного на 15-е сутки выявлена ложная киста головки поджелудочной железы, которая была дренирована под контролем УЗИ. В ранние сроки заболевания 1 (8%) больному было выполнено оперативное вмешательство (лапаротомия, санация и дренирование брюшной полости, секвестрэктомия, санация и дренирование сальниковой сумки) в связи с развитием распространенного перитонита на фоне прогрессирования некротических процессов в поджелудочной железе и нарастания эндогенной интоксикации. У 2 (16%) больных на стадии поздних гнойных осложнений выявлены внутренние дигестивные свищи, которые закрылись самостоятельно. У 2 (16%) больных этой подгруппы на стадии ранних гнойных осложнений как исход воспалительного процесса были флегмоны забрюшинного пространства. Этим пациентам произведены люмботомии с вскрытием и дренированием гнойных полостей.
В основной группе больных с тяжестью состояния 12 и более баллов осложненное течение заболевания наблюдалось в 92% случаев. У 1 (9%) пациента отмечен абсцесс сальниковой сумки, а в последующем образование оментогастрального свища. У 2 (18%) больных возникли флегмоны забрюшинного пространства, в связи с чем больным были выполнены люмботомии с санацией и дренированием гнойных полостей. Еще у 2 (18%) пациентов на 12-е сутки после операции выявлены абсцессы различной локализации, которые были вскрыты и дренированы. У всех больных с благоприятным исходом заболевания,(несмотря на развившиеся осложнения, отмечено улучшение общего состояния, исчезновение болевого синдрома в среднем к 8-м суткам от начала применения мексидола. Летальные исходы в данной подгруппе отмечены в 7 (58%) наблюдениях: 3 (28%) умерли на высоте развития панкреатогенного шока в ранние сроки заболевания; 2 (18%) — в раннем послеоперационном периоде на стадии развития панкреатогенного шока с развитием ДВС-синдрома и аррозивного кровотечения и 2 (18%) умерли на стадии развития гнойных осложнений. Во всех случаях причиной смерти были прогрессирующий эндотоксикоз и синдром полиорганной недостаточности. Диагнозы подтверждены при патологоанатомическом исследовании.
В контрольной подгруппе, несмотря на проводимое комплексное лечение, заболевание у всех больных закончилось летальным исходом. В раннем послеоперационном периоде на высоте развития панкреатогенного шока умерли 8 (67%) больных. На стадии развития гнойных осложнений 4 (33%) летальных исхода наступили вследствие прогрессирующего синдрома эндогенной интоксикации с развитием функциональных полиорганных нарушений, что подтверждено результатами аутопсии.
Таким образом, включение мексидола в комплекс лечебных мероприятий при остром панкреатите позволяет ускорить стабилизацию деструктивных процессов в поджелудочной железе, достигнуть быстрого отграничения воспалительного процесса в окружающих тканях, что в свою очередь позволяет снизить число обширных хирургических вмешательств. Количество обширных лапаротомий в основной группе сократилось в 2,2 раза по сравнению с контрольной группой. Последнее обстоятельство в свою очередь влияет на уровень летальности при данном заболевании (рис. 1). Произошло снижение госпитальной летальности среди больных основной группы с острым панкреатитом в 1,8 раза по сравнению с группой больных, получавших стандартный лечебный комплекс. К непосредственным результатам лечения следует также отнести снижение сроков госпитализации в среднем на 25 койко-дней среди больных с благоприятным исходом (рис. 2).
Рис. 1. Летальность в группах больных с ОП.
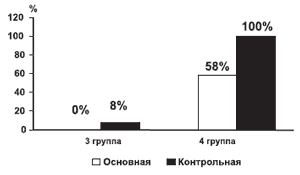
Рис. 2. Длительность стационарного лечения среди больных с благоприятным исходом ОП.
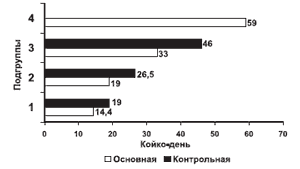
Таким образом, нами получены данные, свидетельствующие об отчетливом благоприятном действии мексидола на динамику местного патологического процесса не только в ткани поджелудочной железы, но и в парапанкреатической зоне и брюшной полости с более быстрым снижением объема поражения при некротическом панкреатите. В контрольной группе на фоне проводимого комплексного лечения в те же сроки у ряда больных отмечено прогрессирование патологического процесса в брюшной полости.
Проведенные исследования показали, что использование препаратов группы производных 3-оксипиридина в комплексе лечебных мероприятий при остром панкреатите является патогенетически обоснованным, так как позволяет в короткие сроки купировать метаболические нарушения и проявления эндогенной интоксикации, предупредить прогрессирование полиорганной недостаточности и за счет этого улучшить результаты лечения больных.
Мексидол может быть рекомендован для включения в комплексную терапию ОП при любом варианте и тяжести течения этого заболевания.
Таким образом, применение препарата мексидол в комплексной терапии ОП позволяет замедлить деструктивные процессы в ПЖ, способствует более быстрому отграничению воспалительного процесса, ускоряет сроки купирования ферментной токсемии и гипергликемии.
Мексидол обладает гепатопротекторным действием, что позволяет купировать проявления печеночного цитолиза, функциональной недостаточности гепатоцитов и метаболических нарушений у больных с ОП.
Применение препарата мексидол в комплексном лечении ОП позволяет эффективно снизить уровень токсических среднемолекулярных соединений, повысить резерв связывания альбумина, что приводит к более быстрому купированию явлений эндогенной интоксикации у пациентов.
Разработанные схемы применения мексидола в комплексной терапии имеют высокую эффективность у большинства больных ОП, однако они не могут существенно изменить течение заболевания у пациентов с необратимыми декомпенсированными системными нарушениями.
Использование препарата мексидол в комплексной терапии ОП позволяет достигнуть существенного снижения частоты осложнений, количества обширных оперативных вмешательств, летальности, а также значительно снизить сроки госпитализации больных острым панкреатитом.
Мексидол может быть рекомендован для широкого применения в клинической практике как препарат, снижающий риск неблагоприятного исхода ОП.
Назначать препарат необходимо в первые сутки начала патогенетического лечения. Вводимые дозы зависят от формы и тяжести острого панкреатита, распространенности процесса, вариантов клинического течения.
Рекомендуемые схемы лечения
1. Острый отечный (интерстициальный) панкреатит — мексидол 100 мг 3 раза в день.
2. Легкая степень тяжести (ТФС 0-3 балла) некротического панкреатита — мексидол 100-200 мг 3 раза в день.
3. Средняя степень тяжести (ТФС 4-7 баллов) некротического панкреатита — мексидол 200 мг 3 раза в день.
4. Тяжелое течение некротического панкреатита (ТФС 8-11 баллов) — мексидол в пульс-дозировке 1000 мг в первые сутки при двукратном режиме введения; далее по 300 мг 3 раза в день с постепенным снижением суточной дозы.
5. Крайне тяжелое течение некротического панкреатита (ТФС 12 и более баллов) — мексидол в стартовой дозировке 1000 мг/сут до стойкого купирования проявлений панкреатогенного шока, по стабилизации состояния по 300-400 мг 3 раза в день с постепенным снижением суточной дозировки.
Отмена препарата должна производиться постепенно, только после достижения устойчивого положительного клинико-лабораторного эффекта.
Препарат, разведенный в 400,0 мл 0,89% раствора хлорида натрия, следует вводить ежедневно. Больным с тяжестью состояния 0-3 балла возможно внутримышечное введение препарата. Пациентам с тяжестью состояния 4 балла и более предпочтительно введение препарата внутривенно капельно, это позволит быстрее купировать явления острого панкреатита.
Площадь пропитывания (см2) стандартных полосок десневой жидкостью, полученной из десневых бороздок (пародонтальных карманов) в области моляров у пациентов с различной степенью нарушения архитектуры
альвеолярной кости
Верхние моляры (n=16) Нижние моляры (n=21)
Разница рабочая балансирующая рабочая балансирующая
площадей проекций 5′ 10′ 15′ 5′ 10′ 15′ 5′ 10′ 15′ 5′ 10′ 15′
< 15 % 0,550±0,05 0,550±0,05 0,583±0,05 0,520±0,05 0,520±0,05 0,569 ±0,05 0,475±0,04 0,475±0,04 0,496±0,04 0,449±0,04 0,449±0,04 0,504±0,04
> 15% 0,520±0,05 0,540±0,05 0,612 ±0,05 0,449±0,04 0,467±0,05 0,529±0,04
соединяющими точки опоры, при проецировании данного тела на плоскость, на которой данное тело находится. «Площадь, на которую опирается тело», и «контур, образованный линиями, соединяющими точки опоры», — номенклатура, применяемая в механике. Описывая стоматологические исследования, логично использовать понятия: «площадь проекции интраальвеолярной части зуба», если речь идёт об исследовании конкретного зуба, и «площадь, образованная линиями, соединяющими контуры интрааль-веолярных частей зубов», говоря об ортопедической конструкции. После удаления зуба линия, разграничивающая интра- и экстраальвеолярные части зубов, ограничивающих дефект целостности, перемещается апикально. Площадь проекции интраальвеолярной части корня зуба на условную линию, параллельную окклюзионной плоскости, сокращается.
Цель работы: определить влияние нагружения на динамику экссудации десневой жидкости, полученной в области зубов, ограничивающих дефект целостности зубного ряда.
Материалы и методы: в исследовании приняли участие 37 пациентов в возрасте от 28 до 40 лет, страдающие локализованным пародонтитом лёгкой и средней степени тяжести, с дефектом целостности зубного ряда III класса по Кеннеди. Всем пациентам с целью стабилизации инфекционной составляющей пародонтита проводилось пародонтологическое лечение.
По данным томографического исследования определяли максимальные площади проекций ин-
траальвеолярной части корней зубов, ограничивающих дефект зубного ряда, и одноимённых зубов на противоположной стороне челюсти на условную плоскость, параллельную окклюзионной плоскости. Сравнив площадь проекций контралатеральных зубов, пациентов объединили в группы: утративших более 15% площади опоры и менее.
Нагружали пародонт заданно, пациенты употребляли жевательную резинку в течение 15 минут. С целью диагностики состояния пародонта получали десневую жидкость, по методу Г.М. Барера и соавт. . Экссудацию определяли по завершении 5-й, 10-й минут и по окончании нагружения (таблица).
Выводы:
1. Кратковременное нагружение пародонта не приводит к достоверному увеличению экссудации десневой жидкости ни на рабочей, ни на балансирующей стороне.
2. Пятнадцатиминутное нагружение увеличивает экссудацию десневой жидкости на 9-12% в области зубов, утративших до 15% площади проекции паро-донта, и на 18% в области зубов, утративших более 15% площади проекции.
3. С целью профилактики нагрузочной составляющей пародонтита необходимо рекомендовать пациентам восстанавливать целостность зубных рядов.
Библиографический список
1. Количественная характеристика десневой жидкости лиц с интактным пародонтом / Г.М. Барер, Э.С. Халитова,
B.В. Кочержинский, Л.М. Лукиных // Стоматология. 1986. № 5
C. 24-26.
УДК -002.44-085.21 Краткое сообщение
ПРИМЕНЕНИЕ МЕКСИДОАА В ЛЕЧЕНИИ БОЛЬНЫХ ВОСПАЛИТЕЛЬНЫМИ ЗАБОЛЕВАНИЯМИ ПАРОДОНТА В СОЧЕТАНИИ С ЯЗВЕННОЙ БОЛЕЗНЬЮ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ
Л.Ю. Островская — ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития, доцент кафедры терапевтической стоматологии, доктор медицинских наук; Ю.А. Кобзева — ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития, ассистент кафедры терапевтической стоматологии, кандидат медицинских наук; Н.А. Хариш -ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития, ассистент кафедры терапевтической стоматологии, кандидат медицинских наук; А.П. Могила — ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцраз-вития, аспирант кафедры терапевтической стоматологии.
Дата поступления — 01.02.2011 г. Дата принятия в печать — 16.02.2011 г
Саратовский научно-медицинский журнал. 2011. Том 7, № 1 (приложение).
С целью определения клинико-патогенетической эффективности мексидола в комплексной терапии пародонтита у больных язвенной болезни желудка и двенадцатиперстной кишки проведены обследование и лечение 296 больных.
Установлено, что использование в комплексном лечении больных пародонтитом на фоне язвенной болезни желудка и двенадцатиперстной кишки мексидола позволяет уменьшить инфекционную нагрузку Helicobacter pylori в пародонтальных карманах и выраженность местного воспаления, нормализовать процессы нейрогумо-ральной и цитокиновой регуляции, что обеспечивает ускорение процессов выздоровления, снижение частоты рецидивов.
Ключевые слова: пародонтит, язвенная болезнь желудка и двенадцатиперстной кишки, мексидол.
Key words: periodontitis, peptic ulcer of stomach and duodenal intestine, Mexidol.
Традиционные методы лечения воспалительных заболеваний пародонта направлены на устранение микробного фактора и включают контроль образования зубного налета, использование антимикробных, противовоспалительных средств местного и общего применения, совершенствование хирургических методов устранения инфекционно-деструктивного очага в пародонте. Однако они не всегда достаточно эффективны и нередко не препятствуют обострению патологии. Перспективным в комплексном лечении хронического гингивита и пародонтита в сочетании с язвенной болезнью желудка и двенадцатиперстной кишки является использование антиоксидантов и ан-тигипоксантов. В последние годы во многих областях клинической медицины успешно применяется антиоксидант мексидол (3-окси-6-метил-2-этилпиридин сукцинат), являющийся структурным аналогом соединений группы витамина В6
Цель работы: оптимизация терапии пациентов с воспалительными заболеваниями пародонта на фоне язвенной болезни желудка (ЯБЖ) и двенадцатиперстной кишки (ЯБДК).
Обследованы 85 пациентов с воспалительными заболеваниями пародонта на фоне ЯБДК и 62 — на фоне ЯБЖ, которые получали, помимо стоматологического лечения и 7-дневной эради-кационной терапии, мексидол внутримышечно в сочетании с местным применением 10 дней. Группу сравнения составили 90 пациентов с воспалительными заболеваниями пародонта на фоне ЯБДК и 59 — на фоне ЯБЖ, которые получали стоматологическое лечение и эрадикационную терапию первой линии в течение семи дней. Контрольную группу составили 25 практически здоровых лиц.
Для идентификации эпителиоцитов десны, продуцирующих мелатонин и NO-синтазу, проводили иммуногистохимическое исследование с использованием моноклональных мышиных антител к NO-синтазе (1:150, Novocastra), кроличьих антител к мелатонину (1:100, CIDtech Res. Comp.). Определение концентрации интерлейкина-6, интерлейкина-10, интерлейкина-12 и ин-
Ответственный автор — Островская Лариса Юрьевна.
Адрес: 410056, г. Саратов, ул. Мичурина, 4, кв.20.
Тел.: 89053201853.
E-mail: nastya_ostrovska@mail.ru
терлейкина-18 в ротовой жидкости проводили методом твердофазного иммуноферментного анализа с помощью иммуноферментного анализатора «Униплан» с использованием наборов реактивов «Интерлейкин-6» и «Интерлейкин-10» (ООО «Цитокин», Россия), «Интерлейкин-18 -ИФА — БЕСТ» (ЗАО «Вектор-Бест», Россия) и «Интерлейкин-12 + p40» (IBL, США).
По всем определяемым тестам (индекс гигиены, индекс кровоточивости десны, РМА, пародон-тальный индекс) на 2-й неделе лечения и через 2 месяца от начала лечения у больных основной группы показатели были существенно ниже, чем у пациентов группы сравнения. Ремиссия гингивита и пародонтита была достигнута в более сжатые сроки. Недельный курс антибиотикотерапии в сочетании с мексидолом приводит к достоверному снижению Helicobacter pylori в пародонтальных карманах и зубном налете. Анализ регрессии субъективных и объективных симптомов заболеваний пародонта показал, что в основной группе через 2 месяца от начала лечения у всех пациентов достигнута ремиссия гингивита и пародонтита легкой степени, ремиссию пародонтита средней и тяжелой степеней на фоне ЯБДК наблюдали у всех, а на фоне ЯБЖ у 32 (91,4%) больных. Напротив, у пациентов группы сравнения ремиссия пародонтита средней и тяжелой степеней констатирована у 68 и 70% пациентов соответственно с ЯБДК и ЯБЖ.
Высокая клиническая эффективность применения мексидола в комплексном лечении больных воспалительными заболеваниями пародонта на фоне язвенной болезни коррелировала с положительной динамикой количественной плотности эпителиальных клеток десны, иммунопозитивных к синтазе оксида азота и мелатонину, а также местного цитокинового баланса (ИЛ-6, ИЛ-10, ИЛ-12 и ИЛ-18)в ротовой жидкости.
Большинство пациентов, получавших 7-дневную эрадикационную терапию в сочетании с мексидолом, отметили хорошую переносимость курса лечения. Побочные эффекты были отмечены у 20 (13,6%) больных: металлический привкус во рту у 5, головная боль — у 4 больных, которые пациенты связывали с
Saratov Journal of Medical Scientific Research. 2011. Vol. 7, № 1 (supplement).
приемом омепразола, кишечная диспепсия — у 9 пациентов.
Таким образом, применение мексидола у пациентов с сочетанной патологией пародонта и язвенной болезни обосновано с позиции лечения и профилактики патологии пародонта. Обладая универсальным
цитопротективным, иммуномодулирующим действием, мексидол уменьшает клинические проявления и позволяет достичь стабильной ремиссии заболеваний пародонта на фоне язвенной болезни желудка и двенадцатиперстной кишки.
УДК -02-055.2-039.1(047.6) Краткое сообщение
КЛИНИЧЕСКИЕ ОСОБЕННОСТИ И НЕКОТОРЫЕ МЕХАНИЗМЫ ФОРМИРОВАНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПАРОДОНТА У ЖЕНЩИН В ПОСТМЕНОПАУЗАЛЬНОМ ПЕРИОДЕ
Л.Ю. Островская — ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития России, доцент кафедры терапевтической стоматологии, доктор медицинских наук; А.И. Ханина — ГОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития России, врач-стоматолог клиники «Люкс Мастер».
Дата поступления — 01.02.2011 г. Дата принятия в печать — 16.02.2011 г.
Островская Л.Ю., Ханина А.И. Клинические особенности и некоторые механизмы формирования воспалительных заболеваний пародонта у женщин в постменопаузальном периоде // Саратовский научно-медицинский журнал. 2011. Т. 7, № 1 (приложение). С. 318-319.
С целью определения клинико-морфологических особенностей развития воспалительных заболеваний пародонта у женЩин в постменопаузальном периоде проведено обследование 90 пациенток. Установлено, что постменопаузальный остеопороз является фактором риска развития заболеваний пародонта. В формировании патологии пародонта у женщин в этот период важную роль играют гормональные изменения.
Ключевые слова: заболевания пародонта, остеопороз, постменопауза.
Key words: periodontal diseases, osteoporosis, postmenopa^.
Воспалительные заболевания пародонта широко контрольную группу составили 20 практически здо-
распространены среди взрослого населения и явля- ровых женщин фертильного возраста. Диагностику
ются основной причиной преждевременной потери пародонтита проводили в соответствии с терминоло-
зубов. Наиболее высокая распространенность па- гией и классификацией болезней пародонта, утверж-
тологии пародонта наблюдается при гормональных денными на XVI Пленуме Всесоюзного общества
сдвигах в организме, в том числе у женщин в пери- стоматологов (1983). Рентгенологическое обсле-
од постменопаузы. Постменопауза характеризуется дование зубочелюстной системы включало в себя
метаболическими изменениями, в том числе и мине- внутриротовые контактные снимки отдельных групп
ральной плотности костной ткани, микроциркуляции, зубов и ортопантомографию. Степень атрофии аль-
иммунного статуса, что предрасполагает к формиро- веолярн°г° гребня °ценивали на °сн°вании ортогшнь
ванию и прогрессированию воспалительных заболе- т°мограмм с исп°льз°ванием индекса фукса (fuchs,
ваний пародонта. Остеопения и остеопороз — частые 1946). Оценку минеральной плотности костной тка-
спутники постменопаузы. Остеопоротические изме- ни (денситометрию) выполняли на ультразвуков°М
нения, возникающие в различных отделах скелета, пяточном °сте°метре Achilles Express (Liinar, США).
затрагивают и костную ткань зубочелюстной систе- Пров°дили °ценку маркеров костного метаболизма
мы, способствуя развитию и прогрессированию забо- в сыворотке крови: активность костной щелочной
леваний пародонта. фосфатазы (Lahema, Чехия), активность тартрат-
Цель исследовании: определить клинические резистентной кислой ф°сфатазы ксж-
проявления и морфологические особенности хрони- центрацию остеокальцина (N°rdic Дания)
и уровень С-концевых телопептидов, образующихся
при деградации коллагена I типа (Serum CrossLaps
ческого генерализованного пародонтита у женщин в
постменопаузальном периоде.
Обследованы 70 женщин с хроническим гене- e ,Step (Nordic Bioscience Дания). Материал дпя
рализованным пародонтитом (ХГП) в постменопау- морфлогическог° исследования забирали из слизи-
стой оболочки в области межзубного сосочка после
зальном периоде жизни (в возрасте от 53 до 59 лет),
——————————————————— проведения местного обезболивания 2%-ным рас-
огветственньш авт°р — Остро^^ Шриса Юрьевна. твором лидокаина. Для идентификации рецепторов
Адрес: 410056, г. Саратов, ул. Мичурина, 4, кв.20.
Тел- 89053201853 эстрогеновых гормонов в десне использовали имуно-
E-mail: nastya_ostrovska@mail.ru гистохимический метод, морфометрический анализ.
Саратовский научно-медицинский журнал. 2011. Том 7, № 1 (приложение).