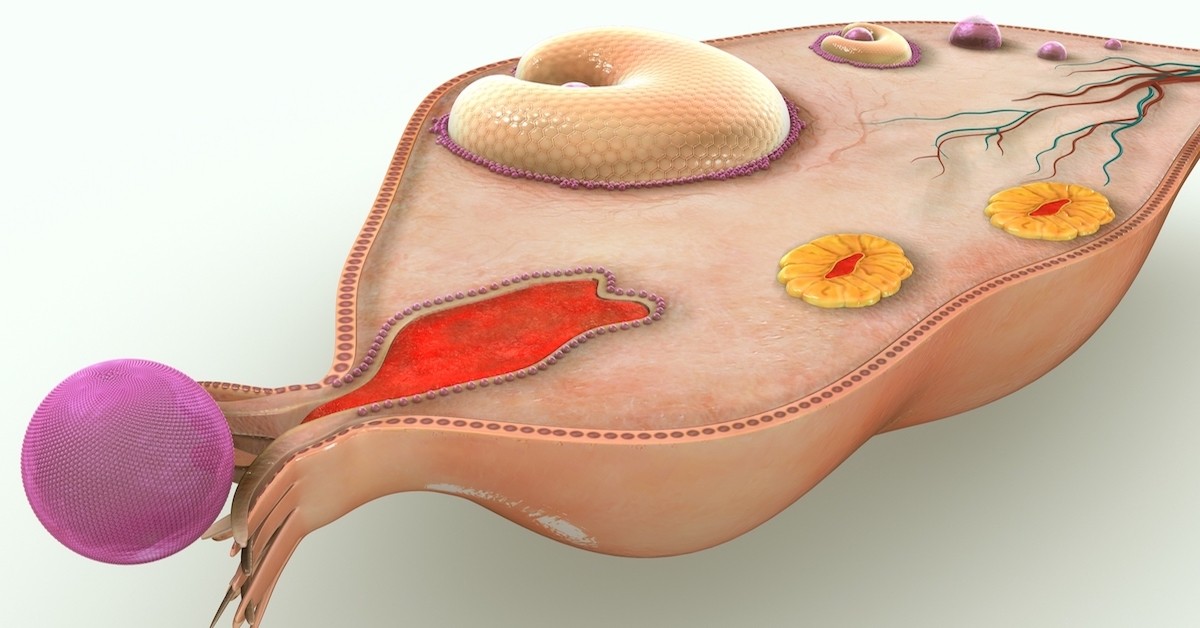
Для стимуляции кишечника в послеоперационном периоде применяют
УДК 616.34 — 089.168.1 — 08
Б. С. ЖАКИЕВ, У Г. КАРСАКБАЕВ, Б. М. МУХАМЕДГАЛИЕВА, М. С. КЕЛИМБЕРДИЕВ, А. У КАРСАКБАЕВ
МОТОРНЫЕ НАРУШЕНИЯ КИШЕЧНИКА В РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ, ПРОФИЛАКТИКА И ЛЕЧЕНИЕ
Западно-Казахстанский государственный медицинский университет имени Марата Оспанова, г. Актобе, Республика Казахстан
B. S. ZHALKIEV, U. G. KARSAKBAYEV, B. M. MUCHAMEDGALIEVA, M. S. KELIMBERDIEV, A. U. KARSAKBAYEV
PREVENTION AND TREATMENT OF FUNCTIONAL INTESTINAL OCCLUSION IN THE EARLY POSTOPERATIVE PERIOD
West Kazakhstan Marat Ospanov state medical universit, The Republic of Kazakhstan, Aktobe
РЕЗЮМЕ.
Объектами наблюдения явились 47 больных в возрасте от 26 до 74 лет, перенесших стандартные оперативные вмешательства с санацией и дренированием брюшной полости и назоинтестинальной интубацией кишечника по поводу распространенного перитонита различного генеза. Для оценки эффективности комплексного лечения послеоперационного пареза кишечника использовались общепринятые клинико-лабораторные методы исследования, учитывались результаты специальных инструментальных методов исследования — электроэнтерография. Применение комбинированных препаратов для инфузионной терапии на основе многоатомных спиртов (сорбилакта) в раннем послеоперационном периоде показывает его высокую эффективность в профилактике и лечении больных функциональной кишечной непроходимостью.
КЛЮЧЕВЫЕ СЛОВА: ПОСЛЕОПЕРАЦИОННЫЙ ПАРЕЗ КИШЕЧНИКА, ПЕРИТОНИТ, СТИМУЛЯЦИЯ КИШЕЧНИКА.
Жакиев Базылбек Сагидоллаевич — д. м. н., профессор, руководитель кафедры хирургического профиля интернатуры и послевузовского обучения; тел. +77014532275; e-mail: Zhakiev1959@mail.ru Карсакбаев Утеугали Ганиевич — к. м. н., доцент кафедры хирургического профиля интернатуры и послевузовского обучения; тел. +77013548989; e-mail: karsakbaev@yandex.ru Мухамедгалиева Ботагоз Молдагалиевна — к. м. н., доцент кафедры хирургического профиля интернатуры и послевузовского обучения; тел. (7132) 54-47-11; e-mail: Ekacimov@mail.ru Келимбердиев Мирсаид Саубетович — ассистент кафедры хирургического профиля интернатуры и послевузовского обучения; тел. +77028767171; e-mail: mirsaid k0612@inbox.ru Карсакбаев Амирбек Утеугалиевич — резидент кафедры хирургического профиля интернатуры и послевузовского обучения; тел.+77080353674; e-mail: Surqut90@mail.ru
КЛЮЧЕВЫЕ СЛОВА: POSTOPERATIVE ENTEROSTPARESIS, PERITONITIS, STIMULATION OF INTESTINE.
ВВЕДЕНИЕ.
Принципиальные изменения в понимании патогенеза и закономерностей течения и развития инфекционного процесса в брюшной полости позволили сконцентрировать пристальное внимание и отношение хирургов к функциональным расстройствам желудочно-кишечного тракта в раннем послеоперационном периоде. Частота послеоперационных парезов кишечника варьирует от 4 до 75% .
Своевременное восстановление моторики ЖКТ является тестом успешности выполненной операции. Несвоевременное разрешение моторных нарушений кишечника становится одной из основных причин тяжелых послеоперационных осложнений, таких как несостоятельность кишечных швов, перитонит, прогрессирующая интоксикация и т. д. . По образному выражению Моше Шайна: «Пока живот открыт, хирург контролирует его, как только вы его закрыли — он контролирует вас».
Множество научных работ как отечественных, так и зарубежных ученых, посвящённых решению этой проблемы, а также наличие разнообразных методов лечения (электростимуляция, перидуральная анестезия, интубация кишечника с целью наружного дренирования) указывает на несостоятельность общепринятых стимулирующих средств . Помимо использования чисто хирургических способов, возникла необходимость в мониторинге и коррекции функциональных нарушений желудочно-кишечного тракта (ЖКТ), поэтому исследования, проводимые в этом направлении, лишь подчёркивают актуальность проблемы.
В этой связи вызывает интерес использование комбинированных препаратов для инфузионной терапии на основе многоатомных спиртов. Одной из таких инфузионных сред является сорбилакт .
ЦЕЛЬ ИССЛЕДОВАНИЯ — изучение влияния сорбилакта на моторно-двигательную функцию кишечника в раннем послеоперационном периоде.
МАТЕРИАЛЫ И МЕТОДЫ.
Объектами наблюдения явились 47 больных в возрасте от 26 до 74 лет, которым выполнялись стандартные оперативные вмешательства с санацией и дренированием брюшной полости и назоинтести-нальной интубацией кишечника, оперированных по поводу распространенного перитонита различного генеза. Основную группу наблюдаемых составили 27 больных, у которых в составе комплексного лечения в послеоперационном периоде применялся сорбилакт. Контрольной группе (20 больным) проводили стандартную терапию. Сравниваемые группы идентичны.
Основной группе больных, начиная с первых суток после оперативного вмешательства, внутривенно капельно вводили сорбилакт со скоростью 40-60 капель в минуту 2 раза в сутки.
Для объективизации оценки эффективности применения сорбилакта в комплексном лечении послеоперационного пареза кишечника использовались общепринятые клинико-лабораторные, биохимические методы исследования, учитывались результаты специальных лабораторных и инструментальных методов исследования: уровня молекул средней массы, определение ЛИИ, электроэнтеро-графия. В данном сообщении нами приводятся результаты электроэнтерографии.
Для электроэнтерографии (ЭЭнГ) использовался российский аппарат электрогастроэнтерограф ЭГСЭ-4М с полосой пропускания частот 0,02-0,20 Гц. Электроэнтерограмма записывалась в течение 1015 минут. Обработка кривых электроэнтерограм-мы осуществлялась по частоте и амплитуде волн. При этом выделялись два вида ритмов — медленный и быстрый.
Первый из них — редкие большие волны, с высоким потенциалом, отражающие перистальтические сокращения кишечника, второй — мелкие зубцы, равномерные по амплитуде, связаны с проявлением биотоков маятникообразных движений. Общая суммарная биоэлектрическая активность (СБАо) представляет собой сумму биоэлектрической активности медленных и быстрых ритмов соответственно (СБА м. р. и СБА б. р).
ОБСУЖДЕНИЕ ПОЛУЧЕННЫХ ДАННЫХ.
Исходная клиническая картина моторной функции кишечника в обеих сравниваемых группах характеризовалась резким снижением или отсутстви-
ем перистальтики кишечника. В основной группе аускультативные признаки перистальтики кишечника появлялись уже в первые сутки, но они были неустойчивыми, стойкий уровень перистальтики отмечен в среднем на 2-3 сутки после операции, в это же время отмечено отхождение газов, на 3-4 сутки самостоятельный стул.
В обеих группах больных объём отделяемого по назоинтестинальному зонду в первые сутки после операции составлял в среднем 1000-1200 мл. В основной группе больных, начиная со вторых суток, отмечалась тенденция к уменьшению объёма кишечного отделяемого, тогда как в сравниваемой группе практически оставалась на том же уровне (800-1000 мл). Уменьшение отделяемого по назоин-тестинальному зонду и восстановление моторной функции кишечника у больных основной группы позволило удалять зонд уже на 3 сутки. У контрольной же группы удаление интистенального зонда осуществлялось на 5-6 сутки.
Положительная динамика моторно-эвакуаторной функции кишечника коррелировала с позитивными изменениями общего состояния больного (нормализация пульса, температуры тела, частоты дыхания, биохимических анализов крови, лейкоцитоза, ЛИИ).
Вышеописанная положительная динамика мо-торно-эвакуаторной функции кишечника нашла подтверждение и результатами электроэнтерограм-мы кишечника, которые фиксировались дважды — до введения сорбилакта и через 1 час после процедуры. Оценка эффективности лечебной процедуры осуществлялась сравниванием результатов этих же исследований и у контрольной группы больных в те же временные промежутки.
Исходно, т. е. в 1-е сутки послеоперационного периода у больных обеих групп, по данным ЭЭнГ выявлено резкое снижение или отсутствие перистальтики кишечника, что связано с исходным парезом, интоксикацией и с травматизацией во время операции. На электроэнтерограммах отмечались редкие, аритмичные низкоамплитудные колебания электрических волн, практически представляющие изолинию с редкими слабыми колебаниями, общая суммарная биоэлектрическая активность равнялась 0,089±0,005 мВ/мин., при норме от 0,13±0,008 до 0,4±0,2 мВ/мин.
После первой процедуры введения сорбилакта отмечались некоторые усиления активности кишечника, что выражалось нарастанием амплитуды и ритмичным чередованием больших и малых волн, и суммарная биоэлектрическая активность составила 0,150±0,006 мВ/мин. Однако они были непродолжительными (7-8 часов) и неустойчивыми. На 2-3 сутки отмечалось постепенное нарастание
амплитуды и частоты больших и малых волн, и СБАо составляла 0,120±0,005 и 0,250±0,007 мВ/мин. соответственно.
Исследование ЭЭнГ на 2-3 сутки показало, что перед очередной лечебной процедурой сохраняется достигнутый накануне уровень активности перистальтики, что подтверждается появлением отчетливых клинических признаков восстановления моторно-двигательной активности кишечника (перистальтические шумы, отхождение газов), которые полностью нормализуются к 3-4 суткам послеоперационного периода. К этому сроку значительно уменьшается количество отделяемого из интубационного кишечного зонда, что свидетельствует о восстановлении всасывающей функции кишечника, улучшается общее состояние больных, исчезают признаки интоксикации, улучшаются показатели лейкограммы.
В контрольной группе больных даже на 3-и сутки СБАо кишечника составляет 0,150±0,007 мВ/мин., тогда как в основной группе этот показатель достигает 0,250±0,007 мВ/мин.
В этой группе больных под влиянием комплексной терапии, программированных озонолапароса-наций происходит постепенное восстановление моторной активности кишечника, достигая нормальных величин к 7-8 суткам.
ВЫВОДЫ.
Применение комбинированных препаратов для инфузионной терапии на основе многоатомных спиртов (сорбилакта) в раннем послеоперационном периоде показывает его высокую эффективность в профилактике и лечении больных функциональной кишечной непроходимостью.
ЛИТЕРАТУРА:
1. Алиев, М. А. Хирургия острой кишечной непроходимости / М. А. Алиев, Ю. Л. Шальков. — Ал-маты : Ыл1м, 1996. — 255 с.
3. Гальперин, Ю. М. Парезы, параличи и функциональная непроходимость кишечника / Ю. М. Гальперин. — М.: Медицина, 1975. — 219 с.
УДК: 616.61-089.843
Б. С. ЖАКИЕВ1, Г. М. КУТТЫМУРАТОВ2, Ж. АЛМУРЗАУЛЫ3, К. К. ЕРМАГАМБЕТОВ3
ТРАНСПЛАНТАЦИИ ПОЧКИ ОТ ЖИВОГО РОДСТВЕННОГО ДОНОРА В УСЛОВИЯХ ОБЛАСТНОЙ КЛИНИЧЕСКОЙ БОЛЬНИЦЫ
1 — Западно-Казахстанский государственный медицинский университет имени Марата Оспанова, г. Актобе, Республика Казахстан
2 — Национальный научный центр онкологии и трансплантологии, г. Астана, Республика Казахстан
3 — Актюбинская областная больница, Республика Казахстан
B. S. ZHAKYEV1, G. M. KUTTYMURATOV2, ZH. ALMURZAULY3, K. K. YERMAGAMBETOV3
OUR PRIMARY EXPERIENCE OF KIDNEY TRANSPLANTATION FROM LIVING RELATIVE DONOR
1 — Marat Ospanov West-Kazakhstan State Medical University, Aktobe, Kazakhstan
2 — National scientific center of an oncology and transplantology, Astana, Kazakhstan
М.М. МИННУЛЛИН1, Д.М. КРАСИЛЬНИКОВ2, А.П. ТОЛСТИКОВ1
1Республиканская клиническая больница МЗ РТ, 420064, г. Казань, Оренбургский тракт, д. 138
2Казанский государственный медицинский университет, 420012, г. Казань, ул. Бутлерова, д. 49
Красильников Дмитрий Михайлович — доктор медицинских наук, профессор, заведующий кафедрой хирургических болезней №1, тел. (843) 231-20-57, e-mail:
Толстиков Алексей Петрович — кандидат медицинских наук, врач-хирург, тел. (843) 231-21-66, e-mail:
Изучены результаты хирургического лечения 546 пациентов с острой кишечной непроходимостью. Установлен диагностический алгоритм, а также методика выбора оптимальных вариантов хирургических пособий у пациентов с острой кишечной непроходимостью. Сформулированы современные принципы диагностики и хирургического лечения больных с острой толстокишечной непроходимостью, спаечной и странгуляционной тонкокишечной непроходимостью. В диагностике острой спаечной тонкокишечной непроходимости решающее значение имеет эндоскопическая катетерная контрастная энтерография, при острой толстокишечной непроходимости — экстренная колоноскопия. Основными критериями в выборе объема и вида операции являются наличие распространенного перитонита, стадия бластоматозного процесса. Экстраперитонизация энтероэнтероанастомоза снижает частоту несостоятельности швов.
Ключевые слова: острая кишечная непроходимость, спайки, опухоли кишечника, диагностика, хирургическое лечение.
M.M. MINNULLIN1, D.M. KRASILNIKOV2, А.P. TOLSTIKOV1
2Kazan State Medical University, 49 Butlerov St., Kazan, Russian Federation, 420012
Содержание
- Обеспечение перорального или энтерального питания в послеоперационном периоде
- Цели изучения
- Основные положения
- 1. Послеоперационный парез желудочно-кишечного тракта
- 2. Торакальная эпидуральная аналгезия
- 3. Отмена опиоидов
- 4. Периоперационный баланс жидкости
- 5. Другие вмешательства для ограничения возможности возникновения послеоперационной динамической непроходимости кишечника
- 6. Желудочно-кишечная функция после хирургических вмешательств на толстой кишке в протоколах быстрого восстановления после операции
- Тест на самооценку
Acute intestinal obstruction. Diagnostics. Surgical treatment
Minnullin M.М. — Cand. Med. Sc., First Deputy Chief Doctor, tel. (843) 231-20-60, e-mail:
Krasilnikov D.М. — D. Med. Sc., Professor, Head of the Surgery Department №1, tel. (843) 231-20-57, e-mail:
Tolstikov A.Р. — Cand. Med. Sc., surgeon, tel. (843) 231-21-66, e-mail:
Key words: acute intestinal obstruction, adhesions, intestine tumors, diagnostics, surgical treatment.
Своевременная диагностика и выбор оптимального варианта хирургического лечения больных с острой кишечной непроходимостью (ОКН) являются одной из самых сложных и актуальных проблем в неотложной хирургии . Несмотря на значительные достижения в современной хирургии, разработку и внедрение новых методов ранней диагностики и хирургического лечения больных с ОКН, наблюдается большое количество неудовлетворительных результатов и летальных исходов при данной патологии. Все это в итоге обусловливает необходимость поиска и клинического применения достоверных способов определения вида и уровня кишечной непроходимости, выбора адекватных оперативных пособий в каждом конкретном случае, усовершенствования существующих алгоритмов диагностики и лечения, способствующих спасению жизни пациентов .
Материалы и методы
С 2009 по 2014 г. в отделении абдоминальной хирургии ГАУЗ «Республиканская клиническая больница МЗ РТ» находились на лечении 546 пациентов с различными видами острой кишечной непроходимости (ОКН). У 81 (14,8%) больного в результате проведенных лечебно-диагностических мероприятий ОКН была разрешена консервативно, в основном благодаря успешно проводимой декомпрессии верхних отделов желудочно-кишечного тракта (ЖКТ). Оперированы 464 пациента, из них 97 (21%) больных — по поводу острой обтурационной кишечной непроходимости опухолевого генеза (ОКН опухолевого генеза), 130 (28%) — странгуляционной кишечной непроходимости, 235 (50,7%) — острой спаечной кишечной непроходимости (ОСКН), два (0,3%) — инвагинации. Причинами развития острой странгуляционной кишечной непроходимости в 109 (84,1%) наблюдениях являлись ущемленные вентральные грыжи различной локализации, шесть человек (4,4%) поступили с заворотом тонкой и 15 (11,5%) — сигмовидной кишки.
Возраст оперированных пациентов составлял от 18 до 87 лет, причем мужчин было вдвое больше, чем женщин. Установлена прямо пропорциональная связь между сроками поступления пациентов в стационар с момента начала заболевания, их возрастом, наличием сопутствующих заболеваний и послеоперационной летальностью. Сроки поступления пациентов в стационар при различных видах ОКН приведены в табл. 1.
Таблица 1.
Сроки поступления пациентов в стационар
Выполнение программы диагностики у больных с ОКН начиналось с изучения клинико-объективных и лабораторных данных. При непроходимости опухолевого генеза характерным было снижение веса, наличие схваткообразных болей, вздутие живота, неотхождение газов и стула. Болевой синдром при данном виде непроходимости отличался тем, что после прохождения перистальтической волны отдела кишки, обтурированного опухолью, боль полностью исчезала и пациенты были спокойны до момента подхода новой волны. Интервал между приступами болей достигал 20 минут, на этом фоне появляется видимая перистальтика кишечника, вызывая асимметрию живота (симптом Валя).
При странгуляционной кишечной непроходимости патогномоничным признаком является наличие выраженных схваткообразных болей в животе на фоне имеющегося постоянного болевого синдрома. Присутствие тошноты, чувства переполнения и тяжести в эпигастрии, неукротимой рвоты характерно высокой ОСКН. Кроме того, при высокой тонкокишечной непроходимости у больного не будет вздутия живота, тимпанита при перкуссии, что характерно низкой кишечной непроходимости. У пациентов отходят газы, отмечается наличие стула, в связи с имеющимся кишечным содержимым в тонкой и толстой кишке ниже места препятствия, что часто приводит хирургов к неправильной интерпретации клинической картины заболевания, поздней диагностики и несвоевременной операции.
Лабораторные исследования, проводимые при ОКН, имеют определяющее значение для оценки нарушений гомеостаза и всем больным выполнялись общие анализы крови и мочи, определялось количество молекул средних масс и лейкоцитарного индекса интоксикации. В большинстве наблюдений определялись высокий лейкоцитоз и нейтрофилез, нарастание количества молекул средних масс, лейкоцитарного индекса интоксикации.
Определяющее значение в диагностике ОКН имеют лучевые методы исследования. Пациентам, поступившим с подозрением на ОКН, выполняли обзорную рентгенографию органов брюшной полости, с целью выявления наличия раздутых петель тонкой и толстой кишки, содержащих газ и жидкость и имеющих вид опрокинутых чаш (чаши Клойбера). При тонкокишечной непроходимости их горизонтальный размер значительно превышает вертикальный, у больных с толстокишечной непроходимостью рентгенологическая картина совершенно иная — вертикальный размер многократно больше горизонтального. Кроме того, для тонкокишечной непроходимости характерно локализованное расширение «отключенной» петли тонкой кишки, поперечная исчерченность кишки, напоминающая скелет селедки, вследствие отека и увеличения расстояния между керкринговыми складками (симптом Кейси), стойкая фиксация раздутой петли при исследовании в латеропозиции. Однако следует подчеркнуть, что информативность данного метода исследования при различных видах ОКН не превышает 45%.
Одними из распространенных и убедительных в диагностике ОКН являются рентгеноконтрастные исследования. Наиболее информативной и достоверной при ОСКН считаем разработанную в нашей клинике методику эндоскопической катетерной контрастной энтерографии (ЭККЭ) (Красильников Д.М., 1992). После промывания желудка и эвакуации желудочного содержимого через манипуляционный канал эндоскопа проводится до связки Трейца полихлорвиниловый катетер. В дальнейшем по катетеру под давлением вводится 500 мл жидкого контраста «БАР-ВИПС» или водорастворимый контраст. Длительность исследования не превышает 1,5 часа. Достоверность диагностики при ОСКН составляет 98%. 235 пациентам с подозрением на ОСКН выполнена ЭККЭ, что за короткий промежуток времени дало возможность установить вид и уровень непроходимости и решить вопрос об показанности оперативного лечения.
При ОКН опухолевого генеза основными методами диагностики являются экстренная колоноскопия, реже ирригография. Проведение экстренной колоноскопии после предварительной подготовки толстой кишки у 69 больных позволило в короткий промежуток времени установить уровень непроходимости, а в 15 случаях временно разрешить кишечную непроходимость путем проведения эндоскопической электрохирургической реканализации пораженного опухолью участка толстой кишки. У 11 больных при проведении экстренной колоноскопии удалось выполнить деторзию заворота сигмовидной кишки. 25 пациентам с подозрением на обтурационную кишечную непроходимость выполнена ирригография.
Ультразвуковое исследование (УЗИ) органов брюшной полости в настоящее время служит скрининговым методом диагностики ОКН. При проведении УЗИ удается оценить состояние кишки, определить ее диаметр, толщину стенки, ширину складок слизистой и характер перистальтических движений. Так, при тонкокишечной непроходимости диаметр кишки составляет от 2,5 до 5,5 см, толщина стенки тонкой кишки 3-4 мм. При нарастании клиники кишечной непроходимости увеличивается диаметр кишки, уменьшается толщина ее стенки, по характеру перистальтических движений судим о передвижении жидкого содержимого в просвете кишки. Ускоренные перистальтические движения тонкой кишки характерны при обтурационной кишечной непроходимости, гораздо реже ускоренная перистальтика отмечается у больных со странгуляционной кишечной непроходимостью, замедление или полное отсутствие перистальтических движений характерно для паралитической кишечной непроходимости.
Большое внимание при подозрении на ОСКН уделяется наличию послеоперационных рубцов, свидетельствующих о ранее перенесенных операциях. При УЗИ устанавливается наличие висцеро-париетальных сращений полых органов, степень их подвижности, определяется наиболее безопасная траектория установки первого троакара и создания пневмоперитонеума при проведении видеолапароскопического адгезиолизиса. УЗИ органов брюшной полости выполнено 546 (100%) больным, при этом у 437 (80%) пациентов в брюшной полости обнаружена свободная жидкость. В 355 случаях петли тонкой кишки были расширены до 5,5 мм в диаметре. У 212 (38,8%) пациентов отмечались ускоренные перистальтические движения, в 138 (25,2%) случаях — замедление перистальтики или полное ее отсутствие.
Видеолапароскопическое исследование является эффективным методом диагностики в начальной стадии ОКН, в частности странгуляционной и ОСКН. Большие возможности открываются при использовании данного метода с целью установления не только диагноза, но и динамического наблюдения в послеоперационном периоде, что позволяет значительно сократить продолжительность клинико-рентгенологического обследования, а в некоторых случаях при помощи видеолапароскопического адгезиолизиса устранить явления ОСКН . С целью диагностики видеолапароскопическое исследование выполнено 75 пациентам. Из них 62 больным был установлен диагноз ОСКН, 13 — заворот тонкой и сигмовидной кишки. При этом 29 пациентам кишечная непроходимость была разрешена путем лапароскопического адгезиолизиса, с эндоскопической декомпрессией верхних отделов ЖКТ.
Результаты лечения больных с ОКН
Восьмидесяти пациентам, поступившим в первые сутки с момента начала заболевания, в результате проведенного комплекса лечебно-диагностических мероприятий удалось купировать явления ОКН консервативным путем. Из них 15 больным при проведении экстренной колоноскопии выполнена эндоскопическая электрохирургическая реканализация участка толстой кишки, стенозированная опухолью, 11 пациентам выполнена деторзия заворота сигмовидной кишки. В 54 случаях ОСКН также была разрешена консервативным путем. 25 пациентам выполнен видеолапароскопический адгезиолизис с назоинтестинальной декомпрессией верхних отделов ЖКТ.
Все операции по поводу ОКН выполнялись под эндотрахеальным наркозом, из традиционного срединного доступа. Важным этапом в ходе операции по поводу странгуляционной и спаечной кишечной непроходимости является определение жизнеспособности ущемленной петли кишки. С этой целью в клинике наряду с визуальной оценкой жизнеспособности органа и отогреванием его теплыми растворами применяем методики трансиллюминации и лазерной спектроскопии.
Из 109 больных с ущемленными вентральными грыжами у 72 пациентов была ущемлена петля тонкой кишки, у 17 — слепая кишка с терминальным отделом подвздошной кишки, в 20 случаях — сигмовидная кишка. 32 пациентам потребовалась резекция тонкой кишки (20 больным резекция тонкой кишки с анастомозом «бок в бок», 12 — резекция тонкой кишки с выведением илеостомы), в четырех случаях выполнена правосторонняя гемиколэктомия с выведением илеостомы, в трех — правосторонняя гемиколэктомия с наложением илеотрансверзоанастомоза. Пяти больным по поводу некроза сигмовидной кишки выполнена операция Гартмана. При больших ущемленных вентральных грыжах операцию заканчивали ненатяжной герниопластикой с использованием сетчатого имплантата. Оперативные вмешательства при ОКН опухолевого генеза чаще выполняем в два этапа (табл. 2).
Таблица 2.
Методы операций при обтурационной кишечной непроходимости опухолевого генеза
| Методы операций | Количество операций (абс.) | % |
| Илеостомия | 12 | 14,4 |
| Трансверзостомия | 5 | 5,4 |
| Наложение илеотрансверзоанастомоза | 6 | 7,7 |
| Сигмостомия | 5 | 6,0 |
| Правосторонняя гемиколэктомия, илеостомия | 8 | 9,7 |
| Правосторонняя гемиколэктомия, илеотрансверзостомия | 6 | 7,5 |
| Левосторонняя гемиколэктомия, колостомия | 9 | 11,4 |
| Операция Гартмана | 31 | 37,9 |
| Всего | 82 | 100 |
Выбор объема и метода оперативного вмешательства осуществляем в зависимости от стадии перитонита, распространенности бластоматозного процесса (табл. 3).
Таблица 3.
Выбор метода оперативного вмешательства при обтурационной кишечной непроходимости опухолевого генеза
| Локализация опухоли | Операбельность | Наличие распространенного
перитонита |
Метод операции |
| Правая половина толстой кишки | Операбельная | Нет | Гемиколэктомия + илеостомия |
| Есть | Илеостомия | ||
| Неоперабельная | Нет | Обходной анастомоз или илеостомия | |
| Есть | Илеостомия | ||
| Поперечная ободочная кишка | Операбельная | Нет | Резекция ободочной кишки + колостомия |
| Есть | Илео- или колостомия | ||
| Неоперабельная | Нет | Обходной илеодесцендоанастамоз или илео- или колостомия | |
| Есть | Илео- или колостомия | ||
| Левая половина толстой кишки | Операбельная | Нет | Гемиколэктомия + колостомия |
| Есть | Трансверзостомия | ||
| Неоперабельная | Нет | Трансверзостомия | |
| Есть | Трансверзостомия | ||
| Сигмовидная кишка | Операбельная | Нет | Резекция сигмы, операция Гартмана |
| Есть | Колостомия | ||
| Неоперабельная | Нет | Колостомия | |
| Есть | Колостомия | ||
| Экстраорганное расположение опухоли | Операбельная | Нет | Удаление опухоли, трансанальная интубация или колостомия |
| Есть | Колостомия | ||
| Неоперабельная | Нет | Колостомия | |
| Есть | Колостомия |
Методы оперативных вмешательств, произведенные у больных с ОСКН, представлены в табл. 4.
Таблица 4.
Методы оперативных вмешательств при ОСКН
| Методы операций | Число оперированных больных | % |
| Висцеролиз | 13 | 7 |
| Висцеролиз + закрытая интубация тонкой кишки (в т.ч. лапароскопический адгезиолизис) | 70 | 38,4 |
| Висцеролиз + резекция различных сегментов тонкой кишки | 29 | 16,3 |
| Висцеролиз + резекция различных отделов тонкой кишки + закрытая интубация тонкой кишки | 48 | 26,7 |
| Висцеролиз + гастроинтестинальная интубация тонкой кишки по Ю.М. Дедереру | 21 | 11,6 |
| Всего | 181 | 100 |
Обязательным в ходе операции считаем проведение декомпрессии и интубации кишечника, при этом предпочтение отдаем выполнению закрытой назоинтестинальной интубации. Внутреннее дренирование — шинирование кишечника значительно улучшает результаты оперативных вмешательств, снижает кишечную гипертензию, позволяет хорошо опорожнять неперистальтирующий кишечник, нормализует кровообращение, обеспечивает функционально выгодное положение кишки, способствует раннему восстановлению моторики, осуществлению раннего энтерального питания. Лучшие результаты при рецидиве заболевания или при ранней послеоперационной спаечной кишечной непроходимости (РПСКН) отмечены при проведении двухпросветного зонда через гастростому по Ю.М. Дедереру . Именно при таком дренировании минимально число легочных осложнений. Кроме того, появляется возможность длительно сохранять зонд в просвете тонкой кишки (в среднем до 14 дней). Данный метод декомпрессии нами применен 15 пациентам, причем срок нахождения гастроинтестинального зонда в одном наблюдении составил 30 дней. С целью профилактики несостоятельности швов межкишечных анастомозов, особенно когда они были сформированы при сомнительном кровоснабжении кишки, распространенном перитоните, выраженных водно-электролитных нарушениях, проводили их экстраперитонизацию (патент №2445022, 2012 «Способ профилактики несостоятельности швов энтероэнтероанастомоза»). Экстраперитонизация энтероэнтероанастомоза выполнена у 17 пациентов.
Осложнения в раннем послеоперационном периоде наблюдали у 87 (18,6%) пациентов. У 20 пациентов возникла несостоятельность энтероэнтероанастомоза, из них в шести случаях несостоятельность швов развилась у пациентов, которым была выполнена экстраперитонизация межкишечного анастомоза; в дальнейшем у данных пациентов сформировались наружные кишечные свищи, закрывшиеся самостоятельно, в 9 случаях — внутрибрюшное кровотечение, 10 пациентов повторно оперированы по поводу РПСКН. Нагноение послеоперационной раны наблюдали в 48 случаях.
Общая летальность при ОКН составила 11,9%, наибольшая в группе больных, оперированных по поводу ОКН опухолевого генеза, — 21,1%. Столь высокая летальность обусловлена поздним обращением больных в стационар с момента начала заболевания, пожилым возрастом пациентов и наличием тяжелой сопутствующей патологии (табл. 5).
Таблица 5.
Причины смерти больных при ОКН
| Причина смерти | Число случаев | |
| Абсолютное число | % | |
| Прогрессирующий перитонит | 16 | 25 |
| Местные гнойные осложнения, сепсис | 11 | 16,7 |
| Тромбоэмболические осложнения | 16 | 25 |
| Острый инфаркт миокарда | 10 | 14,6 |
| Печеночно-почечная недостаточность | 12 | 18,7 |
| Всего | 65 | 100 |
Выводы
1. В диагностике острой кишечной непроходимости наряду с результатами клинико-объективных и лабораторных данных определяющее значение имеют колоноскопия у больных с острой толстокишечной непроходимостью, эндоскопическая катетерная контрастная энтерография при острой тонкокишечной непроходимости.
2. Видеолапароскопия является эффективным методом диагностики и лечения больных при различных видах острой кишечной непроходимости.
3. Оперативное лечение при обтурационной острой кишечной непроходимости опухолевого генеза чаще выполняется в два этапа. Основными критериями в выборе объема и метода операции являются наличие распространенного перитонита, стадия бластоматозного процесса.
4. Обязательным в ходе операции при острой спаечной кишечной непроходимости считаем проведение закрытой декомпрессии и интубации кишечника двухпросветным зондом. При развитии ранней послеоперационной спаечной кишечной непроходимости необходимо осуществлять продленную интубацию тонкой кишки через гастростому по Ю.М. Дедереру.
5. Экстраперитонизация энтероэнтероанастомоза значительно снижает вероятность развития несостоятельности швов межкишечного анастомоза.
ЛИТЕРАТУРА
Обеспечение перорального или энтерального питания в послеоперационном периоде |
printable version |
Mattias Soop
Цели изучения
- Понять причины послеоперационного пареза желудочно-кишечного тракта;
- Подробно изучить периоперационные вмешательства, способствующие послеоперационному функционированию кишки;
- В частности, изучить использование эпидуральной аналгезии и мультимодальной аналгезии, помогающих функционированию кишечника; важность жидкостного баланса и роль, если она существует, прокинетических препаратов;
- Рассмотреть дополнительные виды вмешательства, которые можно использовать.
Основные положения
- Послеоперационного пареза кишечника можно избежать;
- Основными причинами, на которые можно воздействовать, являются подавленная симпатическая активность, манипуляции с кишечником, экзогенные и эндогенные опиоиды и перегрузка жидкостью;
- Торакальная эпидуральная анестезия обеспечивает послеоперационное функционирование кишечника путём блокирования ингибирующих рефлексов, высвобождения катехоламинов и устраняя потребность в систематической опиоидной аналгезии;
- Нестероидные антивоспалительные препараты и парацетамол снижают потребность в опиоидах с окончанием эпидуральной аналгезии;
- Именно достижение послеоперационного жидкостного баланса, а не перегрузка, способствует предотвращению послеоперационного пареза кишечника;
- Прокинетические препараты не играют роли при терапии послеоперационного пареза кишечника, исключая окись магния, которая может иметь положительный эффект;
- Объединяя некоторые из вышеуказанных мероприятий в протокол, возможно добиться нормального времени желудочно-кишечного транзита после операций на толстой кишке.
1. Послеоперационный парез желудочно-кишечного тракта
Парез желудочно-кишечного тракта стал основной проблемой при традиционном хирургическом лечении, ограничивающей переносимость перорального и энтерального питания (1). Время восстановления ЖКТ часто составляет от 2-5 дней. Задержка с пероральным или энтеральным питанием значительно замедляет восстановление и повышает риск инфекционных осложнений по сравнению с ранним введением питания. Причины послеоперационного желудочно-кишечного паралича разнообразны. Основными причинами являются подавленная симпатическая активность в ответ на боль и рассечение брюшины, местное высвобождение нейротрансмиттеров в ответ на манипуляции кишечника, непосредственный ингибирующий эффект эндогенных и экзогенных опиоидов и перегрузки жидкостью. На большинство данных воздействий можно влиять с помощью периоперационных вмешательств, уменьшающих и даже устраняющие послеоперационную динамическую непроходимость кишечника.
2. Торакальная эпидуральная аналгезия
Высвобождение катехоламинов происходит во время и после хирургического вмешательства, как системно, из мозгового вещества надпочечников в ответ на ощущение тревоги и боль, так и местно, из симпатических нервных окончаний в ответ на рассечение висцеральной брюшины. Мозговое вещество надпочечника иннервируется через сегменты T5-T11, тонкий кишечник через T9-T12 и толстая кишка через T11-L2.
Рис. 1 Рассечение брюшины и послеоперационная динамическая непроходимость кишечника.
• С рассечением брюшины запускаются симпатические висцеро-висцеральные рефлексы, ингибирующие подвижность.
• Срединный торакальный эпидуральный блок ингибирует афферентные и эфферентные окончания.
• Должна использоваться регионарная анестезия, а не только опиаты.
Не удивительно, что эпидуральный блок с регионарной анестезией на средне-торакальном уровне эффективно снижает циркулирующие уровни катехоламинов (4, 5) и значительно сокращает продолжительность послеоперационного пареза кишечника (6) по сравнению с периодически вводимыми опиоидами.
Рис. 2 Срединная-торакальная эпидуральная анестезия требуется для симпатического блока кишечного тракта.
• Симпатэктомия с регионарной анестезией требует средне-торакального доступа
• Не было показано положительного воздействия низкой торакальной эпидуральной анестезии на послеоперационную кишечную динамическую непроходимость.
• Не удивительно, что исследования, использующие нижнюю торакальную эпидуральную анестезию, не продемонстрировали положительного эффекта эпидуральной аналгезии на непроходимость кишечника.
Вследствие иннервации мозгового вещества надпочечника и кишечника, эпидуральный блок может быть скорее срединным-торакальным, чем нижним-торакальным или поясничным (7-9) для получения эффективного симпатического блока. Следовательно, это требует более высокого уровня эпидурального блока, чем тот, который необходим для одной лишь аналгезии в нижней абдоминальной и тазовой хирургии. Для повышения обезболивающего эффекта эпидурально введённого местного анестетика в эпидуральный раствор часто добавляются опиоиды. Несмотря на то, что добавление низкой дозы опиоидов в эпидуральный инфузат может способствовать возникновению послеоперационной непроходимости кишечника, данное воздействие невелико (7) и оно позволяет использовать более низкие дозы эпидурально вводимых местных анестетиков, сводя плегию нижних конечностей до минимума.
3. Отмена опиоидов
Парализующий эффект опиоидов в кишечнике в четыре раза сильнее их обезболивающего эффекта. Один из плюсов использования эпидуральной аналгезии это то, что она сокращает потребность в послеоперационной системной опиоидной аналгезии. При прекращении использования эпидуральной аналгезии нестероидные антивоспалительные препараты (НСПВП) и парацетамол сокращают потребность в опиоидной аналгезии, а также, возможно, сокращают послеоперационный парез кишечника. Однако, несмотря на то, что систематического введения опиоидов можно избежать при помощи мультимодальной аналгезии, основанной на эпидуральной аналгезии, нестероидных противовоспалительных препаратах и парацетомоле, производство эндогенных опиоидов важно в послеоперационный период (11). Было показано, что активные локальные пероральные опиоидные антагонисты, будучи всего лишь экспериментальными cредствами, значительно снижают возможность возникновения послеоперационной динамической непроходимости кишечника (12).
4. Периоперационный баланс жидкости
Традиционно было принято щедро замещать реальные и предполагаемые потери жидкости во время и после хирургического вмешательства. Недавно было выяснено, что данная практика, возникшая в результате лечения больных с травмами, является вредной для функционирования ЖКТ (13) и послеоперационных осложнений (14) в плановой хирургии.
Рис. 3 Послеоперационный баланс жидкости и натрия поддерживает желудочно-кишечную функцию.
20 больных подверглись резекции толстой кишки
• Стандартный режим — более 3 литров жидкости, более 154 ммоль натрия в сутки
• Ограниченный режим — менее 2 литров, менее 77 ммоль натрия в сутки
Исходы: частота стула и длительность пребывания в стационаре
Из исследований на животных очевидно, что подобная перегрузка жидкостью вызывает отёк и паралич стенки желудка. У людей периоперационный жидкостный режим, направленный на достижение баланса жидкости, а не на обычную перегрузку жидкостью, показал значительное снижение времени восстановления функции кишечника и его очищение, следующее за резекцией толстой кишки. Тремя факторами, частично отвечающими за повышенную потребность в периоперационных инфузиях, являются: 1) предоперационная подготовка кишечника; 2) предоперационное ночное голодание; 3) эпидуральная аналгезия. Негативные последствия данных факторов можно свести до минимума при современной периоперационной подготовке. На данный момент известно, что при хирургических вмешательствах на толстой кишке обычная предоперационная подготовка кишечника не имеет положительного клинического эффекта и даже повышает риск несостоятельности анастомоза (15). Также положительного эффекта не показало предоперационное ночное голодание. Эпидурально-индуцированную вазодилатацию предпочтительнее лечить вазопрессорами, а не жидкостной нагрузкой (16).
5. Другие вмешательства для ограничения возможности возникновения послеоперационной динамической непроходимости кишечника
Предоперационное обучение пациентов и тренинги по сравнению с обычными успокаивающими разговорами показали значительный положительный эффект в послеоперационном восстановлении, например, раннее восстановление функционирования кишечника (17). Это простое и недорогое лечебное воздействие, которое легко применить. Прокинетические препараты продемонстрировали разочаровывающий результат при воздействии на послеоперационный парез кишечника (10). В некоторых исследованиях цисаприд обладал значительным клиническим эффектом, но он не выводился из организма. Метоклопрамид, всё ещё будучи популярным, не показал какого-либо эффекта на послеоперационную динамическую непроходимость кишечника (10).
Рис. 4 Слабительные средства после операции сокращают время восстановления желудочно-кишечной функции.
У пациентов с аппендэктомией было проведено проведено двойное слепое рандомизированное исследование:
• Послеоперационный бисакодил в низких дозах 10 мг (23);
• Плацебо (23).
Назначенный в послеоперационном периоде слабительный препарат показал значительное снижение времени восстановления функционирования кишки в двойном слепом исследовании у пациентов после аппендэктомии (18).
Послеоперационная стимуляция кишечника оксидом магния стало частью лечебных протоколов в плановой хирургии толстой кишки в течение нескольких лет без увеличения роста осложнений (19).
Хирургическая техника может влиять на продолжительность послеоперационного желудочно-кишечного пареза. Интересно то, что обычные манипуляции на тонкой кишке вызывают то же распространение и продолжительность послеоперационной кишечной динамической непроходимости, что и обширное рассечение правой или левой половины толстой кишки у приматов (20). Таким образом, попытки минимизировать последствия хирургической травмы, такие как использование минимальных разрезов брюшной стенки, могут положительно влиять на послеоперационное функционирование кишечника. Лапароскопическая хирургия на толстой кишке по сравнению с традиционными доступами (10) может способствовать функционированию ЖКТ, хотя данный эффект не был выявлен в ходе недавнего слепого исследования в пределах протокола ускоренной реабилитации после операции (21). Обычное послеоперационное назо-гастральное дренирование не только мешает процессу перорального питания, но также увеличивает частоту послеоперационных осложнений, поэтому его стоить убрать сразу после плановой лапаротомии (22).
6. Желудочно-кишечная функция после хирургических вмешательств на толстой кишке в протоколах быстрого восстановления после операции
Протоколы ранней реабилитации после хирургического вмешательства объединяют некоторые виды лечебных процедур, описанные выше. Влияние на послеоперационное функционирование кишки впечатляет. Резекция толстой кишки никак не влияет на желудочно-кишечный транзит в протоколе, объединяющем торакальную эпидуральную аналгезию и послеоперационное использование оксида магния, по сравнению со здоровыми пациентами (3). Подобные протоколы разрешают пероральный приём твёрдой пищи и пероральные нутриционные добавки сразу же после хирургического вмешательства (23).