Парализовало руку
Вопрос исследования
Какие вмешательства способствуют восстановлению руки и кисти после перенесенного инсульта?
Актуальность
Очень часто после инсульта возникают проблемы с функцией руки (нарушения верхних конечностей). Нарушения верхних конечностей обычно включают в себя нарушения движения и координации рук, кистей и пальцев, что часто приводит к сложностям выполнения повседневных функций, таких как прием пищи, одевание и умывание. Более чем у половины людей с нарушениями в верхних конечностях после инсульта, проблемы всё ещё будут продолжаться от нескольких месяцев до нескольких лет после инсульта. Улучшение функции руки является ключевым элементом реабилитации. Было разработано множество возможных вмешательств; они включают различные упражнения или тренировки, специальное оборудование или технологии, или они могут быть представлять собой лекарство (таблетка или инъекция), назначаемое, чтобы улучшить движения руки.
Реабилитация верхних конечностей после инсульта часто включает в себя несколько различных вмешательств и обычно требует сотрудничества пациента, ухаживающих за ним и реабилитационной команды.
Мы разработали Кокрейновский обзор, чтобы помочь людям легко получить доступ к информации об эффективных вмешательствах, и помочь им сравнить эффекты различных вмешательств. Мы стремились объединить все систематические обзоры вмешательств, осуществляемых для улучшения функции верхней конечности (руки) после инсульта.
Характеристики исследований
Мы провели поиск Кокрейновских и не-Кокрейновских обзоров по эффективности вмешательств для улучшения функции руки после инсульта. Мы включили 40 систематических обзоров (19 Кокрейновских обзоров и не-Кокрейновские обзоры -числом 21). Доказательства актуальны по июль 2013 года.
Обзоры рассмотрели 18 различных типов вмешательств, а также дозу вмешательства и условия, в которых вмешательство было предоставлено. Эти обзоры различались по включенной популяции (начальное ухудшение верхней конечности и тяжесть инсульта), и по включенным группам сравнения (контрольные вмешательства, отсутствие лечения и обычная терапия).
Мы извлекли информацию о 127 сравнениях, которые были изучены в рамках обзоров. Они показали, в какой степени различные вмешательства оказывали эффект на функции верхней конечности, ухудшение верхней конечности и способность выполнять повседневную работу.
Основные результаты
В настоящее время нет доступных доказательств высокого качества для любых вмешательств, которые используются в настоящее время в повседневной практике. Доказательств недостаточно, чтобы показать, какие являются самыми эффективными для улучшения функции верхней конечности.
Доказательства среднего качества позволяют предполагать, что следующие вмешательства могут быть эффективными: двигательная терапия, индуцированная ограничением (напряжением), психоневрологическая практика, зеркальная терапия, вмешательства для сенсорных нарушений, виртуальная реальность и относительно высокие дозы повторных практических заданий. Доказательства умеренного качества также показывают, что одностороннее обучение руки (упражнения для поврежденной руки) может быть более эффективным, чем двустороннее обучение рук (выполнение того же самого упражнения обеими руками одновременно).
Некоторые свидетельства показывают, что большая доза любого вмешательства лучше, чем меньшая. Необходимы дополнительные исследования, чтобы определить оптимальную дозу вмешательства для восстановления руки.
Объединение доказательств всех доступных систематических обзоров помогло нам сделать конкретные рекомендации для будущих исследований. Эти рекомендации включают (но не ограничиваются этим) крупные рандомизированные контролируемые испытания ТИО, психоневрологической практики, зеркальной терапии и виртуальной реальности. Мы рекомендуем высоко-качественные современные обзоры и дальнейшие первичные исследования для ряда конкретных вмешательств.
Качество доказательств
Мы оценили качество доказательств как высокое в отношении одного вмешательства: вариант стимуляции мозга, называемый транскраниальная стимуляция постоянным током (микрополяризация) (tDCS), которая в настоящее время не используется повседневной практике. Эти высококачественные данные показывают, что tDCS не улучшает способность людей выполнять повседневную работу.
Мы оценили качество доказательств как умеренное для 48 сравнений (по семи отдельным вмешательствам), и как низкое или очень низкое для 76 сравнений. Причины понижения качества доказательств до среднего, низкого или очень низкого включают малые числа исследований и участников, плохое качество методологии или представления результатов исследований, включенных в обзоры, значительную неоднородность (гетерогенность, вариацию) между результатами обучения и низкое качество обзора или сообщения о методах.
Мы пришли к выводу, что настоятельно необходимы доказательства высокого качества в отношении эффективности вмешательств, позволяющих улучшить функции верхних конечностей, в частности тех вмешательств, для которых свидетельства умеренного качества позволяют в настоящее время предполагать их благоприятный эффект.
Содержание
Физиотерапевт, реабилитолог Юрий Железняк про причины болевого синдрома
Почему после инсульта возникает боль в плече?
Когда рука или нога лежачего пациента долгое время находится в одном и том же положении, мышцы и связки укорачиваются, их эластичность теряется.
Ведущим механизмом синдрома болевого плеча является перерастяжение капсулы плечевого сустава под действием силы тяжести парализованной руки. Оно возникает вследствие паралича мышц и ослабления корсетирующей функции плечевого сустава.
В таких случаях рентгеновские снимки показывают выхождение головки из суставной щели даже через несколько лет после инсульта.
Нарушение проявляется двумя ведущими симптомами: болью и контрактурами (органичениями в подвижности сустава). Боль локализуется преимущественно в плечевом суставе, надплечье, плече, лопатке и шее. Она усиливается в ночное время и при изменении погоды, а также при движении, особенно при отведении руки или при ее закладывании за спину. Вторая группа симптомов связана с контрактурами мышечно-связочного аппарата в области плечевого сустава. Это приводит к резкому ограничению отведения руки в сторону и вверх, вперед и вверх, при заведении руки за спину, за голову.
Отчего растет мышечный тонус?
Первопричина – значительное повреждение головного мозга. Вслед за этим играет роль активизация шейных тонических рефлексов в результате длительного положения на спине. Также перенапряжение в мышцах может возникать из-за чрезмерных усилий при сидении без достаточной поддержки при плохом равновесии и в момент вставания с низкой кровати, а еще – из-за раздражения ладонной поверхности.
Мышечный тонус повышает любой дискомфорт: холод, боль (в том числе и от инъекций), ощущение грязного тела, пролежни. К этому добавляются психологические факторы – стеснение от нарушения приватности, страх перед падением и болью.

Устройство для реабилитации «МОТОмед Летто 2»
Как минимизировать дискомфорт?
Медицинский персонал, а в дальнейшем ухаживающие, начиная с момента развития паралича должны создать пострадавшему от инсульта комфортные условия, ведь холод, нарушения приватности, чрезмерные усилия при сидении без поддержки или при вставании со слишком низкой кровати, травмы – все это усугубляет ситуацию. Боль мешает восстановлению навыков, приводит к боязни движения.
Человек становится зависимым от окружающих, возрастают общие стрессовые проявления – плохое настроение и нарушения сна.
Реабилитолог Петр Ковальчук о том, как справиться с болью
Что поможет снизить болевой синдром?
В Медицинском доме Odrex применяется комплексный подход. В качестве противоболевого лечения используется:
- Правильное позиционирование пациента после инсульта каждые 2 часа.
- Ортопедическая поддержка плеча:
- В положении сидя – подушкой.
- В положении стоя и при ходьбе использовать косыночные бандажи, плечевые ортезы, слинги.
- Физические упражнения для реабилитации после инсульта. Нагрузки должны усиливаться постепенно, а прогресс не должен тормозиться.
- Медикаментозное лечение (антидепрессанты, НПВС).
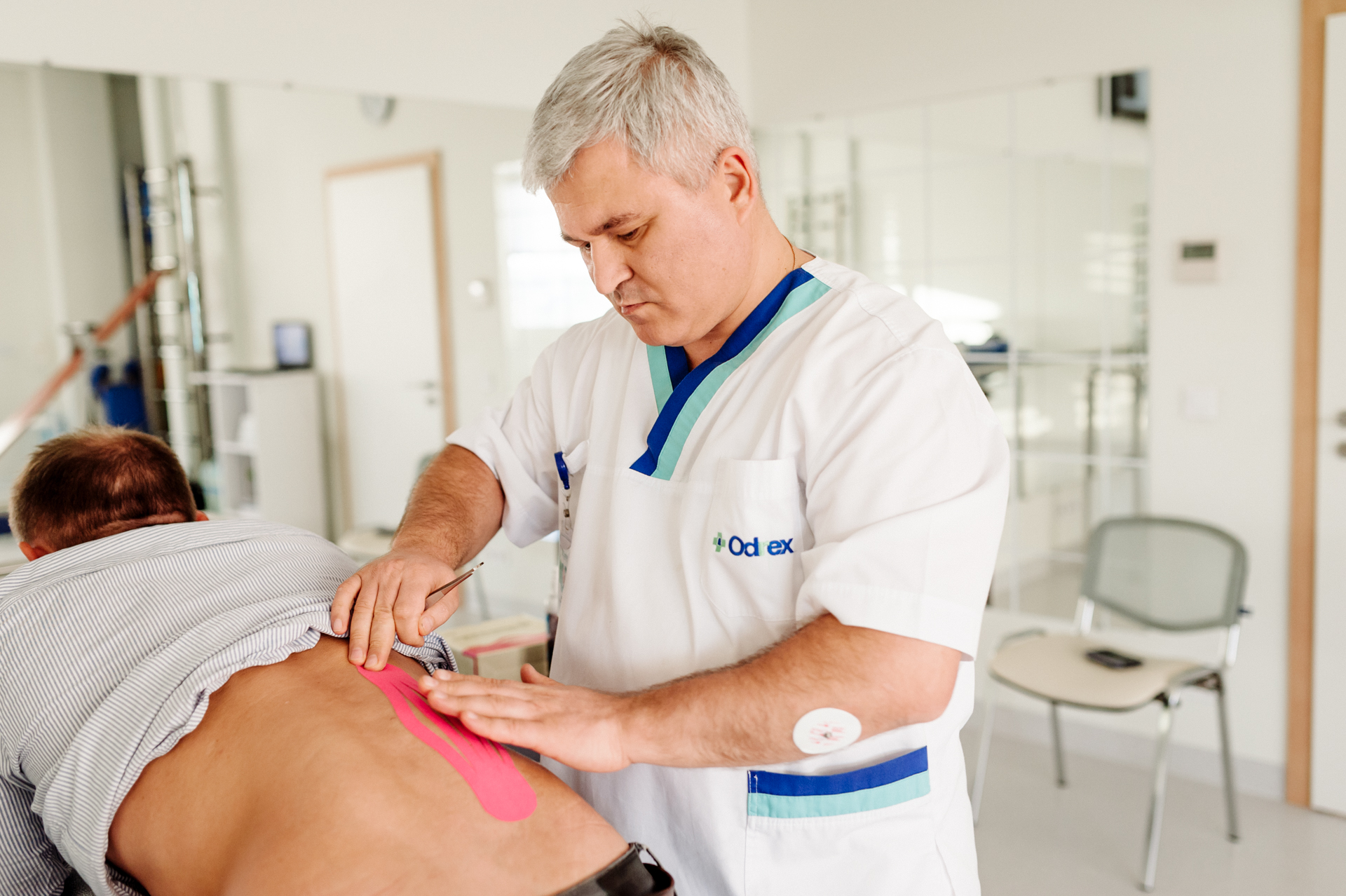
- Физиотерапевтическое лечение: физиотерапия системой Хивамат, ультразвуковая терапия, ЧЭНС-терапия, кинезиотейпирование, рефлексотерапия, массаж.

Команда реабилитологов: Петр Ковальчук, Юрий Железняк, Елена Чумаева, Руслан Волошин
Как избежать ошибок при уходе?
Не вполне верный уход может привести к травматизации. Среди ошибок:
- тянуть пациента за руку
- поднимать руку за кисть;
- помогать при ходьбе, удерживая за руку;
- подтягивать в кресле сзади.
- неправильные пассивные движения в плечевом суставе;
Как боль препятствует восстановлению?
Этот тягостный симптом не дает возможности использовать уже имеющиеся навыки и приобретать новые, снижает реакции равновесия, а это значит – больной может бояться двигаться. Человек становится зависимым от окружающих, что усугубляет такие общие стрессовые проявления, как плохое настроение и нарушенный сон.
Когда начинать терапию?
Лучшие результаты наблюдаются, если лечение проводится в самом начале развития болевого синдрома, когда только появляется небольшая припухлость в области сустава, а также нерезкая болезненность при активных и пассивных движениях и при надавливании.
Вместе с тем в неврологической практике часто наблюдаются так называемые «запущенные» случаи, когда на ранних этапах развития болевого синдрома в плече вышеуказанные методы не применялись. Это обуславливает необходимость дальнейших исследований по реабилитации больных с постинсультной болью в суставах.
Арт-терапевт, эрготерапевт Елена Чумаева о том, что поможет восстановлению

Что нужно делать, чтобы восстановить функцию плеча?
Тренировка навыков самообслуживания. Конечно, больному требуется помощь, но это не означает, что надо стремиться предупредить каждый его шаг. Излишняя опека мешает восстановлению движений. Старайтесь чаще привлекать больного к выполнению посильной домашней работы. Желательно, чтобы все это он делал по возможности больной рукой или с ее участием. Круг обязанностей расширяйте постепенно, при этом необходимо добиваться, чтобы то или иное посильное поручение больной выполнял сам.

Любимое дело и реабилитация?
Арт-терапия в виде рисования, лепки и других занятий широко применяетс при двигательных расстройствах. Сеансы реабилитации стабилизируют эмоциональное состояние, дают возможность вернуть координационные навыки, улучшают мелкую моторику.
Что нельзя и что нужно делать при реабилитации
Что НЕЛЬЗЯ делать
- Использовать методику «лечение положением» по С. И. Уварова-Якобсон 1941 года.
- Поднимать руку за дистальный отдел (кисть).
- Подтягивать пациента, сидящего в кресле, за подмышки.
- Использовать кистевой эспандер.

Что НУЖНО делать
- Рано активизировать больного.
- Помнить, что боль и спастичность легче предупредить, чем лечить.
- Всегда беречь плечо.
- Следить за постоянным использованием всех возможностей руки в повседневной жизни.
- Обучить ухаживающих правильному перемещению пациента.
- Ставить совместно с больным реабилитационные цели – вовлекать пациента в активную реабилитацию.
Записаться на прием к физиотерапевту, реабилитологу, эрготерапевту можно по телефону +38 (048) 730-00-30 либо через форму на сайте (вверху страницы).
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Хачаянц Н.Ю. 1 1 Ставропольский государственный медицинский университет В данном литературном обзоре представлены основные представления о истории вопроса диагностики центральной постинсультной боли, представлены основные направления исследования данного вопроса на современном этапе. Данный обзор представляет разные точки зрения как отечественных, так и за рубежных авторов по вопросам диагностики и лечения данного осложнения после перенесенного ОНМК. Рассмотрены нейрофизиологические аспекты данной проблемы и пути их дальнейшего развития. В конце данного обзора делается вывод, что на современном этапе следует признать, что несмотря на определенные достижения в области терапии центральной постинсультной боли, лечение таких больных остается сложной задачей. В этой связи исследования в данном направлении следует считать актуальными, и требуют дальнейшего понимания и изучения данной проблемы.  1017 KB ОНМК инсульт центральная постинсультная боль 1. Белянова Н.П., Симхес Ю.В., Карпов С.М., Долгова И.Н., Аубекова О.М. Влияние метеоусловий на частоту поступления в стационар больных с острым нарушением мозгового кровообращения. Международный научно-исследовательский журнал. – 2013. – № 10–5 (17). – С. 28–30. 2. Белянова Н.П., Карпов С.М. Посезонное поступление больных с онмк в зависимости от времени года. Международный журнал прикладных и фундаментальных исследований. – 2012. – № 1. – С. 18–19. 3. Виничук С.М., Прокопов М.М., Трепет Л.Н. Изолированный инфаркт таламуса: клинические синдромы, диагностика, лечение и исход. Украинский медицинский журнал. – 2012. – № 2 (88) III–IV; URL: www.umj.com.ua. 4. Гуляев С.А., Овчинникова А.А., Овчинников А.В. Комплексной лечение болей в клинике нервных болезней при синдроме Дежерина – Русси. Русский медицинский журнал. – 2013. – № 35. – С. 1793–1795. 5. Гусев Е.И., Бурд Г.С., Никифоров А.С. Неврологические симптомы, синдромы, симптомокомплексы и болезни. – М., 1999. – С. 323. 6. Диденко Н.Н., Денисюк В.В., Потапова И.Г., Карпов С.М. Актуальные вопросы распространенности ОНМК в Ставропольском крае. Успехи современного естествознания. – 2014. – № 6. – С. 121–122. 7. Данилов А.Б., Давыдов О.С. Возможности терапии центральной нейропатической боли. Справочник поликлинического врача. – 2009. – № 5. – С. 29–32. 8. Данилов А.Б., Давыдов О.С. Центральная нейропатическая боль: клинико-диагностические аспекты и возможности терапии на основе доказательств. Неврология. – 2009. – № 1. – С. 60. 9. Ковальчук В.В., Скоромец А.А. Массаж при восстановлении пациентов после инсульта. Паллиативная медицина и реабилитация. – 2009. – № 3. – С. 80. 10. Королев А.А., Суслова Г.А. Центральная постинсультная боль. Международный журнал прикладных и фундаментальных исследований. – 2011. – № 5. – С. 95–96. 11. Карлов В.А. Неврология. Руководство для врачей. – М., 2011. – С. 589. 12. Муравьев К.А., Карпова Е.Н., Карпов С.М. Организация и вопросы нарушения этапного поступления больных с острым нарушением мозгового кровообращения в г. Ставрополе. Медицинский вестник Северного Кавказа. – 2014. – Т. 9, № 4 (36). – С. 372–374. 13. Муравьева В.Н., Карпова Е.Н. Современные представления о факторах риска и профилактики ОНМК . Международный журнал экспериментального образования. – 2014. – № 3–2. – С. 59–64. 14. Михеев В.В., Мельничук П.В. Нервные болезни. – М., 1981. – С. 274. 15. Мищенко В.Н. Постинсультный болевой синдром. Новости медицины и фармации. Неврология (420), 2012 (Тематический номер). – С. 68. 16. Одинак М.М., Живолупов С.А., Самарцев И.Н. Болевые синдромы в неврологической практике. Журнал неврологии и психиатрии имени С.С. Корсакова. – 2009. – Т. 109, № 9. – С. 80. 17. Ревегук Е.А., Карпов С.М. Распространенность ОНМК среди лиц молодого возраста. Успехи современного естествознания. – 2012. – № 5. – С. 61–62. 18. Сидорова С.А. Постинсультный болевой синдром и возможности коррекции габапентином. Успехи современного естествознания. – 2006. – № 8. – С. 73. 19. Ситнова М.А., Кормачев М.В., Есин Р.Г. Центральная постинсультная боль. Практическая медицина. – 2012. – № 2 (57). – С. 36–38. 20. Сашина М.Б., Кадыков А.С., Черникова Л.А. Постинсультные болевые синдромы. Нервные болезни. – 2004. – № 3. – С. 25–27. 21. Яворская В.А., Бондарев О.Б., Ибрагимова Е.Л. с соавт. Ишемические таламические инфаркты. Международный медицинский журнал. – 2009. – № 1. – С. 12–15. 22. Boivie J. Central Pain. The Paths of Pain. Seattle:IASP Press, 2005, p. 299–312. 23. Dostrovsky J.O., Manduch M., Davis KD et al. Thalamic stimulation-evoked pain and temperature sites in pain and non-pain patients. Proceedings World Congress on Pain. Seattle:IASP Press. 2000, pp. 419–425. 24. Greenspan J.D., Ohara S., Sarlani E. et al. Allodynia in patients with post-stroke central pain (CPSP) studical by statistical quantitative sensory testing within individuals. Pain, 2004, № 109, pp. 357–366. 25. Hansson P. Post-stroke pain case study. Clinical characteristics, therapeutic options and long-term followup. Eur J Neurol, 2004, № 11 (Suppl 1), pp. 22–30. 26. Henry J., Yashpal K., Lalloo C. Central poststroke pain:a perspective. Central Neuropathic Pain:Focus on Poststroke Pain. Seattle:IASP Press, 2007, pp. 3–5. 27. Jones A.K., Watabe H., Cunnihgham V.J. et al. Cerebral decreases in opioid receptor binding in patients with central neuropathic pain measured by diprenorphine binding and PET. Eur J Pain, 2004, № 8, pp. 479–485. 28. Maruno N., Kaminaga T., Mikami M et al. Activation of supplementary motor area during imaginary movement of phantom toes. Neurorehabil Neural Repair, 2000, № 14, pp. 345–349. 29. Roux F.E., Ibarrola D., Lazorthes Y. et al. Chronic motor cortex stimulation for phantom limb pain:a functional magnetic resonance imaging study. Technical case report. Neurosyrgery, 2001, № 40, pp. 681–687. 30. Scadding J.W. Treatment of neuropathic pain:historical aspects. Pain Med, 2004, № 5 (Suppl 1), pp. 3–8. 31. Schott G.D. From thalamic syndrome to central poststroke pain. J Neurol Neurosurg Psychiatry, 1996, № 61, pp. 560–564. 32. Sprenger T., Berthele A., Platzer S. et al. What to learn from in vivo opioidergic brain imaging? Eur J Pain, 2005, № 9, pp. 117–121. 33. Thom T., Haase N., Rosamond W. et al. Heart disease and stroke statisties:a report from the American Heart Association. Statistics Committee and Stroke Statisties Subcommittee. Circulation, 2006, № 113, pp. 85–151. 34. Tasker R. Central pain, states. In:Loeser J.D., editor. Bonica s Management of Pain, 3rd edn. Philadelphia:Lippincott Williams and Wilkins, 2001, pp. 432–453.
1017 KB ОНМК инсульт центральная постинсультная боль 1. Белянова Н.П., Симхес Ю.В., Карпов С.М., Долгова И.Н., Аубекова О.М. Влияние метеоусловий на частоту поступления в стационар больных с острым нарушением мозгового кровообращения. Международный научно-исследовательский журнал. – 2013. – № 10–5 (17). – С. 28–30. 2. Белянова Н.П., Карпов С.М. Посезонное поступление больных с онмк в зависимости от времени года. Международный журнал прикладных и фундаментальных исследований. – 2012. – № 1. – С. 18–19. 3. Виничук С.М., Прокопов М.М., Трепет Л.Н. Изолированный инфаркт таламуса: клинические синдромы, диагностика, лечение и исход. Украинский медицинский журнал. – 2012. – № 2 (88) III–IV; URL: www.umj.com.ua. 4. Гуляев С.А., Овчинникова А.А., Овчинников А.В. Комплексной лечение болей в клинике нервных болезней при синдроме Дежерина – Русси. Русский медицинский журнал. – 2013. – № 35. – С. 1793–1795. 5. Гусев Е.И., Бурд Г.С., Никифоров А.С. Неврологические симптомы, синдромы, симптомокомплексы и болезни. – М., 1999. – С. 323. 6. Диденко Н.Н., Денисюк В.В., Потапова И.Г., Карпов С.М. Актуальные вопросы распространенности ОНМК в Ставропольском крае. Успехи современного естествознания. – 2014. – № 6. – С. 121–122. 7. Данилов А.Б., Давыдов О.С. Возможности терапии центральной нейропатической боли. Справочник поликлинического врача. – 2009. – № 5. – С. 29–32. 8. Данилов А.Б., Давыдов О.С. Центральная нейропатическая боль: клинико-диагностические аспекты и возможности терапии на основе доказательств. Неврология. – 2009. – № 1. – С. 60. 9. Ковальчук В.В., Скоромец А.А. Массаж при восстановлении пациентов после инсульта. Паллиативная медицина и реабилитация. – 2009. – № 3. – С. 80. 10. Королев А.А., Суслова Г.А. Центральная постинсультная боль. Международный журнал прикладных и фундаментальных исследований. – 2011. – № 5. – С. 95–96. 11. Карлов В.А. Неврология. Руководство для врачей. – М., 2011. – С. 589. 12. Муравьев К.А., Карпова Е.Н., Карпов С.М. Организация и вопросы нарушения этапного поступления больных с острым нарушением мозгового кровообращения в г. Ставрополе. Медицинский вестник Северного Кавказа. – 2014. – Т. 9, № 4 (36). – С. 372–374. 13. Муравьева В.Н., Карпова Е.Н. Современные представления о факторах риска и профилактики ОНМК . Международный журнал экспериментального образования. – 2014. – № 3–2. – С. 59–64. 14. Михеев В.В., Мельничук П.В. Нервные болезни. – М., 1981. – С. 274. 15. Мищенко В.Н. Постинсультный болевой синдром. Новости медицины и фармации. Неврология (420), 2012 (Тематический номер). – С. 68. 16. Одинак М.М., Живолупов С.А., Самарцев И.Н. Болевые синдромы в неврологической практике. Журнал неврологии и психиатрии имени С.С. Корсакова. – 2009. – Т. 109, № 9. – С. 80. 17. Ревегук Е.А., Карпов С.М. Распространенность ОНМК среди лиц молодого возраста. Успехи современного естествознания. – 2012. – № 5. – С. 61–62. 18. Сидорова С.А. Постинсультный болевой синдром и возможности коррекции габапентином. Успехи современного естествознания. – 2006. – № 8. – С. 73. 19. Ситнова М.А., Кормачев М.В., Есин Р.Г. Центральная постинсультная боль. Практическая медицина. – 2012. – № 2 (57). – С. 36–38. 20. Сашина М.Б., Кадыков А.С., Черникова Л.А. Постинсультные болевые синдромы. Нервные болезни. – 2004. – № 3. – С. 25–27. 21. Яворская В.А., Бондарев О.Б., Ибрагимова Е.Л. с соавт. Ишемические таламические инфаркты. Международный медицинский журнал. – 2009. – № 1. – С. 12–15. 22. Boivie J. Central Pain. The Paths of Pain. Seattle:IASP Press, 2005, p. 299–312. 23. Dostrovsky J.O., Manduch M., Davis KD et al. Thalamic stimulation-evoked pain and temperature sites in pain and non-pain patients. Proceedings World Congress on Pain. Seattle:IASP Press. 2000, pp. 419–425. 24. Greenspan J.D., Ohara S., Sarlani E. et al. Allodynia in patients with post-stroke central pain (CPSP) studical by statistical quantitative sensory testing within individuals. Pain, 2004, № 109, pp. 357–366. 25. Hansson P. Post-stroke pain case study. Clinical characteristics, therapeutic options and long-term followup. Eur J Neurol, 2004, № 11 (Suppl 1), pp. 22–30. 26. Henry J., Yashpal K., Lalloo C. Central poststroke pain:a perspective. Central Neuropathic Pain:Focus on Poststroke Pain. Seattle:IASP Press, 2007, pp. 3–5. 27. Jones A.K., Watabe H., Cunnihgham V.J. et al. Cerebral decreases in opioid receptor binding in patients with central neuropathic pain measured by diprenorphine binding and PET. Eur J Pain, 2004, № 8, pp. 479–485. 28. Maruno N., Kaminaga T., Mikami M et al. Activation of supplementary motor area during imaginary movement of phantom toes. Neurorehabil Neural Repair, 2000, № 14, pp. 345–349. 29. Roux F.E., Ibarrola D., Lazorthes Y. et al. Chronic motor cortex stimulation for phantom limb pain:a functional magnetic resonance imaging study. Technical case report. Neurosyrgery, 2001, № 40, pp. 681–687. 30. Scadding J.W. Treatment of neuropathic pain:historical aspects. Pain Med, 2004, № 5 (Suppl 1), pp. 3–8. 31. Schott G.D. From thalamic syndrome to central poststroke pain. J Neurol Neurosurg Psychiatry, 1996, № 61, pp. 560–564. 32. Sprenger T., Berthele A., Platzer S. et al. What to learn from in vivo opioidergic brain imaging? Eur J Pain, 2005, № 9, pp. 117–121. 33. Thom T., Haase N., Rosamond W. et al. Heart disease and stroke statisties:a report from the American Heart Association. Statistics Committee and Stroke Statisties Subcommittee. Circulation, 2006, № 113, pp. 85–151. 34. Tasker R. Central pain, states. In:Loeser J.D., editor. Bonica s Management of Pain, 3rd edn. Philadelphia:Lippincott Williams and Wilkins, 2001, pp. 432–453.
Сосудистые заболевания головного мозга продолжают оставаться одной из важнейших медицинских и социальных проблем современного общества . Инсульты являются одной из наиболее частых причин тяжелой и длительной инвалидизации в большинстве стран мира. В России уровень инвалидизации через год после перенесенного инсульта колеблется от 76 % до 85 %, в то время как в странах Западной Европы этот показатель составляет 25–30 %. В нашей стране среди пациентов, перенесших инсульт, к трудовой деятельности возвращаются не более 10–12 %, а 25–30 % остаются до конца жизни глубочайшими инвалидами. Таким образом, восстановительное лечение постинсультных больных, в том числе и центральной постинсультной боли, является одной из наиболее актуальных научно–практических задач современной неврологии .
Боль – самый частый симптом, встречающийся в неврологической практике. Несмотря на многовековую историю изучения боли до сих пор существуют разные мнения в понимании патогенеза болевых синдромов. Эволюция концепции боли начинается с античных времен, когда боль расценивали как «божью кару» или следствие нарушения внутренней «жизненной энергии». Во времена Гиппократа и Аристотеля сердце считалось центром чувствительности, а боль рассматривалась как форма восприятия окружающего мира. С развитием идей нервизма в медицине (1-я половина XVII в.) появилась концепция специфичности боли. Наиболее приемлемым является определение боли, предложенное Международной ассоциацией по изучению боли (IASP) в 1994 г. : «Боль – неприятное сенсорное и эмоциональное переживание, связанное с существующими или возможными повреждениями ткани или описываемое в терминах такого повреждения» .
Центральная постинсультная боль развивается в течение 1-го года после инсульта у 8 % пациентов. Поскольку распространенность инсульта велика – около 500 случаев на 100 тыс. населения, число лиц с постинсультной болью значительно. У 50 % пациентов боль возникает в течение 1-го месяца после инсульта, у 37 % – в период от 1 месяца до 2-х лет после инсульта, у 11 % – после 2-х лет от момента инсульта .
Центральный болевой синдром или таламический заднелатеральный синдром или синдром Дежерина – Русси описали в 1906 году французские врачи – невропатолог J. Dejerine (1849–1917) и патолог G. Roussy ( 1874–1948). Это следствие поражения латерального отдела таламуса, в том числе заднелатерального вентрального его ядра. На противоположной стороне при этом наблюдаются постоянные приступообразно усиливающиеся, жгучие боли, гиперпатии. Жгучая, нечетко локализуемая боль приступообразно усиливается при раздражении покровных тканей, эмоциональном напряжении. Она сочетается со снижением поверхностной и особенно глубокой чувствительности, сенситивной гемиатаксией, псевдостереогнозом, преходящим гемипарезом, при этом преимущественно страдает рука, возможны гиперкинезыв ней по типу хореоатетоза, характерен феномен, известный как таламическая рука. Иногда отмечается также обеднение спонтанных мимических реакций, тогда как произвольные мимические движения остаются сохранными. Обычна неустойчивость внимания, ориентации. Могут быть изменения речи – нарушения внятности, монотонность, литеральные парафазии, угасание звучности. Возможна гемианопсия .
Долгое время развитие центральной постинсультной боли связывалось с поражением только таламуса. До сих пор нет четкой позиции в отношении механизма развития центральной постинсультной боли. После внедрения методов нейровизуализации удалось установить, что:
1) центральная постинсультная боль развивается при поражении как таламуса, таки внеталамических структур;
2) болевой синдром при центральной постинсультной боли имеет клинические особенности в зависимости от локализации инсульта;
3) центральная постинсультная боль может рассматриваться как генетически детерминированная идиосинкразия, возникающая при повреждении сенсорных структур и связанная с дефицитом определенных тормозных процессов в ЦНС.
Инфаркты в латеральных отделах таламуса (бассейн ветвей a.thalamogeniculata) проявляются двигательными расстройствами (неловкость и атаксия), входящими в структуру таламического синдрома Дежерина – Русси и имеют клиническую особенность, которая связана с нарушением моделей движения в результате повреждения экстрапирамидных волокон, идущих:
1. От базальных ганглиев через ansa lenticularis;
2. От верхних ножек мозжечка и красного ядра, которые образуют синапсы в вентролатеральных ядрах таламуса;
3. От заднего ядра внутренней капсулы, которое примыкает к вентролатеральной части таламуса .
Для синдрома Дежерина – Русси характерны такие клинические проявления: умеренный преходящий гемипарез на противоположной очагу поражения стороне без признаков спастичности мышц, выраженная гемигипестезия, гемиатаксия, боль и парестезия после инсульта в дистальных отделах конечностей, часто распространяющиеся на всю половину тела – гемиалгия .
Хотя боль центрального происхождения обычно описывают как поверхностное жжение, разрывающую или колющую боль, вызываемую прикосновением или холодом, но описания, даваемые пациентами, весьма различны. Она обычно сочетается с каким-либо нарушением чувствительности и может начаться сразу же после инсульта или спустя недели или месяцы. К счастью, центральная боль после инсульта встречается нечасто, так как она очень плохо отражается на состоянии больного и ее трудно лечить. С этой целью применяли антидепрессанты, антиконвульсанты и антиаритмические препараты. Амитриптилин оказался более эффективен, чем плацебо. Объективные методы, такие как акупунктура и чрезкожная электростимуляция нервов можно попытаться применять в некоторых трудных случаях. При тяжелых болях может помочь стереотаксическая мезентеральная трактотомия, но она несет высокий риск инвалидизации и смертности .
Таламическая гиперпатия иногда проявляется в виде резких так называемых центральных или таламических болей, крайне мучительных, протекающих с ощущением жжения в дистальных отделах руки, половине лица, а иногда и в ноге. С наступлением сна они даже нарастают, окончательно лишая больного покоя. Боли эти плохо снимаются, лучше всего действует аминазин .
При инсульте, возникшем в области таламуса, обычно остро возникает контралатеральный гемипарез. После того, как он начинает подвергаться обратному развитию, у больных появляется боль, наиболее остро ощущаемая в лице и в руке паретичной стороны. Нередко боль концентрируется в глубине глаза. Боль описывается как жгучая и усиливающаяся при прикосновении, эмоциональных воздействиях. Объективно определяются признаки гиперпатии .
Международная ассоциация по изучению боли дает следующее определение хронической боли: это болевое ощущение, которое продолжается сверх нормального периода заживления. Одним из синдромов хронической боли, с которым встречается врач-невролог в своей повседневной работе, является синдром центральной постинсультной (таламической) боли. Это боли нестерпимого характера с ощущениями ломоты, жжения, выкручивания. Также у пациентов можно наблюдать приступы насильственного смеха или плача и контралатеральные вегетативно-трофические нарушения с формированием в последующем специфической установки рук с хореатетоидными движениями в пальцах. По современным представлениям, синдром Дежерина – Русси развивается вследствие поражения ядер таламуса. Такое многообразие клинических проявлений синдрома Дежерина – Русси часто вызывает сложности, как на этапе его первичной диагностики, так и лечения. В настоящее время для лечения используют различные методы, в том числе и хирургические, но главной остается фармакотерапия с применением нестероидных противовоспалительных препаратов, антиконвульсантов, антидепрессантов, анестетиков и др. .
У больных ишемическим инсультом постинсультный болевой синдром коррелирует со степенью выраженности гемипареза, гемиатаксии, сенсорных нарушений по геми – или монотипу, с преобладанием в кисти и ноге по типу парадоксального жжения. Интенсивность постинсультного болевого синдрома варьирует от нестерпимой, мучительной боли, полностью инвалидизирующей пациента, до незначительного чувства дискомфорта. Развитие постинсультного болевого синдрома возможно и при отсутствии двигательных нарушений – «чисто сенсорный инсульт» .
В патофизиологии центральной постинсультной боли играют важную роль:
Гипервозбудимость и активность в спиноталамическом тракте;
Очаг в латеральном таламусе, который прерывает подавляющие пути и вызывает растормаживание медиального таламуса (теория растормаживания);
Изменения в таламусе, поскольку он играет роль генератора боли и в нем происходит потеря тормозящих ГАМК – содержащих нейронов и активизация микроглии.
Диагноз ЦПБ основывается на данных анамнеза болезни, результатах клинико-неврологического обследования. Учитываются сведения о начале болезни, ее характере, наличии дизестезии или аллодинии, чувствительных нарушений. Используется визуально-аналоговая шкала для оценки боли, а также данные нейровизуализации (КТ или МРТ головного мозга) .
При постинсультном болевом синдроме, кроме непосредственно жгучей боли в конечностях, часто встречаются нарушения высших функций и психические нарушения (эмоциональные аффекты, дефицит внимания, нарушения поведения, памяти и сознания, ориентации, сна, иногда галлюцинации), обусловленные тесной функциональной связью таламуса с лимбикоретикулярным комплексом и лобной корой.
Инструментальные методы диагностики являются вспомогательными и их нельзя рассматривать как методы диагностики и оценки нейропатической боли. Для оценки интенсивности боли используются визуальная аналоговая шкала, валидизированные в России опросники DN4 и painDETECT.
Кроме количественной оценки, неврологическое обследование должно включать картирование двигательных, сенсорных и вегетативных феноменов с целью идентификации всех признаков неврологической дисфункции. Для лечения постинсультного болевого синдрома Европейская федерация неврологических сообществ рекомендует прегабалин как препарат первой линии, трамадол как препарат второй линии. Доказана неэффективность или противоречивые результаты для карбамазепина, габапентина, ламотриджина, вальпроатов. При неэффективности медикаментозной терапии показаны хируругические методы лечения .
Хотя механизмы формирования центральной постинсультной боли остаются до конца неясными, большинство исследователей придерживаются мнения, что в основе центральной постинсультной боли лежат два возможных механизма:
1. Повышенная возбудимость нейронов в поврежденных структурах латеральной части ноцицептивной системы;
2. Неадекватное функционирование ингибирующих антиноцицептивных сенсорных путей.
Что касается лечения центральной постинсультной боли, то еще Дежерин и Русси указывали, что возникшая после инсульта непереносимая боль не уменьшалась при назначении анальгетиков. Это является одним из критериев постановки диагноза центральной постинсультной боли, так как центральная боль, в отличие от «ноцицептивной», не связана с активацией периферических ноцицепторов. Определенный обезболивающий эффект при центральной постинсультной боли наблюдается при использовании транскраниальной электростимуляции, активирующей эндорфинные структуры антиноцицептивной системы головного мозга .
На основании практического врачебного опыта установлено, что в лечении центральной постинсультной боли эффективны антидепрессанты в сочетании с антиконвульсантами .
При лечении центральной постинсультной боли показана эффективность амитриптилина, которая была выше при его назначении сразу после появления боли. Селективные ингибиторы обратного захвата серотонина малоэффективны. Попытки лечения центральной постинсультной боли с помощью нестероидных противовоспалительных препаратов были неудачными. Данные об использовании опиоидных анальгетиков неубедительны. Перспективы лечения связывают с применением антиконвульсантов.
Следует признать, что, несмотря на определенные достижения в области терапии центральной постинсультной боли, лечение таких больных остается сложной задачей. В этой связи исследования в данном направлении следует считать актуальными, и требуют дальнейшего понимания и изучения данной проблемы.
Библиографическая ссылка
Хачаянц Н.Ю. ЦЕНТРАЛЬНАЯ ПОСТИНСУЛЬТНАЯ БОЛЬ (ЛИТЕРАТУРНЫЙ ОБЗОР) // Международный журнал прикладных и фундаментальных исследований. – 2015. – № 5-1. – С. 74-77;
URL: https://applied-research.ru/ru/article/view?id=6766 (дата обращения: 29.10.2020). Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания» (Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления) «Современные проблемы науки и образования» список ВАК ИФ РИНЦ = 0.791 «Фундаментальные исследования» список ВАК ИФ РИНЦ = 1.074 «Современные наукоемкие технологии» список ВАК ИФ РИНЦ = 0.909 «Успехи современного естествознания» список ВАК ИФ РИНЦ = 0.736 «Международный журнал прикладных и фундаментальных исследований» ИФ РИНЦ = 0.570 «Международный журнал экспериментального образования» ИФ РИНЦ = 0.431 «Научное Обозрение. Биологические Науки» ИФ РИНЦ = 0.303 «Научное Обозрение. Медицинские Науки» ИФ РИНЦ = 0.380 «Научное Обозрение. Экономические Науки» ИФ РИНЦ = 0.600 «Научное Обозрение. Педагогические Науки» ИФ РИНЦ = 0.308 «European journal of natural history» ИФ РИНЦ = 1.369 Издание научной и учебно-методической литературы ISBN РИНЦ DOI
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания» (Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления) «Современные проблемы науки и образования» список ВАК ИФ РИНЦ = 0.791 «Фундаментальные исследования» список ВАК ИФ РИНЦ = 1.074 «Современные наукоемкие технологии» список ВАК ИФ РИНЦ = 0.909 «Успехи современного естествознания» список ВАК ИФ РИНЦ = 0.736 «Международный журнал прикладных и фундаментальных исследований» ИФ РИНЦ = 0.570 «Международный журнал экспериментального образования» ИФ РИНЦ = 0.431 «Научное Обозрение. Биологические Науки» ИФ РИНЦ = 0.303 «Научное Обозрение. Медицинские Науки» ИФ РИНЦ = 0.380 «Научное Обозрение. Экономические Науки» ИФ РИНЦ = 0.600 «Научное Обозрение. Педагогические Науки» ИФ РИНЦ = 0.308 «European journal of natural history» ИФ РИНЦ = 1.369 Издание научной и учебно-методической литературы ISBN РИНЦ DOI
После девяти дней лечения в стационаре 35-летнего тюменца, пережившего ишемический инсульт, перевели в реабилитационный центр. Сейчас у него важный и ответственный этап – восстановление и возвращение к прежней жизни. По словам врачей, прогноз благоприятный, однако многое теперь зависит от самого человека, его готовности работать над собой. Об этом «Вслух.ру» рассказали в департаменте здравоохранения Тюменской области.
В первый раз ощущение онемения в левой руке и ноге у него возникло 3 июня ранним утром, но он не придал этому значения и снова заснул. Проснувшись, почувствовал себя гораздо лучше, поэтому обращаться за медпомощью не стал. К вечеру симптомы появились опять и уже не исчезли. С вызовом скорой помощи мужчина все равно тянул, убеждая себя, что все пройдет само.
Срочный вызов на «103» поступил только в 2.55 ночи, бригада сразу направилась к пациенту, которого парализовало. «Утром у пациента произошла транзиторная ишемическая атака – временное прекращение циркуляции крови в одном из участков головного мозга по причине спазма или тромбоза, – рассказывает врач скорой помощи Алексей Юшков. – Это был первый звоночек, после развился полноценный инсульт. На момент осмотра мужчина не смог удержать левую руку на весу, сжать с достаточной силой мою руку. Оказав медицинскую помощь по стандарту, мы в экстренном порядке госпитализировали пациента в областную клиническую больницу №2».
Специалисты скорой помощи напоминают, что заподозрить инсульт можно по следующим признакам:
• Ослабла или не двигается одна рука (нога)
• Уголок рта опущен и лицо перекошено
• Нарушение речи и ее понимания
• Частичная или полная потеря зрения
• Внезапная сильная головная боль
Необходимо сразу вызывать скорую помощь. До прибытия бригады медиков не рекомендуется давать никаких лекарств. Больному нужно обеспечить состояние покоя: уложить на кровать, расстегнуть сдавливающую одежду.
В течение 4,5 часов от появления первых симптомов причину инсульта врачи регионального сосудистого центра могут устранить без последствий для жизни и здоровья человека.
Специалисты сосудистого центра рекомендуют фиксировать точное время развития симптомов инсульта, поскольку это напрямую сказывается на эффективности мероприятий по растворению тромба: чем раньше – тем лучше. При транспортировке в больницу желательно, чтобы с пациентом был сопровождающий – человек, который владеет информацией о здоровье и жизни больного и может сообщить доктору, какие лекарственные препараты принимал пациент в течение последних нескольких дней перед развитием инсульта.