Иммунодефицит вторичный
Щербина Анна Юрьевна, заместитель директора Института гематологии, иммунологии и клеточных технологий, д.м.н., заведующая отделением иммунологии НМИЦ ДГОИ им. Дмитрия Рогачева, врач-педиатр, иммунолог-аллерголог, профессор кафедры гематологии факультета усовершенствования врачей Российского национального исследовательского медицинского университета им. Н.И. Пирогова.
Образование: 2-й Московский ордена Ленина государственный медицинский институт имени Н.И. Пирогова (сейчас — Российский национальный исследовательский медицинский университет им. Н.И. Пирогова), ординатура по педиатрии НИИ детской гематологии.
Регалии и звания: доктор медицинских наук, профессор, автор более 100 публикаций, член Российской ассоциации аллергологов и клинических иммунологов, Европейского общества иммунодефицитов.
Про виды иммунодефицитов
Иммунодефицит — это состояние, сопровождающееся значительными и долговременными изменениями в иммунной системе и серьезными симптомами. Есть иммунодефициты вторичные, а есть первичные (ПИД). Первичные обусловлены генетически. Как правило, симптомы возникают в раннем возрасте, однако иногда могут возникнуть и у взрослых. Но в любом случае проявления будут очень тяжелыми. С первичными иммунодефицитами встречаются крайне редко. Подтвердить многие такие заболевания можно, обнаружив дефект гена. Но пока, правда, найдены мутации не при всех ПИД, поиск продолжается.
Вторичные иммунодефициты — это те, которые возникли в течение жизни под воздействием каких-то факторов, приведших к стойким изменениям иммунитета, возможно пожизненным, но не всегда. Вторичный иммунодефицит может пройти без лечения: если, например, ушел воздействующий фактор. ПИД же обязательно нужно лечить.
Про СПИД и другие вторичные иммунодефициты
По международной классификации вторичными иммунодефицитами считаются серьезные изменения в иммунитете, возникшие под воздействием химиотерапии, облучения, после трансплантации органов и тканей (что сопровождается иммуносупрессивной терапией), при потере белка (основного инструмента, которым оперирует иммунная система). Последний вариант может возникнуть, когда у человека какое-то почечное заболевание и белок уходит с мочой. Или когда у пациента тяжелое заболевание кишечника, нередко врожденное, при котором возникает длительный понос, что также вызывает потерю белка.
СПИД тоже относится к вторичным иммунодефицитам, но он стоит несколько особняком. И во всем мире, и в России обычно этим синдромом занимаются отдельные люди. Но, естественно, у нас с ними есть какое-то взаимодействие, потому что к нам, например, может прийти человек с симптомами как при первичном иммунодефиците, но окажется, что у него СПИД. Таких детей я видела немало.
Про ложные диагнозы
В России понятие «вторичный иммунодефицит» распространилось до неприличия широко: нередко мы слышим, что у каждого человека можно выявить вторичный иммунодефицит. И это, по сути, только потому, что он живет в мире, где много вирусов, бактерий и грибков. Я не сторонник такой точки зрения. Если у человека насморк, это не значит, что у него тяжелая болезнь полости носа. Просто на слизистую попал вирус, его нужно удалить — вот и потекли сопли. Вирус уйдет — сопли прекратятся. Точно так же большинство изменений в иммунитете носят приспособительный характер — это не значит, что иммунная система не в порядке.
Есть критерии, по которым можно заподозрить наличие иммунодефицита. Основное его проявление — наличие инфекций, часто и тяжело протекающих. Нормально, если взрослый человек четыре–шесть раз в год болеет легкими инфекционными заболеваниями, от которых быстро вылечивается, хотя у него и может иногда быть бронхит или пневмония, требующие применения антибиотиков. Но если он использует антибиотики, а выздороветь никак не получается, это уже подозрительно.
Про настоящие причины инфекционных заболеваний
Иммунодефициты редко проявляются частыми простудами. Обычно это чувствительность к более серьезным инфекциям. Есть целый спектр состояний, которые могут мимикрировать под иммунодефициты. Например, если у человека два раза в месяц обычный насморк и болит горло, чаще всего причина в рефлюксе — забросе кислоты из желудка, которая смывает защитный слой слизистой. У взрослых это иногда превращается в хронический тонзиллит: инфекция уже поселилась в миндалинах, ее сложно оттуда «выгнать», и она проявляется при любом минимальном охлаждении, стрессе. По большому счету никакого отношения к иммунитету это не имеет. Да, в каком-то смысле местный иммунитет нарушен, но всегда принципиально понимать причину, чтобы ее можно было устранить. Если человеку просто дать какой-нибудь иммуномодулятор, то мы усилим на два дня местный иммунитет, но скоро все вернется в прежнее русло. Такие лжедиагнозы создают много проблем разного рода: настоящая причина ведь не ищется.
Если у человека хроническая инфекция, от которой он не может избавиться никакими антибиотиками, то причину нужно устанавливать сугубо индивидуально. Нередко хроническая инфекция возникает из-за какого-то врожденного порока, дефекта строения, который мешает нормально функционировать органу. Причиной может быть нарушение pH-среды, кровоснабжения, как при диабете, и т.п. Иммунодефициты довольно редко служат причиной хронических инфекций одного органа.
Про «слабый иммунитет»
Нет такого понятия «просто слабый иммунитет». Если мы действительно считаем, что он слабый, то это начало пути: нужно посмотреть на лабораторные исследования. В каких-то случаях там выявляются значимые изменения, и тогда мы стараемся поставить конкретный диагноз и в соответствии с ним пытаемся помочь больному. Если обнаруживается, что все анализы абсолютно нормальные, но человек, по нашим понятиям, болеет чаще и тяжелее, чем ему положено, тогда мы просто до последнего ищем причину нарушения иммунитета какими-то более сложными методами. Кроме того, постоянно обнаруживаются новые поломки в генах. Однако, как уже говорилось, нередко причиной инфекций являются совсем не иммунологические факторы. И в таких случаях дойти до первопричины необязательно должен иммунолог — это может сделать любой врач со здравым смыслом. Заподозрить иммунодефицит тоже в состоянии каждый доктор. Но, конечно, чтобы поставить точный диагноз, если речь идет об этом редком заболевании, нужен соответствующий опыт.
Про иммуномодуляторы
Иммуномодуляторы я практически не назначаю, хотя многие это делают. Вероятно, когда-нибудь я поменяю свое мнение, но пока меня никто не убедил, что иммуномодуляторы кому-то помогают. Я подозреваю, что среди этих препаратов есть такие, которые несут реальную пользу. Но у нас существуют определенные российские особенности: например, очень плохо проводятся клинические испытания препаратов, в том числе и иммуномодуляторов. К любому зарубежному препарату довольно жесткие требования в этом смысле. У нас какие-то исследования могут пройти формально — то, что там участвовало пятнадцать алкоголиков и три ребенка, никого не волнует.
Когда на большинстве иммуномодуляторов пишут, что у них нет побочных эффектов, я в это верю с трудом: либо мы не достигаем терапевтической концентрации (тогда зачем мы вообще применяем такой препарат?), либо эти проявления не очень хорошо искали. К тому же наша иммунная система — тонко сбалансированный механизм. Большинство веществ «стимулируют» сразу несколько его составляющих. И ведь можно простимулировать и то, что потом не лучшим образом даст о себе знать. Например, была в организме одна плохая клетка (условно) — иммунитет с ней успешно боролся. А если их станет сто пятьдесят? Сложно представить такой высокоселективный иммуномодулятор, который не затрагивает другие винтики нашей иммунной системы.
Про пользу инфекционных заболеваний
Если ко мне придет пациент и скажет, что ему назначил другой доктор иммуномодулятор, я не буду ничего отменять, а просто выскажу свое мнение об этой проблеме. Продолжать ли прием иммуномодулятора — личное дело пациента. Просто чем старше я становлюсь, тем меньше во мне категоричности. Иммуномодуляторы, которые основаны на использовании белков стенок бактерий и являются зарубежными, то есть прошли серьезные клинические исследования, имеют небольшую эффективность, но она есть. В редких случаях я назначаю какие-то препараты из этой группы. Такое бывает, когда пациент, даже выслушав все доводы, очень хочет чем-то полечиться. Но я предупреждаю — не ожидайте чуда, это не лекарство от всех болезней: может быть, вместо пяти раз заболеете четыре. Здоровый образ жизни, мытье рук, хорошее питание — это все уменьшает заболеваемость различными инфекциями, но люди не могут ими не болеть совсем. Чтобы так было, у нас должен иметься специфический иммунитет ко всем инфекциям. Он появляется у человека, когда тот хоть раз встречался с этой инфекцией.
Препараты вроде эхинацеи усиливают лишь местный иммунитет. Они могут чуть укоротить период знакомства с инфекцией, ускорить выздоровление. Вакцины покрывают лишь малое количество инфекций. Поэтому дети должны болеть. Более того, у детей, которые ограничены в контактах с потенциальными патогенами (единственный ребенок — к нему никого не подпускают, все стерильно), чаще всего развиваются аллергические заболевания, потому что здесь есть условные весы. Когда мы рождаемся, у нас так устроен иммунитет, что мы больше предрасположены к аллергии. Когда мы сталкиваемся с инфекциями, эти весы выравниваются. Если дети не болеют, у них гораздо дольше, а может быть и навсегда, остается предрасположенность к аллергии.
Про «заблудившийся» иммунитет
Аутоиммунные заболевания возникают, когда иммунитет, грубо говоря, заблудился. В нормальном состоянии он должен распознавать свои и чужие клетки. Поэтому так сложно осуществить трансплантацию сердца, почки или любого другого органа: организм тут же понимает, что это не его, и пытается от такого объекта избавиться. Но изначально эта система была придумана природой в основном для борьбы с инфекциями. При аутоиммунных заболеваниях механизм распознавания нарушается, организм воспринимает свое как чужое и атакует. Борьба может начаться с разными клетками или с клетками какого-то одного вида.
Мы занимаемся аутоиммунными заболеваниями, но по большому счету не очень много. Исторически так сложилось, что эти патологии чаще относят к кардиологии, ревматологии и гематологии. Однако и у наших больных с иммунодефицитами встречаются аутоиммунные заболевания — и, к слову, намного чаще, чем у обычных людей.
Про невежество
В коммуникации с пациентами и их родными у нас есть одна существенная проблема, которую никак не могут понять мои зарубежные коллеги. Дело в том, что многие пациенты с серьезными диагнозами нас не слушают. Проблема не в недоверии к конкретным иммунологам: мы предлагаем обследоваться в любом другом месте, в том числе и за границей, чтобы подтвердить диагноз; мы говорим: «Сделайте что-нибудь, иначе ребенок умрет». — «Нет, у нас все хорошо».
Один мальчик, например, не лечится, потому что родители сказали: «Мы раньше жили неправильно, поэтому он заболел. А сейчас будем жить правильно, и он выздоровеет». Даже не знаю, что они имели в виду. Такое случается и тогда, когда родители видят, что ребенок тяжело болеет, но чаще, конечно, тогда, когда болезнь только дебютировала и вся серьезность диагноза неочевидна. То есть для лечения ситуация, в которой пациент приходит рано, хороша, но имеет место такой нюанс — родителям сложно поверить, что болезнь есть.
Дело даже не в том, что они думают, будто мы хотим на них нажиться или поэкспериментировать, — им тяжело перевернуть свою жизнь с ног на голову. Да и слово «иммунодефицит» довольно затасканное. Я говорю, например: «У вашего ребенка иммунодефицит». — «Ага. А болеет-то он чем?» Иммунодефицит ведь «у всех». А на самом деле это очень тяжелая болезнь.
Про будущее иммунологии
Иммунология — довольно сложная область, и наши пациенты не так часто выздоравливают. Поэтому иммунологов не очень много: всем ведь хочется видеть результат своего труда, и сложно жить с мыслью, что большинство твоих больных уже умерло. Конечно, сейчас ситуация лучше, чем раньше: появились новые разработки, методы лечения. Я выбрала эту область, потому что она сложная, по большому счету мало кем изучается и оттого интересная.
Иммунология — не только клиническая наука, но и теория, которая постоянно меняется. Через 20 лет, возможно, мы будем смеяться над теми знаниями, которые имеем теперь. Не исключено, что тогда понимание всей этой проблемы будет другим. Например, в последнее время мы стали выявлять случаи, когда иммунограмма — анализ, показывающий состояние иммунной системы, — нормальная, но с помощью разных хитрых методов выясняется, что у человека иммунодефицит.
Стали обнаруживаться такие дефекты, при которых повышена чувствительность только к определенным группам микробов, а не, как обычно бывает при иммунодефицитах, ко всему сразу: микробам, грибковым инфекциям, вирусам. Недавно, например, выяснилось, что герпетический энцефалит (поражение головного мозга вирусом герпеса) — это тоже иммунодефицит, конкретный маленький дефект, который вызывает подобное состояние. Остальные инфекции такие больные переносят нормально.
Еще обнаружилась группа иммунодефицитов, которые проявляются повышенной чувствительностью к туберкулезу, микобактериям разного рода и небольшому количеству других инфекций, например сальмонеллам. Практически всем людям делают прививки БЦЖ, а это не что иное, как микобактерия. Она ослаблена, но это так с точки зрения обычного иммунитета. При той патологии, о которой мы говорим, микобактерия может вызывать соответствующие заболевания.
Относительно недавно к нам обратилась девочка, у которой основными проблемами были увеличенные шейные лимфоузлы, постоянная температура и периодически появляющиеся сыпи. Девочка также перенесла сальмонеллез, но, насколько я понимаю, после лечения ей не сделали два необходимых посева, которые должны были дать отрицательный результат. В целом картина складывалась довольно странная: сложно предположить, что у человека сразу несколько заболеваний, поэтому в таких случаях всегда хочется найти одну, общую причину проблем.
В процессе обследования выяснилось, что у девочки сальмонеллы высеваются отовсюду: из кишечника, слизистых носа, крови. У пациентки была активная воспалительная реакция, организм пытался избавиться от всех этих микробов. Оттого и увеличенные лимфоузлы, температура, сыпь. При этом стандартные иммунологические тесты не помогли с диагнозом. С помощью зарубежных коллег нам удалось подтвердить недавно описанный и очень редкий генетический дефект, который вызывает повышенную чувствительность к сальмонеллам, а также микобактериям. С помощью более интенсивных и длительных курсов антибиотиков нам удалось взять ситуацию под контроль.
Про диагностику
Со знаниями в области иммунологии у рядовых врачей все очень плохо. Это, конечно, сложная наука, но ее можно упростить. Однако, к сожалению, есть не так много вузов, в которых иммунологию преподают в хорошем объеме. А нужно всего-то, чтобы врачи знали, что могут просто, как стрелочники, направлять таких и таких больных к нам.
Оборотной стороной медали отсутствия знаний в иммунологии становится то, что довольно часто к нам направляют пациентов без иммунодефицитов. Но пусть уж нам лучше пришлют 10 тысяч детей без этого заболевания, чем мы пропустим одного больного с ПИД. Теоретически в России около 15 тысяч таких пациентов, а найдена всего, может быть, тысяча. И необходимо обнаружить остальных, пока они не умерли.
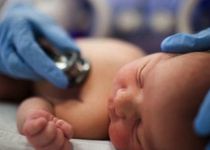
Представьте, что Вы не можете обнять и поцеловать Вашего ребенка, не помыв рук в течение трех минут и не надев специальный костюм. Представьте, что он впервые увидел мир через окно больничной палаты. Представьте, что Ваш ребенок по полгода живет не дома, а в больнице…
Первичный иммунодефицит – страшный диагноз, означающий, что ребенок родился без естественной защиты. Он совершенно не может сопротивляться инфекциям, и то, что для нас с вами является окружающим миром, для него – источник ежеминутной опасности.
Узнать больше про ПИД на портале — PROPID.ru
Первичный иммунодефицит представляет собой врожденные нарушения иммунной системы, которые развиваются вследствие генетических нарушений. Заболевание приводит к развитию тяжелых хронических инфекций и воспалительному поражению органов и тканей. Без лечения дети с первичным иммунодефицитом погибают от различных инфекционных осложнений.
На сегодняшний день открыто более 170 разновидностей подобных нарушений, которые встречаются примерно у одного пациента на 10 тыс. населения, но их реальная распространенность может достигать отношения 1:500.
По оценкам ведущих российских иммунологов, 90% больных Первичным иммуно-дефицитом в России умирают недиагностированными. В Национальном регистре, созданном в 2000 году на базе РДКБ, чуть более 700 пациентов, в регистре Института иммунологии еще столько же, хотя, по оценке Зав. отделением клинической иммунологии Кондратенко И.В, ожидаемое на сегодняшний день реальное количество пациентов в России может составить15000 человек. Несмотря на улучшение условий диагностики в регионах в последние годы, нередко детям ставят неправильные диагнозы и многие из них, особенно младенцы с тяжелой формой иммунодефицитных состояний, погибают в возрасте 2-4 месяцев.
Первичные признаки врожденного иммунодефицита могут быть не обнаружены, потому что у него нет уникальных черт. Он может проявляться как «обычная повторяющаяся инфекция», например носа, ушей или легких. Могут возникать желудочно-кишечные проблемы или воспаление суставов. Родители и врачи часто не осознают, что эти проблемы созданы генетическими дефектами иммунной системы. Инфекции переходят в хроническую форму, создают осложнения, пациент «не реагирует» на обычный курс антибиотиков. Тяжелые формы первичного иммунодефицита обычно проявляются сразу после рождения ребенка или спустя некоторое время после него.
Если врач заподозрил первичный иммунодефицит, то для точного установления типа патологии проводят ряд сложных иммунологических и генетических анализов – это помогает определить место нарушения иммунной защиты (клеточное или гуморальное звено), а также определить тип мутации, которая вызвала заболевание.
Важно понимать, что первичный иммунодефицит — это не СПИД (синдром приобретенного иммунодефицита). Хотя и тот и другой вид иммунодефицита затрагивают иммунную систему, первичный иммунодефицит является генетическим заболеванием, как бы «встроенным» в тело человека его генами. Это похоже на цвет ваших глаз: вы не можете его изменить. Приобретенный иммунодефицит (СПИД) является инфекционным заболеванием и вызывается вирусом.
Лечение первичных иммунодефицитов — сложная задача. Для назначения комплексного лечения обязательно установление точного диагноза с определением нарушенного звена иммунной защиты. В крупных городских больницах пациентов исследуют по рекомендованным клиническим критериям, проводят иммунологический скрининг с последующим уточнением диагноза в отделении клинической иммунологии Российской Детской Клинической больницы Росздрава.
При недостатке иммуноглобулинов проводят пожизненную заместительную терапию сыворотками, содержащими антитела или обычной донорской плазмой. При возникновении инфекционных осложнений назначают лечение антибиотиками, противовирусными или противогрибковыми препаратами.
Полная иммунологическая реконструкция у детей с тяжелой формой первичного иммунодефицита происходит только при трансплантации костного мозга. Это означает, что при успешной операции у ребенка образуется собственная иммунная система.
Содержание
Пренатальная диагностика и генетическое консультирование.
На сегодняшний день установлено, что многие иммунодефициты являются наследственными заболеваниями: известен тип наследования, выявлена локализация дефектного гена, определен продукт этого гена. Cтановится ясно, что первичный иммунодефицит – не столь редкое состояние, как принято было считать. Родителям и родственникам детей, больных ПИД необходимо знать, что в настоящее время стало возможным выявление носительства дефектного гена и генетическое консультирование семей, планирующих рождение детей с риском возникновения ПИД. Например, выявление одного из самых страшных диагнозов ПИД Тяжелой Комбинированной Иммунной Недостаточности (диагноза, являющегося 100 % летальным без проведения трансплантации костного мозга) возможно до рождения ребенка, если в семье уже есть больной ребенок, а также, если выявлен молекулярный дефект. Если у ранее рожденного больного ребенка проведен анализ мутации можно выполнить диагностическое исследование нерожденного ребенка ( эмбриона или плода с околоплодными тканями). Это можно сделать путем молекулярного анализа ресничек хориона или околоплодной жидкости, содержащей клетки плода и полученной из полости матки путем амниоцентеза.
В России проведение пренатальной диагностики и генетическое консультирование возможно в следующих медицинских диагностических центрах:
— Медико-генетический научный центр Российской академии медицинских наук (МГНЦ РАМН) http://www.med-gen.ru/
Адрес : 115478, Москва, ул. Москворечье, д. 1, Медико-генетический научный центр РАМН, второй этаж ; проезд: метро «Каширская»
Телефоны регистратуры: (495) 324-87-72, 324-18-65, 324-31-57
— «Центр Молекулярной Генетики» Полякова ; http://www.dnalab.ru/
Телефоны регистратуры: (495) 221-90-84, (495) 324-05-01, (495) 324-81-10, (495) 324-98-46
Часто задаваемые вопросы по первичному иммунодефициту
Первичный иммунодефицит – это СПИД?
Нет, первичные иммунодефициты являются наследственными заболевания и не относятся к инфекционным заболеваниям, т.к. дети страдающие первичным иммунодефицитом не опасны для окружающих, скорее окружающие представляют угрозу для детей страдающих первичными иммунодефицита.
Можно ли вылечить первичный иммунодефицит?
На сегодняшний день существует возможность излечения от первичного иммунодефицита, с помощью трансплантации костного мозга. В настоящее время в мире в каждым днем увеличивается количество форм первичных иммунодефицитов, которые можно вылечить с помощью ТКМ. Если еще несколько лет назад считалось что достаточно назначить антибактериальную и заместительную терапию иммуноглобулином, но на сегодняшний день во всем мире стараются как можно раньше провести трансплантацию костного мозга, чтобы избежать различных осложнений.
А не страшно ли то, что больные первичными иммунодефицитами всю жизнь получают антибиотики и другие противомикробные препараты, если считается что антибиотики подавляют иммунитет?
При первичных иммунодефицитах антибактериальная и другая противомикробная терапия назначается для помощи организму т.к. в первую очередь страдает противоинфекционная защита. В большинстве случаев, врачи, занимающими лечением пациентов, страдающих первичными иммунодефицитами, не видят осложнений от антибактериальной терапии, о которых так широко говориться в различных средствах массовой информации.
Если в семье есть дети, страдающие первичным иммунодефицитом, это значит, что у этой семьи не может здоровых детей?
Вероятность рождения больного ребенка составляет 25% независимо от варианта наследования заболевания. В настоящее время известны гены, мутации в которых приводят к развитию первичных иммунодефицитов. В большинстве случаев врачи способны помочь семье, проведя на ранних сроках беременности пренатальную диагностику и установив страдает ли плод первичным иммунодефицитом.
Существуют ли ограничения в социальной жизни у детей, страдающих первичными иммунодефицитами?
В большинстве случаев эти дети ведут такой же образ жизни, как и все остальные, исключения составляют дети, страдающие тяжелыми формами иммунодефицита, например ТКИН, которые нуждаются в изоляции и больные после проведения ТКМ.
Автор-составитель – Юрасова Анна, врач-иммунолог
Нарушение работы иммунной системы, сопровождающееся снижением сопротивляемости организма к различным инфекционным поражениям.
Причины
Иммунодефицит ассоциирован с выпадением одного либо сразу нескольких составляющих иммунной системы либо неспецифических факторов, которые с ней находятся в тесном взаимодействии.
Первичный иммунодефицит – это врожденное нарушение, обусловленное генетическими нарушениями либо негативным воздействием на плод во время его внутриутробного развития.
Вторичные иммунодефициты возникают у представителей различных возрастных групп на фоне болезней либо негативного воздействия внешних факторов. Данный тип можно встретить намного чаще, чем первый.
Развитию вторичного иммунодефицита способствуют неправильное питание, заражение гельминтами, хронические инфекционные заболевания, доминирование потери факторов защиты над скоростью их формирования, продолжительная диарея, травмы или операции, дисфункция эндокринной системы, интоксикации различного генеза.
Самый яркий пример вторичного иммунодефицита – СПИД, возникший на фоне заражения вирусом иммунодефицита человека.
Симптомы
Для заболевания характерна предрасположенность организма к самым разным заболеваниям. Такие пациенты болеют намного чаще, чем здоровые люди, при этом заболевания у них практически в тяжелой форме.
Такие больные подвержены развитию частых респираторных инфекций, инфекционных поражений дыхательной системы, воспалительных поражений околоносовых синусов, анемии, аутоиммунных нарушений, тромбоцитопении, диспепсических нарушений, нарушений работы системы пищеварения, реакций гиперчувствительности, нехарактерных реакций на иммунизацию, сепсиса и новообразований.
Диагностика
Симптомы первичного иммунодефицита возникают у младенцев практически сразу после рождения. Для подтверждения диагноза и определения причин нарушения рекомендовано проведение генетических и иммунологических исследований.
Подозрение на развитие у пациента вторичного иммунодефицита может возникнуть при частых повторениях заболеваниях, характеризующихся переходом в хроническую стадию, а также при недостаточной эффективности стандартной терапии и длительном субфебрилитете. Для постановки диагноза пациенту потребуется назначение биохимического и общего анализа крови, иммунограммы и определение цитокинного статуса.
Лечение
При первичных иммунодефицитных состояниях терапия начинается с точного определения причин заболевания. При низком количестве в крови пациента иммуноглобулина ему назначают заместительную терапию, обусловленную введением сывороток, донорской плазмы либо антител. Также пациент получает иммуностимулирующее лечение, направленное на стимуляцию собственных защитных сил больного. При возникновении инфекционных поражений назначают терапию антибиотиками, а также противогрибковыми либо противовирусными препаратами.
При вторичном иммунодефиците акцент делается на лечении причин его вызвавших. В том случае если патология, ассоциирована с хронической инфекцией, рекомендовано проведение своевременной санации воспалительных очагов. Если заболевание возникло на фоне авитаминоза, то пациенту назначают комплексные витаминные препараты.
В некоторых случаях показано назначение иммуностимулирующих препаратов.
Профилактика
Пока не разработано методов профилактики первичных иммунодефицитных состояний.
Для предупреждения развития вторичных иммунодефицитов рекомендовано соблюдение мер, препятствующих заражению ВИЧ-инфекцией.
Главная / Издательство / Иммунодефицитные состояния
5.8. ИММУНОДЕФИЦИТНЫЕ СОСТОЯНИЯ
Иммунодефицитные состояния (ИДС) – это состояния, характеризую-щиеся снижением активности или неспособностью организма к эффективно-му осуществлению реакций клеточного и/или гуморального звена иммуните-та.
По происхождению все ИДС подразделяются на:
— физиологические;
— первичные (наследственные, врожденные). Они являются результатом генетического дефекта, обусловливающего нарушения процессов про-лиферации, дифференцировки и функционирования клеток иммуноком-петентной системы;
— вторичные (приобретенные в постнатальном периоде). Развиваются под влиянием различных факторов физического или биологического харак-тера.
По преимущественному повреждению клеток иммунокомпетентной систе-мы различают 4 группы ИДС:
— с преимущественным повреждением клеточного иммунитета (Т-зависимые, клеточные);
— с преимущественным повреждением гуморального иммунитета (В-зависимые, гуморальные);
— с поражением системы фагоцитоза (А-зависимые);
Физиологические ИДС
Физиологические ИДС включают в себя иммунодефициты (ИД) новорож-денных, беременных и лиц старческого возраста.
1. Иммунодефицит новорожденных. К моменту рождения у здоровых детей в крови содержатся материнские IgG и небольшое количество собст-венных IgG, IgM, IgA. Иммуноглобулины, полученные от матери, содержат антитела против всех видов микробов, с которыми контактировала мать, бла-годаря чему ребенок оказывается защищенным от них на протяжении первых месяцев жизни. Уровень материнских иммуноглобулинов постепенно снижа-ется, и максимальный дефицит их наблюдается через 2-3 месяца после рож-дения. Затем уровень собственных иммуноглобулинов ребенка в крови начи-нает постепенно повышаться, и количество IgM достигает нормального уровня взрослого человека в конце 1-го года жизни у мальчиков и 2-го – у девочек; IgG1 и IgG4 в возрасте 6-8 лет; IgG3 – в 10, а IgG2 — в 12 лет. Кон-центрация IgE достигает нормального уровня взрослого лишь спустя 10-15 лет после рождения. Секреторные IgA отсутствуют у новорожденных и по-являются через 3 месяца после рождения. Оптимальная концентрация секре-торного IgA устанавливается в возрасте 2-4 лет. Плазменный уровень IgA достигает такового показателя у взрослых в 10-12 лет. ИД новорожденных обусловлен тем, что высокое содержание лимфоцитов в периферической крови у новорожденных сочетается с их низкой активностью. У новорожден-ных детей отмечаются также низкая фагоцитарная активность и опсонизи-рующая способность крови. Уровень комплемента у новорожденных снижен и достигает уровня взрослого человека к 3-6-му месяцу жизни.
2. Иммунодефицит беременных. Иммунный статус беременных отлича-ется снижением числа Т- и В-лимфоцитов. Одновременно отмечается повы-шение активности С3-комплемента, что объясняют влиянием плацентарных стероидов на его синтез в печени.
3. Иммунодефицит лиц старческого возраста. Недостаточность имму-нитета при старении проявляется в снижении активности его гуморального и клеточного звеньев. При старении уменьшается общее число лимфоцитов пе-риферической крови. Функциональная активность Т- и В-лимфоцитов при старении падает, снижается интенсивность образования антител в ответ на антигенную стимуляцию. В старческом возрасте в основном продуцируются антитела класса IgM, резко снижена продукция IgA, IgG, подавляется синтез IgE, в связи с чем ослабевает течение атопических аллергических реакций. По мере старения уменьшается фагоцитарная активность макрофагов, ней-трофилов, снижаются активность комплемента, лизоцима и бактерицидная активность сыворотки крови.
Первичные ИДС
Первичные ИДС — это генетически обусловленная неспособность орга-низма реализовать то или иное звено иммунного ответа. Эндогенные, как правило, генетически обусловленные дефекты одного из компонентов им-мунной системы приводят к нарушению системы защиты организма и кли-нически выявляются как одна из форм первичного ИДС. Так как в нормаль-ном функционировании иммунной системы и иммунном ответе участвуют многие типы клеток и сотни молекул, в основе первичного иммунодефицита лежат многочисленные варианты дефектов. Научная группа ВОЗ в 1997 г. выделила более 70 идентифицированных генетических дефектов на различ-ных уровнях преобразования стволовых клеток в Т- и В-лимфоциты или по-следующих этапах их дифференцировки, лежащих в основе первичных ИДС.
В последнее время в связи с обнаружением молекулярных дефектов, со-ставляющих основу многих иммунодефицитов, и существенной вариабель-ностью клинической картины и тяжести их течения, возможностью их позд-ней манифестации, в том числе у взрослых, становится ясно, что первичные ИДС – это не столь редкое состояние, как это считалось до сих пор. Частота значительной части первичных ИДС составляет 1/25000 — 1/50000, хотя такие варианты врожденных иммунных дефектов, как селективный дефицит IgA, встречается с частотой 1/500 — 1/700 человек. По данным ряда авторов, не-достаточность В-системы лимфоцитов и гуморального звена иммунитета от-мечается у 50-75% из общего числа больных ИДС; в 20% случаев отмечается комбинированная недостаточность клеточного и гуморального иммунитета; в 10% — изолированная недостаточность клеточного иммунитета, в 18% — не-достаточность фагоцитоза и в 2% — недостаточность системы комплемента.
ИДС с преимущественным нарушением клеточного звена иммунитета
Патология клеточного звена иммунитета проявляется на различных этапах созревания Т-лимфоцитов — от стволовой клетки до развития их специализи-рованных субпопуляций (рис. 1).

При дефектах преимущественно клеточного звена иммунитета характер-ны частые инфекции дыхательных и мочевыводящих путей, упорные рас-стройства пищеварения, хронический генерализованный кандидоз кожи и слизистых оболочек полости рта, пищеварительного тракта. Кандидозное по-ражение может выявляться в первые месяцы жизни в виде стоматита, дерма-тита, реактивной гиперплазии аденоидной ткани миндалин, лимфатических узлов, отмечается высокая интенсивность кариеса, развиваются бронхоле-гочная патология, фурункулез, в слюне повышено содержание секреторных IgA. Cледует отметить, что CD8 Т-лимфоциты осуществляют иммунологиче-ский надзор за внутренней средой, обеспечивая, в частности, элиминацию клеток, подвергшихся онкогенной трансформации. В случае недостаточности Т-системы лимфоцитов возникает онкогенноопасная ситуация.
1. Синдром Ди Джорджи возникает при гипо- и аплазии вилочковой же-лезы и паращитовидных желез. Заболевание обусловлено нарушением эм-бриональной дифференцировки эпителия в области 3-го и 4-го глоточных карманов. Число лимфоцитов в периферической крови значительно снижено. Синтез гуморальных антител не нарушен, но отмечается дефект в дифферен-цировке стволовых клеток в Т-лимфоциты. У детей с синдромом Ди Джорд-жи не отторгаются кожные трансплантаты, отсутствуют реакции ГЗТ. Забо-левание проявляется в периоде новорожденности (гипокальциемия, судороги, признаки кандидомикоза, инфекции дыхательных и мочевыводящих путей, упорные расстройства пищеварения).
2. Лимфоцитарная дисгенезия (синдром Незелофа) – количественная и качественная недостаточность Т-системы в результате атрофии тимуса и лимфатических узлов. Характеризуется отсутствием клеточных реакций им-мунологической защиты при нормальном содержании иммуноглобулинов в плазме крови. Проявляется в первые недели и месяцы жизни. Отмечаются за-держка развития ребенка, затяжной септический процесс с гнойно-воспалительными очагами во внутренних органах и коже. В периферической крови отмечается крайне низкое содержание лимфоцитов; резко угнетена ре-акция бласттрансформации лимфоцитов; слабо выражена реакция ГЗТ. Со-держание иммуноглобулинов всех классов в периферической крови – в пре-делах нормы. Дети чаще погибают в первые месяцы жизни от сепсиса.
ИДС с преимущественным повреждением В-системы
Гуморальные иммунодефициты относят к наиболее распространенным формам первичных ИДС.
1. Первичная агаммаглобулинемия — болезнь Брутона. Возникает при дефекте созревания предшественников В-клеток в В-лимфоциты. Болеют только мальчики. При агаммаглобулинемии общее содержание -глобу-лина в крови ребенка составляет менее 2 г/л. Тип наследования «классической формы» — рецессивный, сцепленный с Х-хромосомой. Дети с врожденной ги-погаммаглобулинемией могут нормально развиваться до 2-3 лет, хотя у них чаще наблюдаются ранние проявления заболевания в первые месяцы или на первом году жизни. Резко снижена резистентность к условно-патогенным бактериям, грибам. Часто возникают гнойно-вос-палительные заболевания слизистых оболочек, кожных покровов и паренхиматозных органов. Низкая сопротивляемость к бактериальным инфекциям не сочетается со снижением резистентности к вирусам. Некоторые вирусные инфекции (краснуха, корь, вирусный гепатит) у них протекают даже легче, чем у детей с сохраненной иммунологической резистентностью. Однако отмечена высокая чувствитель-ность больных к вирусу полиомиелита. Антигенная стимуляция не приводит к усилению синтеза антител. Показатели, характеризующие клеточный им-мунитет, не отличаются от таковых в норме. Отмечено уменьшение или от-сутствие лимфоцитов и плазмоцитов в костном мозге, последние не содер-жатся также в лимфатических узлах, селезенке.
2. Общая вариабельная гипогаммаглобулинемия (ОВГ). Это гетероген-ная группа ИДС, развитие которых связано с нарушением способности В-лимфоцитов трансформироваться в плазмоциты на фоне антигенной стиму-ляции. Количество циркулирующих в крови В-лимфоцитов не отличается от нормы, однако имеет место нарушение их дифференцировки. Для больных характерны гиперплазия лимфатических узлов, лимфоидного глоточного кольца, иногда – увеличение размеров селезенки. У детей с ОВГ не формиру-ется специфический иммунитет после вакцинации; у них обнаруживается склонность к развитию рецидивирующих воспалительных процессов инфек-ционной природы (синуситы, отиты, хронические пневмонии, фарингиты, тонзиллиты и др.). У взрослых больных ОВГ часто развиваются восходящий холангит и желчнокаменная болезнь, иногда артриты, атрофический гастрит. Общее количество иммуноглобулинов, особенно IgG, снижено.
Недостаточность местного иммунитета у больных ОВГ не коре-лирует с концентрацией плазматического уровня IgA и, вероятно, связана с наруше-ниями синтеза секреторных иммуноглобулинов. У многих больных отмечена склонность к аутоиммунным процессам. Установлено, что у больных ОВГ резко активированы естественные клетки-киллеры, причем их активность в 5 раз превышает нормальные значения.
3. Селективный дефицит иммуноглобулинов. Возможно развитие ИДС с селективным нарушением синтеза IgG, IgA. В основе их формирования могут лежать как блокада развития отдельных субпопуляций В-лимфоцитов, так и, что бывает чаще, повышение активности CD8 популяции лимфоцитов.
Дефицит субклассов IgG. ИДС развивается при дефиците каждого из подклассов, но при исследовании общего содержания IgG в крови редко об-наруживаются отклонения от нормальных значений, чаще оно в норме или повышено. Так как созревание клонов В-лимфоцитов, секретирующих IgG2 и IgG4, происходит не ранее 2-го года жизни, у детей раннего возраста имеется физиологический дефицит данных субклассов. Дефицит IgG2 обнаруживает-ся у 50% больных первичным ИДС, очень часто при общей вариабельной ги-поглобулинемии и, как правило, у детей старшего возраста проявляется хро-нической пневмонией и синдромом мальабсорбции. Селективный дефицит IgG1 может быть компенсирован за счет образования антител, относящихся к другим субклассам.
Изолированный дефицит IgA — одна из самых частых аномалий иммун-ной системы. Для него характерны низкое содержание IgA в сыворотке крови (менее 50 мг/л), отсутствие дефицита других классов иммуноглобулинов, нормальная способность организма к продукции антител, мало измененные показатели клеточного иммунитета. Так как IgA — основной иммуноглобулин системы местного иммунитета (секреторный IgA), обращают внимание на связь его дефицита с рецидивирующими и хроническими заболеваниями ды-хательных путей и ЛОР-органов. При отсутствии или низком содержании IgA в секретах создаются условия для развития аллергических и аутоиммун-ных заболеваний, предпосылки для развития дисбактериоза и воспалитель-ных заболеваний желудочно-кишечного тракта. С селективным дефицитом IgA может быть связано возникновение рецидивирующего герпетического стоматита, язвенного колита, регионального энтерита и др.
ИДС с поражением системы фагоцитоза
По механизму развития фагоцитарная недостаточность делится на три ос-новные формы:
Лейкопеническая — развивается вследствие подавления процессов проли-ферации и созревания моноцитов (ионизирующее излучение, ряд токсинов, цитостатики и др.) либо в результате наследственной блокады деления и дифференцировки, например миелоидной стволовой клетки.
Дисфункциональная — характеризуется расстройствами различных этапов процессов фагоцитоза и презентации антигена (подвижности фагоцитов, их адгезивных свойств, поглощения объекта фагоцитоза, переработки его и представления антигена лимфоцитам).
Дисрегуляторная — развивается вследствие нарушения регуляции различ-ных этапов фагоцитарной реакции биологически активными веществами (нейромедиаторами, гормонами, простагландинами, биогенными аминами, пептидами и др.).
Комбинированные ИДС
Характеризуются нарушением дифференцировки стволовых клеток, бло-ком созревания Т- и В-лимфоцитов и их дефицитом. Комбинированные фор-мы иммунодефицита встречаются чаще, чем селективные. Как правило, они связаны с нарушением центральных органов иммунной системы. При комби-нированных ИДС ведущая роль принадлежит дефекту Т-клеток.
1. Cиндром ретикулярной дисгенезии — характеризуется уменьшением в костном мозге количества стволовых клеток. Характерна внутриутробная ги-бель плода, или дети гибнут вскоре после рождения.
2. «Швейцарский» тип иммунодефицита — характеризуется поражением Т- и В-систем и, следовательно, нарушением клеточных и гуморальных реак-ций иммунологической защиты. При аутосомно-рецессивных формах по крайней мере у 40% больных обнаруживается недостаточность аденозинде-заминазы, что ведет к нарушению метаболизма аденозина, блокаде синтеза гипоксантина и блокаде в результате этого созревания Т-клеток. У части де-тей на мембранах Т-лимфоцитов отсутствуют антигены МНС 1-го или 2-го класса. Содержание В-клеток может соответствовать норме или превышать ее, но эти клетки не способны секретировать иммуноглобулины в достаточ-ном количестве.
Заболевание проявляется в первые месяцы жизни и часто характеризуется злокачественным течением. Наблюдается задержка прибавки массы тела, уже в первые дни жизни у некоторых детей появляются кореподобные высыпа-ния на коже, что может быть связано с реакциями несовместимости по отно-шению к материнским лимфоцитам, поступающим через плаценту в крово-ток ребенка. Развиваются признаки кожного кандидоза, диарея, острая ин-терстициальная пневмония, приобретающая затяжной и рецидивирующий характер. Дети очень восприимчивы к вирусным инфекциям. В крови выяв-ляется значительная лимфопения, особенно низко содержание Т-лимфоцитов. Содержание иммуноглобулинов всех классов заметно снижено. Исключение составляют грудные дети с IgG, полученными от матери. Патог-номоничны изменения вилочковой железы, гипоплазия миндалин и лимфа-тических узлов. Возникает неспособность проявлять реакции гиперчувстви-тельности замедленного типа. Дети редко доживают до 2-летнего возраста.
3. Синдром атаксии-телеангиэктазии (синдром Луи-Бар) обусловлен дефектом созревания, снижением функции Т-лимфоцитов, уменьшением их числа в крови (особенно Т-хелперов), дефицитом иммуно-глобулинов (осо-бенно IgA, IgE, реже IgG). Синдром характеризуется сочетанием атаксии и других неврологических отклонений с телеангиэктатическими изменениями сосудов склер, лица. Поражение нервной системы проявляется симптомами выпадения функций мозжечка, подкорковых ганглиев, диэнцефальной облас-ти, пирамидной системы. В результате их поражений возникают нарушение походки, замедленность произвольных движений, гиперкинезы, вегетососу-дистая дистония. У многих отмечаются вялотекущие пневмонии, развивают-ся ателектазы, пневмосклероз и бронхоэктазы. При исследовании лимфати-ческой системы устанавливается гипоплазия вилочковой железы, лимфатиче-ских узлов, селезенки. У многих детей отмечается уменьшение содержания в крови лимфоцитов, снижена реакция бласттрансформации лимфоцитов, не определяется IgA.
Заболевание характеризуется аутосомнорецессивным типом насле-дования.Прогноз синдрома неблагоприятен. Около 50% летальных исходов обусловлено хроническим поражением бронхолегочной системы, около 20% — развитием злокачественных процессов, которые связывают с утратой функ-циональной активности тимусзависимых лимфоцитов, а в общем плане – с отсутствием цензорной функции вилочковой железы – функции иммуноло-гического надзора. Некоторые больные доживают до 40-50 лет.
4. Синдром Вискотта-Олдрича характеризуется дефицитом перифери-ческих Т-лимфоцитов, нарушением их структуры и физико-химических свойств мембран, уменьшением клеточного иммунитета. Дефект, вероятно, связан с отсутствием на клеточной мембране лимфоцитов и тромбоцитов гликопротеида с относительной молекулярной массой 110 kD. При этом за-болевании выявляются снижение плотности микроворсинок на лимфоцитах, нарушение активации Т-лимфоцитов и не объясненная до сих пор нестабиль-ность экспрессии сиалогликопротеинов. Иммунологическая недостаточность обусловлена гипофункцией вилочковой железы. Часто обнаруживаются де-фицит IgM при нормальном содержании IgG и увеличение уровня IgA, IgE в крови. Характерно уменьшение продукции антител к антигенам-полисахаридам, но эти больные нормально реагируют на белковые антигены. Кроме того, имеют место врожденные дефекты тромбоцитов (нарушения ад-гезии, агрегации), тромбоцитопения. Болеют только мальчики. Заболевание проявляется в раннем возрасте, иногда в периоде новорожденности. Дети страдают частыми вирусными и бактериальными инфекциями. Характерны рецидивирующий гнойный отит, экзема, пиодермии, пневмония, колиты. Ге-моррагический синдром может быть ведущим.
Прогноз тяжелых форм неблагоприятен, дети погибают в возрасте до 10 лет. К летальному исходу приводят инфекции, геморрагии или злокачест-веннные новообразования лимфоретикулярной системы.
Недостаточность системы комплемента
Система комплемента представлена протеолитическими ферментами и ре-гуляторными белками. В крови имеются 20 комплементарных факторов, ак-тивация которых может осуществляться классическим или альтернативным путем. Активация комплемента обеспечивает защиту организма от любых чужеродных агентов; с активацией комплемента связаны и повреждающие эффекты при развитии аллергических и аутоиммунных реакций. При врож-денном и приобретенном расстройстве комплементарных факторов наруша-ются процессы фагоцитоза и происходит освобождение биологически актив-ных веществ.
При врожденном дефиците С1 невозможна активация системы компле-мента по классическому пути, поэтому, вследствие нарушения фаго-цитоза и лизиса микробов, наблюдаются повторные тяжелые гнойные процессы. При врожденном дефиците ингибитора С3б постоянно активируется комплемент С3, в результате чего содержание его в крови уменьшается. Хотя количество предшествующих комплементарных факторов (С1, С2, С4) не изменяется, однако из-за дефицита С3 нарушаются процессы фагоцитоза и лизиса бакте-рий, что проявляется повторными гнойными инфекциями.
При врожденном дефиците С5 склонность к инфекции также связана с на-рушением фагоцитоза и лизиса из-за невозможности образования соответст-вующих компонентов комплемента.
Содержание комплемента у детей на 30% ниже, чем у взрослых, что дела-ет понятным их склонность к инфекции и сепсису. Расстройства системы комплемента приобретенного характера проявляются в измене-нии количест-ва комплементарных факторов. При поражениях печени (цирроз, гепатит, хронический холецистит) нарушается синтез С1, С3, С6, С9. С другой сторо-ны, при аллергических, аутоиммунных заболеваниях комплементарные фак-торы уменьшаются в крови из-за связывания их иммунными комплексами.
Принципы лечения первичных ИДС
Лечение зависит от типа первичной иммунологической недостаточ-ности. Выделяются 3 основных направления иммунокоррекции.
Иммунная инженерия (трансплантация органов и тканей иммунной сис-темы: эмбриональной печени, тимуса, комплекса тимус-грудина, костного мозга, клеток иммунной системы; введение -глобулинов, иммуноглобулинов отдельных классов; сорбционные методы: гемосорбция, аффинная сорбция, иммуносорбция).
Коррекция гормонами и медиаторами иммунной системы (тимические гормональные факторы, миелопептиды, цитокины типа интерферона, интер-лейкины).
Фармакологическая коррекция — левамизол, диуцифон, полианионы и др.
Также применяется активная иммунизация против частых инфекций с по-мощью убитых вакцин, вводятся антибиотики, сульфаниламиды, противо-грибковые препараты.
предыдущий раздел |
