Виферон или анаферон что лучше?
■ О. И. Карпов и ар. Путь повышения эффективности и переносимости антибиотикотерапии при синусите у летей
Таблица 5. Нежелательные эффекты примененных антибиотиков при синусите у детей
Заключение
Итак, нами впервые в отечественной практике получены подтверждения большей клинической эффективности, более быстрого наступления клинического эффекта и принципиально лучшей переносимости амоксициллина/клавуланата в форме Солютаб, чем Аугментина, что существенным образом расширяет возможности антибиотикотерапии синусита. Повышение всасывания клавуланата уменьшает вероятность нежелательных эффектов со стороны желудочно-кишечного тракта. По сути дела мы впервые сталкиваемся с ситуацией, когда воспроизведенный препарат оказывается по своим свойствам лучше оригинала.
Таким образом, применение флемоклава Солютаб при остром синусите у детей более эффективно, чем использование обычных форм амоксициллина/ клавуланата, и сопровождается достоверно лучшей переносимостью антибиотикотерапии.
Литература:
G. Tellier, S. A. Brunton, R. Nusrat // South Med. J. — 2005. — V. 98. — № 9. — P. 863—868.
9. Amoxicillin clavulanic acid: bioequivalence of a novel Solutab tablet and rationale for a twice-daily dosing regimen /
H. Sourgens et al. // Int. J. Clin. Pharmacol. Ther. — 2004. — V. 42. — № 3. — P. 165—173.
10. Vandenplas Y. Gastroesophageal reflux: medical treatment // J. Pediatr. Gastroenterol. Nutr. — 2005. — V. 41 (Suppl. 1). — P. S41—42.
Нежелательный эффект (л) флемоклав Солютаб Аугментин
Диарея 1 6
Боли в животе — 3
Запор 1 —
Аллергические реакции 2 3
Поражения грибами слизистых оболочек 1 1
Всего 5 13
Противовирусная терапия ОРВИ у детей
Ф. И. Ершов, С. С. Григорян, Т. Г. Орлова, Т. А. Семененко, Л. Н. Мазанкова, Т. А. Чеботарева, Л. Ф. Нестерина, Е. И. Исаева
ГУ НИИ эпидемиологии и микробиологии им. Н. ф. Гамалеи РАМН, Кафедра детских инфекционных болезней ГОУ ДПО РМАПО Росздрава, ГУ НИИ вирусологии им Д. И. Ивановского, Москва
В настоящем исследовании проведен сравнительный анализ эффективности терапии ОРВИ у детей тремя известными отечественными препаратами: арбидолом, вифероном и анафероном. Было обследовано 88 детей с ОРВИ различной этиологии в возрасте от 1 года до 7 лет. Дети I группы в дополнение к базисной терапии получали виферон (28 пациентов), II — арбидол (20 детей), III — анаферон (22 ребенка), IV — получали только базисную терапию (группа контроля — 18 детей). В результате исследования рекомендовано при гриппе и других ОРВИ детям 1 —7 лет назначать виферон-2 при тяжелом дебюте заболевания пятидневным курсом с 1 —2-го дня болезни. Для лечения пациентов с клиническими симптомами гриппа, а также имеющих указание на контакт с больным гриппом в период эпидемического подъема заболеваемости, препаратами выбора являются арбидол и виферон. Ключевые слова: ОРВИ, грипп, арбидол, виферон, анаферон, дети
Актуальность проблемы ОРВИ не вызывает сомнения и определяется, прежде всего, высоким уровнем заболеваемости среди детей всех возрастных групп. По данным федерального центра Госсанэпид-
надзора России в разные годы она составляет от 50 000 до 72 000 случаев на 100 тысяч детского населения до 14 лет . Кроме этого у детей наиболее высок риск возникновения тяжелых синдромов (синдром
Таблица 1. Динамика иммунологических показателей при разных видах терапии
Показатель (%) Базисная терапия +
Виферон Арбидол Анаферон Контроль
(1 группа) (II группа) (III группа) (IV группа)
СР16 до лечения 12,82 ± 0,36 9,25 ± 4,13 14,57 ± 7,09 12,71 ± 6,63
СР16 после лечения 17,37 ± 3,21 8,7 ± 5,11 10,92 ± 5,96 11,67 ± 5,57
Р < 0,05 > 0,05 > 0,05
СР38 до лечения 12,82 ± 0,36 11,5 ± 6,5 18 ± 6,2 20 ± 12,40
СР38 после лечения 17,37 ± 3,21 10,5 ± 5,26 17,69 ± 7,74 25 ± 11,50
Р > 0,05 > 0,05 > 0,05
СР71 до лечения 2,0 ± 0,4 0 ± 0,1 1,5 ± 0,3 0 ± 0,3
СР71 после лечения 7,39 ± 2,23 0 ± 0,2 2,0 ± 0,4 0 ± 0,2
Р < 0,05 > 0,05 > 0,05
Статистическое различие (р) приводится в сравнении с группой контроля после лечения.
крупа, нейротоксикоз, судорожный синдром, бронхит и др.) и бактериальных осложнений, которые определяют тяжесть, длительность и исход заболевания.
ОРВИ — полиэтиологическая группа инфекций дыхательных путей, где ведущую роль играют многочисленные респираторные вирусы (вирусы гриппа типов А, В, С, парагриппа, респираторно-синцитиаль-ный вирус, аденовирусы, коронавирусы) и другие агенты, тропные к эпителию респираторного тракта. При оценке тяжести и выборе терапевтической тактики ОРВИ необходимо учитывать повреждающий эффект возбудителя заболевания, особенности клинических проявлений, свойственных вирусной инфекции, динамику клинической картины. Известно, что вирусы (особенно вирус гриппа) вызывают дегенерацию, некроз и метаплазию эпителия, влияют на проницаемость кровеносных и лимфатических сосудов, нарушают фагоцитоз и хемотаксис, уменьшают мукоцилиарный клиренс, увеличивают бактериальную адгезию и колонизацию патогенными микробами.
Различные респираторные вирусы могут вызвать однотипную, сходную клиническую картину, что затрудняет дифференциальную диагностику заболевания. С другой стороны, каждой вирусной инфекции характерны признаки, позволяющие по клинической картине заподозрить и поставить правильный диагноз. Так, например, в клинической диагностике гриппа надо учитывать два механизма агрессии вируса: эпителиотроп-ность (преимущественное поражение гортани, трахеи, крупных и средних бронхов с развитием характерной клинической картины ларингита, крупа, бронхита) и токсичность (токсикоз, судорожный синдром, возможное развитие инфекционно-токсического шока и синдрома Рейе при наиболее тяжелых вариантах заболевания) . При парагриппозной инфекции решающее значение имеет остро возникающий синдром крупа (острый стенозирующий ларингит, ларинготра-хеобронхит) при умеренно выраженном токсикозе. Не исключается развитие обструктивного бронхита, брон-хиолита. Наиболее часто поражаются дети первых двух-трех лет жизни . Наиболее широк диапазон клинических проявлений аденовирусной инфекции из-
за особых свойств аденовирусов: поражаются дыхательные пути (преимущественно крупные и средние бронхи), лимфоидная ткань при умеренно выраженном общетоксическом синдроме, который, в основном, проявляется фебрильной лихорадкой. При респираторно-синцитиальной инфекции ведущим клиническим симптомом является бронхиолит, симптомы токсикоза не выражены. При манифестных формах ОРВИ имеются типичные признаки заболевания, позволяющие клинически заподозрить ту или иную вирусную инфекцию. Вместе с тем, при легких и среднетяжелых формах все респираторные вирусы могут вызвать сходную клиническую картину, весьма затрудняющую дифференциальную диагностику между ними, и, как следствие, выбор этиотропного средства для терапии.
Противовирусные препараты различаются по механизму действия на этиопатогенез ОРВИ: химиопрепа-раты подавляют внеклеточные вирионы (оксолин, бо-нафтон), способны препятствовать адсорбции вирусов на клетки-мишени (ремантадин, арбидол) и угнетать синтез вирусных РНК и ДНК (рибавирин, виразол); ин-терфероны (природные, рекомбинантные) активируют внутриклеточные ферменты, вследствие чего снижается синтез вирусных белков и выход вирионов из клетки, способны активировать натуральные киллеры,
макрофаги.
%
60,0-т
50,0-40,0-30,0-20,0-10,0-0,0- я
кий лизис ческий температура
» Арбидол С Виферон А Анаферон О Контроль Рисунок 1. Влияние терапии на темп снижения лихорадки
АРБИДОЛ Насморк
□ Контроль
АНАфЕРОН Насморк
Синдром крупа
Осиплость
физикальные изменения легких
Осиплость
физикальные изменения легких
Рисунок 2. Влияние терапии на сроки купирования респираторного синдрома
Ограничения для проведения специфической химиотерапии ОРВИ обусловлены не только трудностями клинической диагностики. Различная чувствительность вирусов, быстро развивающаяся их резистентность к препаратам, высокая частота смешанных форм ОР3, высокая токсичность лекарственных средств этой группы делают терапию неэффективной, а иногда и невозможной из-за возрастных ограничений . Лишены подобных недостатков используемые в клинике препараты интерферонов, обладающие широким спектром противовирусной активности и иммуномодулирующи-ми эффектами. В последнее время для терапии ОРВИ предлагаются и гомеопатические препараты. Мировой опыт показывает, что безусловный приоритет принадлежит противовирусным препаратам и интерферонам, выбор которых в настоящее время достаточно широк . Несмотря на это, отсутствуют четкие рекомендации для рационального выбора конкретного препарата, так как большинство исследований проводится без учета законов доказательной медицины (двойной слепой контроль, применение плацебо и препаратов сравнения, мониторинг лабораторных показателей и пр.).
В настоящем исследовании проведен сравнительный анализ эффективности терапии ОРВИ у детей тремя известными отечественными препаратами: арби-долом, вифероном и анафероном. Арбидол — химио-препарат этиотропного действия — ингибирует слияние липидной оболочки вирусов гриппа А и В с мембранами клеточных эндосом, обладает иммуномодулирующим эффектом. Виферон суппозитории — комбинированный препарат, в состав которого входят рекомбинант-ный интерферон а2Ь, токоферол ацетат, аскорбино-
вая кислота. Обладает широким спектром антивирусной и иммуномодулирующей активности. Анаферон — гомеопатический препарат, содержащий сверхмалые дозы антител к у-интерферону человека. Предлагается разработчиками как детский иммуномодулятор, обладающий антивирусной активностью. Учитывая схожесть механизма действия названных препаратов, их противоречивую оценку в литературе мы попытались сопоставить клиническую эффективность арбидола, ви-ферона и анаферона с показателями интерферонового (ИфН) и иммунного статуса детей, больных гриппом и др. ОРВИ.
Материалы и методы исследования
Исследование проводилось в период с 1998 по 2005 гг. на базе Тушинской детской городской больницы г. Москвы.
С целью выявления клинической эффективности ви-ферона, арбидола, анаферона было обследовано 88 детей с ОРВИ различной этиологии в возрасте от 1 года до 7 лет. Дети I группы в дополнение к базисной терапии получали виферон (28 пациентов), II — арбидол (20 детей), III — анаферон (22 ребенка), IV — получали только базисную терапию (группа контроля — 18 детей). Виферон назначался в дозе 500 тысяч МЕ интерферона в суппозитории (Вифе-рон-2) по 1 суппозиторию 2 раза в день; арбидол — в дозе 0,05 г 3 раза в день; анаферон назначался по схеме: в первые 2 часа лечения по 1 растворенной в воде таблетке каждые 2 часа (5 табл.), затем еще 3 таблетки через равные промежутки времени, со 2-х суток лечения по 1 таблетке 3 раза в день. Лечение
-46 «35
■46 «35
■40 ■20
-80 -40
-50 -30
40 30
40 -40 25 -35
80 г90 *
Е-60 -60 -60
40 «» -40 -40 —
т; -30 -тп —
-60 -60 «» _ -40 -40 -30 | 20 -30 «30
1—2
3—4 дни болезни
6—8
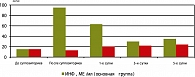
Рисунок 3. Влияние терапии на способность лейкоцитов к продукции а-ИфН (биометод): * — различие достоверно (виферон—контроль); *1 — различие достоверно (анаферон до терапии— анаферон после терапии)
— Виферон
— Арбидол
— Анаферон
— Контроль
препаратами проводилось 5-дневным курсом во всех группах детей.
Для этиологической расшифровки диагноза применяли метод твердофазного иммуноферментного анализа индикации и идентификации вирусных антигенов и специфических антител в сыворотке крови больных. Этиологическая структура ОРВИ была представлена ведущими респираторными вирусами: гриппа, парагриппа, аденовирусом и др. В среднем частота регистрации гриппа как моноинфекции или смешанной с парагриппом инфекции по группам составила 51,1% случаев. Однако, у больных, получавших виферон, грипп регистрировался достоверно чаще, чем у детей, получавших арбидол и анаферон (72,9% против 25 и 25% соответственно). Пациенты поступали в стационар в первые двое суток заболевания с жалобами на фебрильную лихорадку, плохое самочувствие и головную боль у старших детей; беспокойство, нарушение ритма сна, бледность, отказ от еды у детей младшего возраста. У всех больных отмечался респираторный синдром: заложенность носа до выраженного ринита, кашель, хрипы в легких. У 57% больных отмечалась клиника крупа I—II, II степени, практически у всех отмечался бронхит разной степени выраженности. У 23,7% больных состояние было тяжелым.
Наряду с клинической оценкой больным проводилось иммунологическое обследование: определяли ин-терфероновый (ИфН) статус, отдельные параметры иммунного статуса. Исследование ИфН-статуса проводилось всем больным в 1—2, 3—4 и 6—8-й дни болезни и включало определение сывороточного ИфН, а также способности лейкоцитов к продукции а- и у-ИфН в интерфероновой реакции лейкоцитов (ИРЛ) биологическим методом. У 40 пациентов был использован иммуноферментный метод для определения уровней сывороточного, спонтанного и индуцированного а- и у-ИфН. Особое внимание уделялось оценке функционального состояния клеточного звена иммунитета — учитывалось число активированных Т-лимфоцитов (CD38, CD71) и натуральных киллеров (CD16), изученных методом ИфА.
Результаты исследований обработаны методами вариационной статистики и корреляционного анализа с использованием пакета стандартизированных программ «Paradox», «Qwatro». Статистический анализ данных проводился в лаборатории медицинской информатики ГУ НИИ неврологии РАМН (рук. — д.м.н. Реброва О. Ю.) с использованием коммерческого пакета программ STATISTICA 6.0 (StatSoft Inc., США).
Проверка гипотез о виде распределений признаков осуществлялась с помощью методов Лиллефорса, Колмогорова-Смирнова, Шапиро-Уилка. Для количественных и качественных порядковых признаков сравнение несвязанных групп проводилось с использованием теста Манна-Уитни. Для качественных признаков с целью сравнения несвязанных групп проводился анализ таблиц сопряженности с использованием критерия X2 с поправкой Иетса и точного критерия фишера. При сравнении связанных групп (анализ динамики) применялся метод Вилкоксона.
Во всех видах статистического анализа различия считались статистически значимыми при достигнутом уровне значимости р < 0,05.
Результаты и их обсуждение
Критериями клинической эффективности препаратов при ОРВИ являлись сроки и темпы обратного развития основных проявлений болезни.
Прежде всего мы оценили влияние препаратов на темп снижения и длительность лихорадки. Оказалось, что у больных, получавших виферон и арбидол, критическое снижение температуры отмечалось значительно чаще, чем у детей в группе контроля (53,6 и 55% соответственно против 33,3%, р < 0,05). «Обрывающий» лихорадку эффект отмечался у всех больных гриппом, получавших арбидол. Вероятней всего этот эффект можно объяснить противовирусным действием виферона и арбидола, подкрепленным универсальностью виферо-на в отношении всех респираторных вирусов и подтверждением узкого противовирусного эффекта в отношении вирусов гриппа у арбидола. Статистически значимого влияния анаферона на вариант купирования лихорадки у больных не выявлено (рис. 1). Длительность лихорадки у пациентов с неосложненным течением ОРВИ составила 1—6 дней и по средним показателям (I группа — 2,29 ± 0,21; II — 2,11 ± 0,3; III — 2,89 ± + 0,65 дня, у детей группы контроля (IV) — 3,5 + + 0,57, р > 0,05) не выявлено влияния на продолжительность лихорадки всех вариантов терапии.
Токсикоз у получавших виферон и арбидол проявлял тенденцию к более быстрому купированию. Клинически это проявлялось улучшением самочувствия, аппетита, исчезновением бледности кожи и видимых слизистых, нормализацией пульса. Длительность интоксикации у больных, получавших виферон, составляла 2,33 + 0,55 дня, у получавших арбидол — 2,0 + 1,3 дня по сравнению с группой контроля — 3,29 + 0,66 (р > 0,05), у получавших анаферон — 2,84 + 0,35 дня. Вместе с тем, значимым оказалось различие в сроках восстановления двигательной активности у пациентов I группы — 1,67 + 0,41 дня на фоне виферонотерапии, 2,84 + + 0,35 — в группе контроля, р < 0,05.
Что касается влияния виферона, арбидола и анафе-рона на респираторный синдром, то воздействие их было неоднозначным. Так продолжительность кашля, бронхита, ринита при назначении виферона была наименьшей, чем в контрольной группе больных или у больных, получавших арбидол и анаферон (рис. 2). Хотя достоверного влияния препаратов на сроки купирования синдрома крупа не выявлено, тем не менее интенсивность проявлений каждого симптома (голос, кашель, стенотическое дыхание) заметно снижалась при назначении всех препаратов.
Бактериальные осложнения (пневмония, отит, гайморит) отмечались, как правило, у детей с неблагоприятным преморбидным фоном, но у больных, получавших виферон или арбидол, при прочих равных условиях регистрировались достоверно реже, чем в контрольной группе (3,3 против 8,8%, р < 0,05).
Известно, что пребывание больных в респираторном отделении сопряжено с опасностью наслоения новой вирусной инфекции в раннем периоде реконва-лесценции основного заболевания. В нашем исследовании мы зафиксировали факт развития суперинфекции у 1 ребенка в III группе. На фоне терапии виферо-
ном и арбидолом, а также в группе контроля суперинфицирования не было.
Таким образом, наиболее выраженный положительный клинический эффект в течении и исходе ОРВИ у детей был отмечен при назначении виферона и арби-дола.
Исследование ИфН-статуса у больных выявило определенные закономерности его динамики, коррелирующие с периодом и тяжестью болезни. В первые 1 — 2 дня болезни по средним показателям отмечено достоверное повышение уровня сывороточного ИфН по сравнению с «нормой». Однако у части детей (36,4%) изменений этого показателя не отмечено. Более чем у половины этих пациентов заболевание протекало в тяжелой форме, что достоверно (в 4,3 раза) превышает частоту этой формы у детей с более высокими «стартовыми» показателями сывороточного ИфН. Следует отметить, что именно эти дети составляли большую часть группы тяжелобольных, при этом более половины из них были в раннем возрасте (1—3 года). В динамике сывороточной концентрации ИфН выявлены следующие особенности: повышенный уровень ИфН у детей сохранялся в 1—2 дни болезни, а с 3-го дня болезни происходило его быстрое снижение. Наряду с этим, начиная с ранних сроков заболевания, наблюдалось угнетение ИфН-продуцирующей способности лейкоцитов, обусловленное, как свидетельствуют исследования ряда авторов, выработкой «сигнального» белка («фактор-1»), проявляющего тормозящее действие в отношении названной функции лейкоцитов . Включение в терапию наблюдаемых больных виферона оказывало существенное влияние на ин-терфероновый статус. Через 1—2 дня после начала лечения (3—4 дни болезни) отмечалось повышение сывороточного ИфН, которое сохранялось и к периоду реконвалесценции — 6,40 + 0,98 МЕ/мл и 2,90 + + 0,64 МЕ/мл в контроле, р < 0,05. Назначение ви-ферона также положительно влияло на способность клеток синтезировать а- и у-ИфНы. Исследование на 3—4 дни болезни показало увеличение доли детей с нормальными или незначительно сниженными показателями при применении виферона, тогда как в группе контроля происходил обратный процесс. Достоверным оказалось влияние виферона на стимуляцию у-интерфероногенеза — 15,0 + 3,0 МЕ/мл против 4,3 + 2,8 МЕ/мл в контрольной группе, р < 0,05, исследование способности лейкоцитов к продукции а-ИфН выявило аналогичную тенденцию (рис. 3). При исследовании на 6—8 дни болезни динамики показателей не наблюдалось. Включение в терапию арбидо-ла и анаферона не влияло на изменение концентрации сывороточного ИфН в динамике наблюдения. Не получено статистически значимых по сравнению с контролем различий в способности лейкоцитов к продукции а- и у-интерферонов. Однако, при анализе показателей ИфН статуса в динамике терапии арбидолом методом ИфА получена достоверная стимуляция указанной функции по у-ИфН к 6—8 дню болезни — 524,85 пг/мл против 186,15 пг/мл — в 1—2 дни.
Динамика иммунных показателей у большинства наблюдавшихся пациентов характеризовалась уменьшением общего количества Т-лимфоцитов и их субпо-
пуляций (С04, С08, С016) при увеличении числа активированных клеток (С038, С071, С08, С016) в разгар болезни с последующей инверсией в период выздоровления. Лечение вифероном способствовало увеличению количества активированных клеток С071. У детей, получавших виферон, отмечался также эффект модуляции пролиферации цитотоксических клеток и естественных киллеров (табл. 1). Терапия арби-долом и анафероном не оказывала влияния на динамику иммунологических показателей.
Заключение
Таким образом, целесообразно рекомендовать при гриппе и других ОРВИ детям 1—7 лет терапию вифероном-2 при тяжелом дебюте заболевания пятидневным курсом с 1—2-го дня болезни. Для лечения пациентов с клиническими симптомами гриппа, а также имеющих указание на контакт с больным гриппом в период эпидемического подъема заболеваемости, препаратами выбора являются арбидол и виферон.
Литература:
1. Информация Федерального центра Госсанэпиднадзора МЗ Рф: «Инфекционная заболеваемость в Российской Федерации» за 2003—2005 гг.
2. Камышев М. В., Стефанов В. Е. Грипп: путь решения проблемы. — «ЭЛБИ-СПб», 2002.
5. Ершов ф. И. Противовирусные препараты. — М., «ГЭОТАР-Медиа». — 2006.
7. Ленва И. Механизм вирусспецифического действия препарата арбидол. Получение и характеристика арбидолрезис-тентных мутантов / И. Ленва, А. Хей // Актуальные вирусные инфекции — теоретические и практические аспекты. — СПб, 2004. — С. 41.
9. фармакология сверхмалых доз антител к эндогенным регуляторам функции / О. И. Эпштейн и др. — Издательство РАМН, 2005. — С. 131—137.
Опыт ПРИМЕНЕНИЯ Иммунала® ПРИ ОРВИ со стенозируюшим ларинготрахеитом у часто и длительно болеюших детей
Ф. С. Харламова, С. Л. Бевза, О. В. Кладова, Т. П. Легкова, Л. И. Фельдфикс, В. Ф. Учайкин
ГОУ ВПО РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ РОСЗДРАВА, МОРОЗОВСКАЯ ДЕТСКАЯ ГОРОДСКАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА, МОСКВА
Целью исследования явилась оценка терапевтической эффективности и безопасности Иммунала® в качестве иммуностимулирующего средства в комплексном лечении острых респираторных инфекций (ОРИ) со стенозирующим ларинготрахеитом у 50 часто болеющих детей в возрасте от 1 года до 14 лет. Из них 30 детей в испытуемой группе получали Иммунал™ с лечебной целью в течение 7 дней. Среди них ОРВИ со стенозирующим ларинготрахеитом 1 ст. стеноза была у 20 и со 2 ст. стеноза — у 10 больных, острый средний отит (ОСО) был у 4 детей, атопический дерматит — у 4 детей. 20 детей группы сравнения получали базисную терапию (симптоматическую и патогенетическую). Среди них ОРВИ со стенозирующим ларинготрахеитом 1 ст. стеноза была — у 12, со 2 ст. стеноза — у 8 детей, ОСО был у 2, конъюнктивит — у 1, атопический дерматит — у 2 детей. У 22 детей проводилась антибиотикотерапия (цефазолином, азитромицином или макропеном), т. к. ОРВИ расценивалась как осложненная бактериальной инфекцией. При применении Иммунала™ достигалось сокращение продолжительности основных клинических симптомов при ОРИ вирусной и вирусно-бактериальной этиологии со стенозирующим ларингитом у детей. Иммунал ™ способствует эрадикации патогенов и улучшает микробиоценоз ротоглотки при ОРВИ со стенозирующим ларинготрахеитом, сокращает сроки антиби-отикотерапии, ускоряет процесс выздоровления и обеспечивает более гладкое течение заболевания. Ключевые слова: ОРВИ, стенозирующий ларинготрахеит, Иммунал™, дети
Острые респираторные инфекции (ОРИ) являются наиболее частой патологией и в структуре всей заболеваемости детского возраста составляют не менее 90%. Многие дети болеют ОРЗ практически ежемесячно, составляя группу так называемых «часто болеющих детей» (ЧБД). Численность их в популяции составляет по данным различных авторов 4—40% .
Инфекции респираторного тракта у этой категории детей часто носят вирусно-бактериальный характер и нередко приводят к осложнениям. Кроме того, более половины этих детей страдают хроническими заболеваниями носо- и ротоглотки, рецидивами ларинго- и/или бронхообструкции, острого среднего отита (ОСО), синусита и пр. В результате частых ОРЗ формируются
Минздрав РФ выпустил временные методические рекомендации по профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19) (версия 5 от 08.04.2020). Данные рекомендации в значительной степени основаны на материалах по COVID-19, опубликованных специалистами ВОЗ, китайского, американского и европейского центров по контролю за заболеваемостью, нормативно-правовых документах Минздрава РФ и Роспотребнадзора, а также на результатах анализа отечественных и зарубежных научных публикаций.
В первую очередь данный документ предназначен для специалистов и содержит информацию об обеспечении максимально эффективного ведения больных в стационаре.
Но что же полезного из этих рекомендаций могут почерпнуть обычные граждане?
Согласно рекомендациям Минздрава, в связи со сходством клинической картины легких форм COVID-19 с клинической картиной сезонных ОРВИ, до подтверждения этиологического диагноза в схемы терапии следует включать препараты, рекомендованные для лечения сезонных ОРВИ, такие как интраназальные формы интерферона альфа, препараты индукторов интерферона, а также противовирусные препараты с широким спектром активности.
Что это за препараты и почему на них возлагают надежду специалисты?
Начнем с того, что такое интерфероны. Это — группа биологически активных белков, синтезируемых клетками организма как часть защитной реакции на чужеродные агенты, (например, на вирусы). Система интерферона, включающая сами интерфероны, а также молекулы, распознающие их, существует в каждой клетке нашего организма. Интерфероны оказывают влияние на весь каскад защитных реакций организма, что делает их важнейшим фактором защиты от инфекций. К основным эффектам интерферонов можно отнести противовирусный, антимикробный, иммуномодулирующий и ряд других.
Интерфероны вырабатываются в первые часы после инфицирования и от эффективности их работы на данном этапе зависит вероятность развития инфекции, а также тяжесть ее протекания. Поэтому, пока не установлен возбудитель заболевания и нет возможности применять средства специфической терапии, направленные на инфекционный агент, целесообразно поддерживать данную неспецифическую систему противовирусной защиты организма.
В настоящее время десятки фармацевтических компаний производят широкий спектр препаратов, способных эффективно регулировать работу интерферонов.
В качестве подходов используют как введение экзогенных интерферонов (т.е. молекул интерферона, которые были синтезированы в лабораториях и способные заменить собственный интерферон человека), так и индукторов интерферонов – лекарств, стимулирующих прирост собственных защитных белков организма. Подробно о данных способах к терапии инфекционных заболеваний и существующих лекарственных препаратах уже писалось ранее в СМИ.
В качестве еще одного из подходов стала разработка отечественных ученых, которые предложили ни вводить экзогенный интерферон, ни стимулировать продукцию собственного интерферона, а применить лекарство, которое будет усиливать работу собственных интерферонов, когда это нужно (это предотвратит чрезмерную активацию системы интерферонов и ее истощение).
А нужно это только во время инфекции, так как эта система является чрезвычайно чувствительно и «узнает» о попадании вируса в организм практически сразу и мгновенно активирует все имеющиеся резервы.
Достичь задуманного коллективу ученых, под руководством академика РАМН Е.Д. Гольдберга, при участии академиков М.Б. Штарка, В.Н. Ярыгина, профессора О.И. Эпштейна и других известных специалистов, которым удалось создать новую группу лекарственных препаратов на основе особых белков – антител, подвергнутых специальной обработке. Еще в 2005 году данная разработка была удостоена премии правительства РФ. Использование технологически обработанных антител к интерферону-гамма, позволяет изменять конформацию вырабатываемых в организме интерферонов и переводить их в более активную форму. Данные антитела входят в препараты «Анаферон» и «Эргоферон».
Впервые «Анаферон» был зарегистрирован в Российской Федерации в 2001 году, а «Эргоферон», являющийся «усиленной» версией «Анаферона» (за счет дополнительных компонентов) в 2010 году. Следует отметить, что одним из ключевых достоинств данных препаратов является высокий уровень научных исследований.
При этом в исследованиях принимали участие не только российские ученые, но и специалисты из Европы и США.
С точки зрения клинических исследований, эти лекарственные средства смело можно назвать одними из самых изученных среди отечественных противовирусных препаратов: в реестре Минздрава РФ завершенных исследований «Анаферона» — 5, «Эргоферона» — 7. Всего с 2010 года бренд «Анаферон» участвовал в пяти двойных слепых рандомизированных плацебо-контролируемых исследованиях (золотой стандарт клинических исследований), включавших более 2 тыс. пациентов.
Эргоферон участвовал в семи двойных слепых рандомизированных плацебо-контролируемых клинических исследованиях с участием 1700 пациентов.
В ходе исследований подтвердились безопасный профиль и высокая эффективность «Эргоферона» и «Анаферона» при профилактике и лечении ОРВИ и гриппа.
Информация о клинических исследованиях опубликована не только в официальном реестре Минздрава России, а также в международном реестре клинических исследований Национальных институтов здоровья США, что указывает на открытость проводимых исследований, доступность их для любого анализа.
Главное необходимо помнить, что выбор же конкретных лекарственных средств как врачами, так и пациентами, разумеется, должен основываться на их безопасности и эффективности. Применение таких препаратов должно быть в полном в соответствии с инструкцией. Напоминаем — не стоит заниматься самолечением. Не болейте!
Действие Анаферона
Действующее вещество Анаферона активирует все звенья защитных сил организма и увеличивает количество вырабатываемых антител. После приема препарата отмечается стабилизация состояния больного ребенка – снижается температура, исчезают признаки интоксикации организма. Если лекарство было принято в течение 24 часов с момента заражения, то вероятность развития осложнений после ОРВИ снижается до нуля.

Анаферон считается гомеопатическим препаратом с безопасным составом, как для взрослых, так и для детей. Благодаря этому свойству препарат можно совмещать с лекарствами других фармакологических групп.
Можно заменить Анаферон препаратом Виферон или другими аналогами. Однако пациентам редко приходится подбирать препараты с похожим составом из-за невысокой стоимости Анаферона и минимального риска побочных действий. Одной упаковки средства хватает на полный курс терапии. В среднем лечение обходится в 200-250 рублей.
Лекарство требуется принимать по определенной схеме: в первый день терапии нужно принять 7 таблеток, а далее по 1 капсуле трижды в день.
Вопрос о необходимости приема лекарства решается педиатром, так как при нормально функционирующей иммунной системе иммуномодуляторы ребенкуне нужны. Разница между Вифероном и Анафероном прежде всего заключается в показаниях к применению.
Последний препарат назначается:
- при цитомегаловирусном заболевании;
- при иммунодефицитном состоянии;
- при заболеваниях, возбудителями которых является энцефалит или ротовирус;
- для комплексного лечения бактериальных осложнений.
Как видно из показаний, Анаферон больше подходит для терапии болезней, вызванных вирусом. Виферон одинаково часто назначают и при вирусных, и при инфекционных заболеваниях.
Показания к Виферону
Если сравнивать препараты, то можно отметить еще одно существенное отличие: Анаферон выпускается в таблетированной форме, а Виферон в форме ректальных суппозиторий. Свечи используются для лечения детей школьного, подросткового возраста, а также недоношенных и новорожденных малышей.

У Виферона имеются следующие показания к применению:
- ОРВИ и грипп, которые грозят бактериальными осложнениями;
- заражение пневмококковой или менингококковой инфекцией;
- внутриутробное заражение, связанное с герпетической, хламидийной, кандидозной, цитомегаловирусной инфекцией;
- вирусные формы менингита;
- вирусный гепатит, осложненный циррозом печени;
- первичное или хроническое поражение кожных покровов вирусом герпеса.
Какой препарат выбрать? Отличия Анаферона от Виферона заключаются в составе, форме выпуска и показаниях к применению. Гомеопатическое средство не является полноценным аналогом Виферона, так как оба препарата имеют разные действующие компоненты (в первом случае интерферон гамма, а во втором интерферон альфа-2b).
По перечню показаний препарат в виде свечей значительно превышает Анаферон. Суппозитории могут использоваться не только при гриппе и ОРВИ, но и при урологических, гинекологических заболеваниях. Различия заключаются и в противопоказаниях к иммуномодуляторам. Таблетки не назначаются новорожденным детям и женщинам на начальных сроках беременности. Виферон – один из немногих препаратов, который считается безопасным в период вынашивания плода и грудного вскармливания.
При выборе того или иного средства обращают внимание на возраст пациента и особенности заболевания. При легком вирусном заболевании использовать любой иммуномодулятор. При патологиях, осложненных инфекционным процессом, предпочтение отдают Виферону.