Такоцубо кардиомиопатия
Сведения об авторе
© Коллектив авторов, 2016 г УДК 616.12-008
синдром «разбитого сердца» или стресс-индуцированная кардиомиопатия (синдром такоцубо)
ФГКУ «1477 ВМКГ» МО РФ, г. Владивосток, Приморский край.
Синдром «разбитого сердца» (СРС) или стресс-индуцированная кардиомиопатия (синдром апикального баллонирования) является остро возникающую дисфункцию левого желудочка при отсутствии значимых гемодинамических нарушений коронарного русла. Впервые описанное в 1991 году в Японии как кардиомиопатия такоцубо, это заболевание, характеризующее ся транзиторными нарушениями систоличе ской функции левого желудочка, имитирующим клинику острого инфаркта миокарда. В статье описывается случай кардиомиопатии после перенесенного эмоционального стресса у пациента 21 года с клиникой острого инфаркта миокарда, характерными изменения ЭКГ и преходящими нарушениями сократимости левого желудочка. На контрольных ЭКГ и ЭХО-КГ отмечалась быстрая положительная динамика в виде обратного развития ранее выявленных изменений. Рассматриваются этиопатогенетические аспекты СРС.
Ключевые слова: синдром «разбитого сердца» (СРС) или стресс-индуцированная кардиомиопатия, карди-омиопатия такоцубо, клиника, диагностика, лечение.
Синдром разбитого сердца (СРС) в западной литературе известен также под названием стрессовой или стресс-индуцированной кардиомиопатии, она же — обратимая апикальная дискинезия, а также «кардиомиопатия такоцубо» (takotsubo). Впервые синдром был описан в 1991 г. в Японии. Он получил свое название от японского слова <йако^иЬо» — ловушки для осьминогов, в виде горшка с широким основанием и узким горлышком, поскольку при этом синдроме форма левого желудочка становится похожей на нее . По данным литературы, типичные симптомы СРС — это боль за грудиной и затрудненное дыхание, что совершенно идентично симптомам инфаркта миокарда. Оказалось, что среди всех случаев инфаркта миокарда примерно 2% являются стресс-индуцированной кардиомиопатией .
В кардиологии этот синдром стал широко известен с 2006 г. после обсуждения этой темы на Ев-
ропейском конгрессе кардиологов в Барселоне. Тем не менее, многие практические врачи недостаточно осведомлены о его существовании .
Считается, что данное заболевание вызвано сильными эмоциями и характеризуется преходящим нарушением работы левого желудочка сердца, что проявляется изменениями на ЭКГ и в крови (повышением содержания кардиотропных ферментов), свойственными острому инфаркту миокарда. Несмотря на изначально тяжелое состояние пациентов, почти все они полностью выздоравливают в течение нескольких дней или недель без каких-либо последствий. Но в 1% случаев возможны тяжелые осложнения .
Провоцирующим фактором этого заболевания является сильный стресс, физические нагрузки или эмоциональные переживания. У больных возникают сильная боль в области сердца, нарушение дыхания, что обычно диагностируется, как острый инфаркт
миокарда, так как симптомы и соответствующие изменения ЭКГ не вызывают никаких сомнений в отношении этого диагноза.
Загрудинные боли при этом синдроме более длительные, чем при инфаркте миокарда . Патогно-моничным признаком СРС является характерное изменение формы сердца у пациентов. Оно как будто сдавлено невидимым обручем. По данным ЭхоКГ выявляется выбухание верхушки левого желудочка с гиперкинезом его основания. Этот симптом поможет отличить это заболевание от инфаркта миокарда и вывести на путь правильной постановки диагноза. Окончательный диагноз можно верифицировать с помощью коронарографии, которая демонстрирует совершенно здоровые артерии сердца .
Цель сообщения: обзор современных представлений о СРС и обмен клиническим опытом ведения пациентов с данной патологией.
В кардиологическом отделении ФГКУ «1477 ВМКГ» МО РФ за последние три года также наблюдались случаи инфарктов миокарда верхушечной, передней локализации у молодых мужчин (вследствие специфики военного лечебного учреждения), отличающиеся необычным течением, быстрой положительной динамикой, благоприятным прогнозом. Во всех случаях проводился дифференциальный диагноз с СТ. В качестве примера клинических случаев приводим свой опыт диагностики СТ, который был подтвержден в одном из центральных госпиталей МО РФ.
Клинический пример
Пациент А-ев, 1993 г.р., матрос, военнослужащий по контракту, проснулся в 3.00 час 30.01.2014 г. от интенсивных сжимающих болей за грудиной. Накануне принимал участие в спортивных соревнованиях. Самостоятельно обратился в медицинскую роту. После приема анальгетиков боли исчезли. 31.01.2014 г. в 4.00 час вновь развился типичный ангинозный приступ, который продолжался в течение 20-30 минут. В консультативно-диагностической поликлинике пациенту была выполнена ЭКГ, выявлены признаки ишемического повреждения в области верхушки, передней и боковой стенок левого желудочка. Диагностирована ИБС, острый инфаркт миокарда с подъемом сегмента ST в области передней, боковой, нижней стенок левого желудочка от 30.01.14 г. (рис. 1). Пациент был направлен на стационарное лечение в ФГКУ «1477 ВМКГ» МО РФ. При поступлении получены положительная реакция на тропо-нин Т и повышение активности КФК-МВ, на ЭХО-КГ выявлены зоны гипокинеза в области верхушки левого желудочка и прилегающих отделов. В процессе обследования были исключены инфекционно-токсический миокардит, ушиб сердца, подтвержден диагноз инфаркта миокарда (рис. 2).
Рис. 1. ЭКГ пациента А-ва от 31.01.2014 г.: признаки ишемического повреждения в области верхушки, передней и боковой стенок левого желудочка
Рис. 2. Эхо-ЭКГ пациента А-ва от 31.01.2014 г.: зоны гипокинеза в области верхушки левого желудочка и прилегающих отделов
Пациент с 31.01.14 г. по 04.02.14 г. получал терапию по протоколу ОКС в центре анестезиологии и реанимации: нитроглицерин и гепарин инфузома-том, бета-блокаторы, антиагреганты, с 03.02.14 г. назначен амлодипин 5 мг в сутки. На фоне лечения ангинозные боли повторялись до 1-2 раза в первые сутки и снимались наркотическими анальгетиками. Боли сопровождались депрессией ST в отведениях от нижней стенки левого желудочка.
С 03.02.14 г. боли не рецидивировали. Для дальнейшего обследования и лечения был переведен в кардиологическое отделение, где находился с 05.02. по 13.03.14 г. В отделении пациент отмечал удовлетворительное самочувствие, гемодинамика стабилизировалась. При контрольных исследованиях ЭКГ и ЭХО-КГ от 12.03.2014 г. отмечалась быстрая поло-
Рис. 3. ЭКГ пациента А-ва от 12.03.2014 г: отмечается положительная динамика в виде обратного развития ранее выявленных патологических изменений
жительная динамика в виде обратного развития ранее выявленных патологических изменений. Исчезли зоны гипокинеза левого желудочка, фракция выброса (ФВ) увеличилась до 70% (рис. 3).
Таким образом, ангинозные боли у пациента прекратились также быстро, как вышеизложенные патологические изменения показателей функциональных исследований сердца. Диагностические представления о пациенте с учетом результатов наблюдения и обследования изменились. Так, наличие инфаркта миокарда в рамках ИБС практически маловероятно в связи с молодым возрастом пациента и отсутствием факторов риска: дислипидемии, курения, ожирения, артериальной гипертензии. Быстрая динамика нормализации ЭКГ и маркеров некроза миокарда, восстановление нормальной ФВ и исчезновение гипокинеза при инфаркте миокарда не происходят так быстро, тем более, протекающим с подъемом сегмента ST. Зубец Q не сформировался. Особый интерес в плане дифференциального диагноза представляет локализация инфаркта миокарда — верхушка левого желудочка с распространением на переднюю, нижнюю и боковую стенки. Таким образом, если имеет место абортивное течение заболевания, соответствующая локализация поражения миокарда, то это указывает прямо на кардиомиопатию такоцубо.
Прогноз заболевания после завершения первого этапа (риск смерти) в дальнейшем благоприятный с обратным развитием всех симптомов. Значительного ремоделиро-вания сердца не произошло вследствие интенсивного лечения препаратами с различным механизмом действия. Окончательный диагноз: стрессовая кардиомио-патия (синдром такоцубо) был подтвержден позднее, в марте 2014 г. в ФГКУ «3 ЦВКГ имени А.А. Вишневского» МО РФ после проведения коронарографии.
Обсуждение
Транзиторное шарообразное расширение верхушки левого желудочка — разновидность неише-мической кардиомиопатии, при которой развивается внезапное преходящее снижение сократимости миокарда. Сердечная мышца увеличивается и недоста-
точно хорошо качает кровь, в то время как другие показатели остаются относительно нормальными.
Это временное состояние сердца, вызываемое сильными стрессовыми ситуациями, такими как смерть любимого человека. Такое состояние связано, предположительно, с повышением так называемых «гормонов стресса» — катехоламинов (преимущественно адреналина), которые выбрасываются организмом при сильных переживаниях. Уровни катехоламинов повышены у 74% данных больных, при этом у пациентов с СРС они могут быть увеличены в десятки раз .
Пациенты с СРС могут испытывать боли в груди, возможно внезапное развитие острой сердечной недостаточности, тяжелых желудочковых аритмий, вплоть до разрыва стенки желудочка . Боли в груди могут сопровождаться изменениями на ЭКГ, характерными для переднего инфаркта миокарда. При благоприятном исходе начального приступа функция левого желудочка восстанавливается в течение 2 месяцев .
Более 90% случаев этого заболевания возникает у женщин в климактерическом периоде, перенесших недавно тяжелый эмоциональный или физический стресс. Причина этого не ясна, но существует несколько гипотез: большая чувствительность женщин к действию гормонов стресса и проблемы в сосудах и мышце сердца, спровоцированные низким уровнем женских половых гормонов. Симптомы этого заболевания легко контролировать, а сама болезнь обычно проходит в течение нескольких недель. В план обследования пациентов включается коронарография, при которой не выявляется гемодинамически значимых стенозов, способных привести к левожелудочковой дисфункции.
Причины болезни
Точные причины СРС не совсем ясны. Ученые считают, что стресс запускает выработку катехоламинов, которые временно нарушают работу сердца у некоторых людей. Но непонятно, как эти гормоны повреждают сердце, а также, почему одни люди склонны к этому состоянию, а другие нет. Возможно, важную роль в этом процессе играет временное сужение коронарных артерий. СРС всегда предшествует интенсивный физический или эмоциональный стресс.
Вот некоторые возможные триггеры развития синдрома:
— внезапная смерть родного человека;
— насилие в семье или коллективе;
— потеря большого количества денег;
— перенесенная авария, теракт и др.;
— страх большой ответственности;
— приступ бронхиальной астмы;
— тяжелая инфекция;
— хирургическая операция;
— шокирующий медицинский диагноз.
Если при ИБС большая часть сердечных приступов вызвана частичной или полной непрохо-
димостью коронарных артерий, пораженных атеросклерозом, то при синдроме разбитого сердца коронарные артерии не блокируются, а резко суживаются, что нарушает кровоток .
Факторы риска
Синдром разбитого сердца гораздо чаще поражает женщин, чем мужчин. Большая часть больных -это женщины в возрасте старше 50 лет, женщины в постменопаузе .
Патогенез
Вентрикулограмма левого желудочка во время систолы, демонстрирует характерное шарообразное расширение и неподвижность верхушки сердца у пациента с кардиомиопатией такоцубо. Патогенез заболевания не ясен, однако предполагается несколько механизмов:
1. Заворачивающаяся левая передняя нисходящая артерия.
Левая передняя нисходящая артерия кровоснаб-жает переднюю стенку левого желудочка у большинства пациентов. Если эта артерия заворачивается вокруг верхушки сердца, она может отвечать также за кровоснабжение верхушки и нижней стенки сердца. Некоторые исследователи отмечали корреляцию между СРС и данным типом расположения левой передней нисходящей артерии .
2. Транзиторный вазоспазм.
Первые исследователи СРС предполагали, что множественные одновременные спазмы коронарных артерий способны вызывать снижение кровотока, достаточные для развития преходящего сбоя в работе миокарда. Другие исследования показали, что вазоспазм значительно менее распространен, чем предполагалось первоначально .
3. Микрососудистая дисфункция.
Эта теория предполагает, что развивается дисфункция мелких ветвей коронарных артерий, которые невозможно визуализировать посредством коронарографии. Изменения могут проявляться как микрососудистым вазоспазмом, так, возможно, и микроангиопатией, подобной наблюдаемой при сахарном диабете. В этих условиях мелкие артерии неспособны обеспечить адекватную оксигенацию миокарда .
Вероятно, в развитии стрессовой кардиомиопатии имеют значение многие факторы — вазоспазм, недостаточность микроциркуляции и патологический катехоловый ответ. В большинстве случаев синдром развивался после эмоционального стресса или, в иных случаях, после предшествующего физического стресса (астматического статуса или внезапного заболевания). Примерно у одной трети пациентов стрессовый фактор отсутствовал. СРС имеет несколько большую частоту в зимнее время. Это может быть обусловлено двумя возможными патофизиологическими причинами: спазмом мелких ветвей
коронарных артерий, преобладающим в холодную погоду, и вирусными инфекциями, которые чаще наблюдаются в зимний сезон .
Диагностика СРС
Диагностика СРС основывается на клинической картине, электрокардиографии, данных ЭхоКГ и результатах коронарографии. Клиническая картина (за-грудинные боли, диспноэ) затрудняют диагностику. Но сбор анамнеза позволяет заподозрить синдром разбитого сердца — отсутствие в анамнезе заболеваний сердца до стрессовой ситуации, которая послужила толчком. ЭХО-КГ в острую стадию стрессовой кардиомиопатии демонстрирует дилятацию левого желудочка, преходящую дисфункцию подвижности верхушки (выбухание) сердца, обратимую апикальную дискинезию.
ЭКГ изменения часто ошибочно трактуются как проявление переднего инфаркта миокарда: элевация ST-сегмента, инверсией T-зубца или удлинением QT-интервала. Регистрируется незначительный подъем кардиоселективных ферментов. Уточняет диагноз ко-ронарография, которая демонстрирует совершенно здоровые коронарные артерии. Отсутствуют гемоди-намически значимые стенозы артерий сердца, способные привести к левожелудочковой дисфункции .
Содержание в сыворотке крови кардиоспецифич-ных маркеров (СК-МВ, тропонинов I и T) увеличено в разной степени у 90% пациентов с СРС . При этом характерно отсутствие корреляции степени повышения с объёмом повреждённого миокарда и подъёмом сегмента ST. Считается, что при уровне тропонина T больше чем 6 нг/мл и тропонина I больше чем 15 нг/мл более вероятна ИБС, независимо от других полученных данных . Была обнаружена прямая корреляционная связь между снижением ФВ и содержанием тропонина T .
В ряде исследований при оценке уровней нора-дреналина, адреналина и допамина в плазме крови при СРС было обнаружено, что почти у 75% пациентов в острой стадии их содержание было существенно выше, чем при ИМ .
Кроме того, СРС характеризуется достоверно более высоким увеличением мозгового натрийуре-тического пептида (BNP) . У большинства пациентов с КТ отмечается повышение содержания в плазме крови BNP, в десять и более раз превышающее референтные значения , что является маркёром увеличенного конечного диастолического давления и диастолической дисфункции и предиктором неблагоприятного прогноза .
Патоморфология
Морфологическая картина при СРС представлена фокальным миоцитолизом. Ассоциированных микробиологических агентов не выявляется. В некоторых случаях обнаруживается инфильтрация малыми моно-
нуклеарами. Эти патологические находки позволяют предположить, что стрессовая кардиомиопатия является вариантом воспалительного заболевания сердца, а не коронарной патологии. Также имеются сообщения о гистологическом повреждении миокарда без ИБС .
Лечение
При стресс-индуцированной кардиомиопатии необходима неотложная госпитализация больного в отделение интенсивной кардиологии. При этом заболевании возникает сердечная недостаточность, которая бесследно исчезает через несколько дней. В современной литературе нет четких стандартов для лечения этого синдрома. Терапия кардиомиопатии такоцубо в большинстве случаев поддерживающая. У пациентов с артериальной гипотензией используется поддержка инотропными препаратами или внутриаортальная контрпульсация. Стандартно назначается ацетилсалициловая кислота, ингибиторы АПФ или антагонисты рецепторов ангиотензина-I с целью снижения АД. А также ß-адреноблокаторы для контроля ЧСС и нитраты для устранения спазма коронарных артерий. У многих пациентов функция левого желудочка восстанавливается в течение 2 месяцев .
Прогноз заболевания
Несмотря на грозные исходные клинические проявления у некоторых больных, большинство пациентов переживают начальный приступ с очень низким уровнем больничной летальности и осложнений. После перенесенной острой стадии заболевания пациентов ожидает благоприятный исход с хорошим долгосрочным прогнозом. Даже при тяжелой систолической дисфункции в начале заболевания, сократительная способность миокарда начинает восстанавливаться уже в первые сутки и нормализуется в течение нескольких месяцев. В очень редких случаях могут быть тяжелые осложнения: мерцательная аритмия в 4,2%, кардиоген-ный шок в 1,5% случаев. Смертность составляет лишь 1,1%. В 5% случаев возникает рецидив заболевания, вероятно, провоцируемый ассоциированным пусковым механизмом .
Профилактика болезни
Нет никаких надежных методов профилактики. Тем не менее, многие американские врачи рекомендуют длительный прием b-адреноблокаторов (мето-пролол, атенолол). Важна помощь психолога в профилактике стрессов.
Учитывая особенности обслуживаемого нами воинского контингента — преимущественно лиц мужского пола, необходимо помнить о данном заболевании в случае передне-верхушечного инфаркта миокарда у молодых людей.
Выводы
Сравнительно недавно открытое заболевание, СРС, представляет собой особый вариант кардиомиопатии, характеризующейся обратимой дисфункцией левого желудочка. Она имитирует острый коронарный синдром и при ней повышается уровень кардиомаркеров. Основным триггером синдрома является выраженный физический и эмоциональный стресс, относительно часто встречается у пожилых женщин в постменопаузе. Существующие в настоящее время патофизиологические теории в разной степени объясняют механизм возникновения заболевания, но ни одна из них не является окончательной, объясняющей все клинические проявления. Однако, независимо от причины, пациенты с классической кардиомиопатией, развившейся после эпизода острого стресса, заслуживают особого внимания. Эта обширная функциональная аномалия сердечной стенки потенциально может иметь грозные осложнения и связанные с ними последствия.
ЛИТЕРАТУРА:
1. Гиляревский С Р. Кардиомиопатия такоцубо. Подходы к диагностике и лечению. — М.: МЕДпресс-информ, 2013.
4. Connelly K.A., MacIsaac A.I., Jelinek V.M. Stress, myocardial infarction and the «tako-tsubo» phenomenon. Heart. 2004; 90: 52.
9. Kawai S., Kitabatake A., Tomoike H. Guidelines for diagnosis of takotsubo (ampulla) cardiomyopathy. Circ. J. 2007; 71(6): 990-2.
13. Sealove B.A., Tiyyagura S., Fuster V. Takotsubo cardiomyopathy. J.Gen.Intern.Med. 2008; 23(11): 1904-8.
FGKU «VMKG 1477» Defense of the Russian Federation, Vladivostok, Primorsky region, Russia.
Сведения об авторах
Определение
Стресс-индуцированная кардиомиопатия, также называемая синдром преходящей дисфункции левого желудочка или Takotsubo-кардиомиопатия, становится все более известной, обычно характеризуется транзиторной систолической дисфункцией и обширной акинезией апикальных и / или средних сегментов левого желудочка, жалобами имитирующие острый коронарный синдром, но при отсутствии обструкции коронарных артерии , сопровождаются изменениями на ЭКГ, а также ограниченным выбросом сердечных маркеров, не соответствующих этой степени акинезией.
Около 20 лет назад этот синдром описывался только у японских пациентов. Однако во всем мире на данный момент по статистике 2% из 300000 сердечных приступов приходится на это заболевание. Это говорит о большей информированности врачей, улучшении диагностики и установления четких критериев для постановки диагноза. Следует ожидать увеличения частоты своевременной диагностики такоцубо-кардиомиопатии при условии доступности неотложной коронароангиографии в большинстве кардиологических центров в первые 24 часа, как того и требуют современные рекомендации по оказанию неотложной помощи больным с острым коронарным синдромом .
Термин «такоцубо» (tako-tsubo) в переводе с японского языка означает приспособление для ловли осьминогов – керамический горшок с круглым основанием и узким горлышком. Именно такую форму у больных при эхокардиографии приобретает левый желудочек (ЛЖ) в систолу, что объясняется отсутствием сокращения его верхушки с одновременным избыточным сокращением базальных отделов .
Патогенез
Патогенетические механизмы включают в себя избыток катехоламинов спазм коронарных артерии, и микрососудистую дисфункцию .
Потенциальная роль разрыва холестериновой бляшки и тромбоза со спонтанным тромболизисом не были установлены. Однако результаты внутрисосудистого ультразвукового исследования (ВСУЗИ) показали доказательство разрыва бляшки в середине левой передней нисходящей коронарной артерии в 5 из 5 пациентов с диагнозом стресс-индуцированной кардиомиопатии , но другая серия ВСУЗИ не нашла никаких доказательств относительно этой гипотезы .
Связь развития стрессовой кардиомиопатии с физическим или эмоциональным стрессом , показывают, что это расстройство может быть вызвано диффузным действием катехоламинов вызванным микрососудистым спазмом или дисфункцией, путем прямого токсического действия катехоламинов . У некоторых пациентов с индуцированной стрессом кардиомиопатией, единственным очевидным стрессом является воздействие препаратов катехоламинов или бета-агонистов в обычных клинических дозах .
Возможность патогенной роли катехоламинов выявлена в ряде исследований определения в плазме катехоламинов . Объединяя результаты из этих серий, плазменные уровни норадреналина были повышены в 74 % и составили следующие концентрации: эпинефрин-1264 пг/мл против нормальной концентрации 376 пг / мл; норэпинефрин-2284 пг/мл против 1100 пг / мл . Повышение уровня катехоламинов и обратимые изменения левого желудочка наблюдались также в крысиной модели, вызванной стрессом . Однако, высокий уровень катехоламинов в крови не является повсеместно встречаемым у обследуемых пациентов и некоторые исследования показали нормальный уровень .
Дальнейшая поддержка гипотезы действия катехоламинов обеспечивается наблюдениями подобной обратимой кардиомиопатии с глобальной или очаговой дисфункцией у пациентов с феохромоцитомой и в условиях острого повреждения головного мозга, которые также постулируются связанными с действием катехоламинов . По данным эндомиокардиальной биопсии в серии из восьми пациентов в период дисфункции левого желудочка обнаружены гистологические признаки катехоламиновой токсичности — отсутствие признаков миокардита , обнаружение интерстициального фиброза , внутриклеточное накопление гликогена, множество вакуолей, дезорганизованность цитоскелета миокардиоцитов, увеличение белка внеклеточного матрикса . Эти изменения нивелировались почти полностью после функционального восстановления. Предположительно, что наибольший эффект в апикальной части миокарда может быть связан с более высокой плотностью бета-адренорецепторов в этом месте .
Эпидемиология
Стресс-индуцированного кардиомиопатия гораздо чаще встречается у женщин, чем у мужчин. В обзоре десяти проспективных серий, женщины составляли от 80 до 100 % случаев, со средним возрастным интервалом от 61 до 76 лет . У женщин > 55 лет риск развития заболевания был в 4,8 раза выше, по сравнению с женщинами <55 лет, особенно у женщин в постменопаузальном периоде, выступающим как стрессовый триггерный фактор и меняющий гормональный фон . Исследователи подозревают, что пожилые женщины более уязвимы из-за снижения уровня эстрогена после менопаузы. Кардиомиопатия диагностируется и у детей. Клинические проявления и данные ЭКГ у подростков были сходные с острым коронарным синдромом. Это объясняется тем, что дифференцировка надпочечников продолжается после рождения ребенка вплоть до 14—16 лет, что и объясняет некорректный ответ на стресс .
Факторы риска
К факторам риска, которые обычно связаны с развитием стрессовой кардиомиопатии следует отнести курение, злоупотребление алкоголем, тревожные состояния и гиперлипидемия. Провоцирующими факторами могут выступать: физический стресс, внезапное падение артериального давления, тяжелая болезнь, операция или медицинская процедура (например, сердечный стресс-тест), сильная боль, насилие в семье, приступ астмы, получение плохих новостей (например, диагностика рака), несчастный случай, неожиданная потеря или болезнь близкого родственника, финансовый убыток, сильный страх, публичные выступления .
Клиника
Наиболее распространенным симптомами являются острая загрудинная боль (58,8% случаев), а затем одышка (30% случаев), обмороки, тахикардия. Острыми осложнениями стресс-индуцированной кардиомиопатии являются остановка сердца, тахиаритмии (включая желудочковую тахикардию и фибрилляцию желудочков), брадиаритмии. Стресс-индуцированный гиперкинез левого желудочка может способствовать развитию шока и серьезной митральной регургитации , верхушечное тромбообразование и инсульт . Вероятность развития острой сердечной недостаточности возможно предсказать на основе наличия или отсутствия следующих трех переменных : возраст > 70 лет, наличие физического стрессора и снижение фракции выброса левого желудочка ( ФВ ЛЖ ) < 40 процентов . При обследовании 118 больных, вероятность развития острой сердечной недостаточности был < 10 процентов при отсутствии этих факторов риска.
Диагностика
Диагностическими критериями клиники Мейо являются :
- Переходные гипокинезия, акинезия или дискинезия левого желудочка середины сегментов с или без апикального участия.
- Региональных аномалий движения стенки обычно выходят за рамки одного эпикардиальной коронарного распределения.
- Наличие стрессовых триггеров часто, но не всегда.
- Отсутствие обструкции коронарных артерий или ангиографических признаков острого разрыва бляшки.
- Электрокардиографические аномалии (либо изменение высоты ST- сегмента и / или инверсия зубца Т).
- Скромные высоты сердечного тропонина и креатинфостокиназы.
- Отсутствие феохромоцитомы или миокардита.
- Фракция выброса левого желудочка (ФВ ЛЖ ) < 40 процентов.
Электрокардиографические проявления имитируют острый коронарный синдром. Характерен инфарктоподобный подъем сегмента ST, наиболее распространенной в передних грудных отведениях ; диффузная инверсии зубца Т с продлением интервала QT , аномальные волны Q , неспецифические нарушения. Восстановление ЭКГ происходит на 2-3 неделе болезни.
Наиболее специфичные изменения при ЭХО-кг и контрастной вентрикулографии. Характерен акинез или дискинез верхушки и средней части ЛЖ с гиперконтрактильностью основания и обструкцией выходного тракта ЛЖ. При этом форма ЛЖ напоминает приспособление для ловли осьминогов. Общая систолическая функция снижается, а средняя ФВ ЛЖ варьируется в диапазоне от 20 до 49 процентов .
Ангиография является ценным методом диагностики. Принципиальное отличие кардиомиопатии токацубо от острого коронарного синдрома – отсутствие гемодинамически значимого стеноза коронарных артерий.
МРТ с гадолинием помогает в дифференциальном диагнозе с такими заболеваниями как инфаркт миокарда и миокардит. Гадолиний не накапливается при стресс-индуцированной кардиомиопатии, в отличие от инфаркта миокарда, в котором интенсивное (т.е. > 5 стандартных отклонений выше средней интенсивности сигнала дистанционного миокарда) субэндокардиально или трансмурально. При миокардите характерно неоднородное накопление гадолиния. МРТ может также дать определение тромбов в левом или правом желудочке, которые не могут быть обнаружены с помощью ЭХО-кг .
Повышение сердечных сывороточных маркеров контрастирует с часто тяжелыми нарушениями гемодинамики. Распространенность повышения креатинкиназы-МВ и / или тропонина у пациентов было в 89,3% случаев, в 10,7% показало нормальный уровень этих сердечных ферментов. Средняя максимальная вариабельность креатинкиназы-MB и рост тропонина были 27,4 мкг/л (норма 5.2-115.7 мкг / л) и 18,7 мкг / л (норма 2.0-97.6 мкг/л), соответственно .
Лечение
До настоящего времени отсутствуют формальные рекомендации по лечению больных с СКМП. Считается, что в острой фазе заболевания показано применение транквилизаторов, если развитию синдрома предшествовал эмоциональный стресс, а также устранение других возможных провоцирующих факторов, например боли. Назначаются ингибиторы АПФ, бетаадреноблокаторы, антикоагулянты, диуретики, антагонисты кальция. Кроме того, в таких случаях целесообразно выполнение внутриаортальной баллонной контрпульсации. При динамической обструкции выходного тракта ЛЖ противопоказано использование препаратов положительного инотропного действия. Продолжительность приема антикоагулянтов варьируются в зависимости от скорости восстановления функции сердца. На фоне поддерживающей терапии всегда происходит спонтанное выздоровление в течение 2 месяцев. В 5% случаев возникает рецидив заболевания, вероятно, провоцируемый ассоциированным пусковым механизмом.
Заключение
Takotsubo кардиомиопатия представляет собой новый вариант кардиомиопатии, который стал диагностироваться в последние годы. Основным пусковым фактором заболевания является выраженный физический и эмоциональный стресс, относительно часто встречается у пожилых женщин. Патогенетические механизмы обуславливаются токсическим действием катехоламинов, поэтому сочетании α-и β-адреноблокаторов, добавление эстрогенов в терапию у женщин в постменопаузе может защитить от его развития или смягчить клинические проявления. Этот вид кардиомиопатии следует считать возможной причиной внезапной сердечной смерти в результате аритмии, в том числе у лиц без явных сердечных заболеваний. Чтобы лучше понять патогенетические механизмы, разработать рациональную систему профилактики и схем лечения, созданы регистры.
Наиболее значимые из них:
- многонациональное, проспективное и ретроспективное, обсервационное исследование пациентов с Takotsubo кардиомиопатией — международный Takotsubo регистр Цюрихского университета (InterTAK Registry) ;
- многоцентровый регистр сети отделений кардиореанимации г.Токио ;
- INTrial является надежной, проверенной и одобренной системой для онлайн ввода данных, проверки данных и управления данными для клинических испытаний, в том числе по кардиомиопатии takotsubo .
Библиографическое описание:
В 1990 г. японский кардиолог Sato H. и соавт. обнаружили, что у 22 пожилых женщин с, казалось бы, тяжёлой картиной острого коронарного синдрома (ОКС), по данным коронарографии не выявляется столь тяжёлых поражений. Более того, выраженное снижение функции левого желудочка, которое отмечалось в момент госпитализации, нивелировало и состояние больных восстанавливалось быстрее, чем при ОКС. Стало понятно, что речь идёт о ранее не изученном заболевании и в МКБ-10 появилась новая нозологическая форма — синдром такоцубо. В статье описана типичная клиническая картина данного синдрома, приведены наиболее современные диагностические критерии и методы лечения.
Ключевые слова: острый коронарный синдром, такоцубо, синдром «разбитого сердца», коронарография, кардиомиопатия.
Синдром такоцубо — транзиторное баллоноподобное расширение средней части верхушки сердца, сопровождающееся одновременной гиперкинезией базальных сегментов левого желудочка при отсутствии гемодинамически значимого стеноза венечных артерий (I51.81) .
Другие названия синдрома: стрессовая кардиомиопатия, кардиомиопатия такоцубо, синдром апикального баллонирования, «синдром разбитого сердца», «синдром счастливого сердца».
Своим названием синдром обязан характерным изменением формы левого желудочка на эхокардиографии, возникающим за счёт акинезии/дискинезии и напоминающим японский глиняный сосуд — такоцубо, представляющий собой ловушку для осьминогов («тако» — осьминог, «цубо» — чаша). Ловушка-такоцубо — это 15-сантиметровый сосуд, который используется японскими рыбаками для ловли осьминогов на дне моря, в который они забираются как в жилище и оставляют снаружи только щупальца. Через некоторое время рыбаки вытаскивают ловушки за привязанную к ним верёвку вместе с осьминогами. Интересен тот факт, что приспособление такоцубо используется только рыбаками Хиросимы.
Эпидемиология. Таким образом, синдром впервые описан в Японии в 1990 г. В США первый случай описан в 1998 г. Sharkey S. W. и соавт. Вскоре после первого описания стало очевидным, что заболевание встречается в разных регионах мира. В Болгарии о первых случаях данного заболевания было доложено в марте 2006 г. на эхокардиографическом курсе Европейского кардиологического общества в Софии, а в последующем — и на Европейском конгрессе по эхокардиографии. Сегодня случаи синдрома такоцубо описаны авторами России, Франции, Бельгии, Мексики, Австралии, Испании, Южной Кореи, Китая, Бразилии, Германии, Израиля, Южной Африки, Турции и Исландии.
На сегодняшний день в Международном регистре синдрома такоцубо зарегистрировано 1750 пациентов.
При этом 90 % больных — женщины после менопаузы в возрасте 66–67 лет, около 10 % — мужчины; кроме того, описаны случаи заболевания даже у детей.
Необходимо отметить, что синдром такоцубо выявляется примерно у 1–2 % среди всех госпитализированных с ОКС.
Анатомические варианты синдрома такоцубо:
- Типичный (верхушечный) вариант (75–80 %) — вовлечение апикальных и средних сегментов левого желудочка, при этом зоны нарушения кинетики миокарда не соответствуют бассейну кровоснабжения какой-либо отдельной коронарной артерии;
- Атипичный вариант («щадящий верхушку вариант») (10–15 %) — верхушка левого желудочка не затронута, а вовлекаются только его средние сегменты;
- Базальный (инвертированный) вариант — 5 %;
- Поражение двух желудочков — менее 0,5 %.
Типичный и атипичный варианты синдрома имеют схожую клиническую картину. Остаётся неясным, почему у некоторых пациентов верхушка левого желудочка не поражается.
Этиология. В первое время считалось, что ведущий этиологический фактор — эмоциональный. Однако в ходе последних наблюдений выяснилось, что более часто провоцирующими факторами являются физические.
Таблица 1
Этиологические факторы синдрома такоцубо
|
Физические факторы — 36 % |
Эмоциональные факторы — 27,7 % |
|
тяжёлая физическая работа; внезапное падение АД; тяжёлая болезнь; хирургическое вмешательство или медицинская процедура; сильная боль; приступ бронхиальной астмы; проведение химиотерапии; инсульт др. |
неожиданная потеря или болезнь близкого человека; получение плохих новостей (например, диагностика рака); несчастный случай; финансовый убыток; потеря работы; семейные конфликты; сильный страх; публичные выступления и др. |
В 28,5 % этиологический фактор остается неизвестным.
Среди 1750 пациентов учёные выделили 485 человек, которые смогли абсолютно точно сказать, какое именно событие стало «спусковым крючком» для синдрома такоцубо. Из этих 485 человек у 465 (26,5 %) приступ случился после печального или трагического события (смерть родственника, посещение похорон, болезнь или смерть любимого человека), вследствие чего синдром получил название «синдром разбитого сердца». Один случай произошёл с человеком, страдавшим от ожирения, после того как он застрял в трубе во время отдыха в аквапарке.
При этом выяснилось, что у 20 (4,1 %) человек болезнь была спровоцирована счастливым событием: празднованием дня рождения, свадьбы, победой любимой спортивной команды, рождением внука. По аналогии с «разбитым сердцем» врачи назвали новое явление «синдромом счастливого сердца».
Таким образом, положительные эмоции тоже могут привести к развитию синдрома такоцубо, т. к. они приводят к ответной реакции вегетативной нервной системы в той же степени, как и отрицательные, что обусловливает изменение ЧСС, ОПСС и уровня АД. Имеются данные о том, что частота развития осложнений сердечно-сосудистых заболеваний может быть на 27 % выше в день рождения по сравнению с другими днями года. Поразителен тот факт, что положительные эмоции вызывают чаще изменения атипичной локализации — поражение средних сегментов (рис. 1).
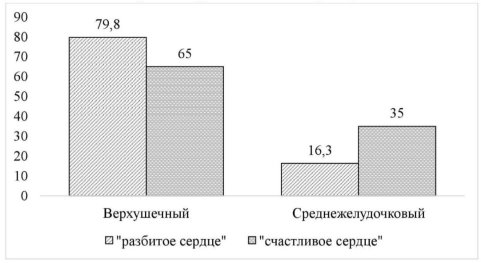
Рис. 1. Анатомические варианты синдрома такоцубо при различных этиологических факторах
Патогенез. Патогенетические механизмы развития синдрома такоцубо сложны и складываются из 3-х составляющих:
- Избыток катехоламинов;
- Спазм коронарных артерий;
- Микрососудистая дисфункция.
Выделение катехоламинов, по всей видимости, играет центральную роль в патофизиологии синдрома такоцубо как пусковой механизм при внезапном стрессе; на момент клинических проявлений отмечаются признаки симпатической активации.
Имеется 2 физиологических момента, требующих рассмотрения.
Во-первых, это когнитивные центры мозга и гипоталамо-гипофизарно-надпочечниковая (ГГН) ось и какое количество адреналина и норадреналина высвобождается в ответ на тот или иной стресс (т. е. «усиление» ГГН-оси).
Во-вторых, реакция сердечно-сосудистой и симпатической нервной системы на внезапную симпатическую активацию и резкое повышение уровня циркулирующих катехоламинов.
Сывороточные уровни катехоламинов на момент клинических проявлений синдрома такоцубо значительно выше, чем в покое, у одного и того же или у сопоставимых пациентов с острым инфарктом миокарда, что указывает на наличие потенциальной возможности избыточного усиления ГГН-оси и высвобождения адреналина.
Возможность патогенной роли катехоламинов выявлена в ряде исследований определения в плазме катехоламинов. Объединяя результаты из этих серий, плазменные уровни норадреналина были повышены в 74 % и составили следующие концентрации: адреналин — 1264 пг/мл (N — 376 пг/мл), норадреналин — 2284 пг/мл (N — 1100 пг/мл). Повышение уровня катехоламинов и обратимые изменения левого желудочка наблюдались также в крысиной модели, вызванной стрессом. Однако, высокий уровень катехоламинов в крови не является повсеместно встречаемым у обследуемых пациентов и некоторые исследования показали нормальный уровень .
Сообщается о ятрогенном синдроме такоцубо после введения симпатомиметических препаратов (например, добутамина при стресс-ЭхоКГ).
У некоторых пациентов с кардиомиопатией такоцубо, единственным очевидным стрессом является воздействие препаратов катехоламинов или β‐агонистов в обычных клинических дозах.
Эти патофизиологические гипотезы не могут быть взаимоисключающими, поскольку вся сердечно-сосудистая система подвергается воздействию того же самого катехоламинового шторма. Многие из этих гипотез до сих пор изучаются, поскольку в настоящее время нет доказанных патофизиологических механизмов, объясняющих синдром такоцубо.
Дальнейшая поддержка гипотезы действия катехоламинов обеспечивается наблюдениями подобной обратимой кардиомиопатии с глобальной или очаговой дисфункцией у пациентов с феохромоцитомой и в условиях острого повреждения головного мозга, которые также постулируются связанными с действием катехоламинов. По данным эндомиокардиальной биопсии в серии из 8 пациентов в период дисфункции левого желудочка обнаружены гистологические признаки катехоламиновой токсичности: отсутствие признаков миокардита, обнаружение интерстициального фиброза, внутриклеточное накопление гликогена, множество вакуолей, дезорганизованность цитоскелета миокардиоцитов, увеличение белка внеклеточного матрикса. Эти изменения нивелировались почти полностью после функционального восстановления. Предположительно, что наибольший эффект в апикальной части миокарда может быть связан с более высокой плотностью β‐адренорецепторов в этом месте.
Генетическая предрасположенность. Стрессовые пусковые механизмы синдрома такоцубо указывают на то, что его патофизиология сильно связана с факторами окружающей среды. Тем не менее можно предположить, что у некоторых людей существует генетическая предрасположенность к стресс-индуцированному синдрому такоцубо. Хотя данный синдром не рассматривается в качестве первичной генетической кардиомиопатии, в ряде исследований обнаружена возможность существования генетических факторов риска. Наличие генетической предрасположенности было предположено на основе описания нескольких семейных случаев синдрома такоцубо. Однако в этих исследованиях задействовано относительно небольшое число пациентов. Решение этих противоречий потребует высокого качества фенотипирования, идентификации генов-кандидатов, а также обмена данными высокого качества о большом количестве больных с синдромом такоцубо .
Несмотря на подробный анамнез, в 15 % из случаев стрессовый фактор выявить невозможно; остаётся неясным, почему в одних случаях стресс может привести к развитию кардиомиопатии такоцубо, а в других — при наличии даже более сильного стресса данное заболевание не возникает.
Клинические формы. Выделяют 2 клинических подтипа синдрома такоцубо:
Первичный синдром такоцубо — основной причиной обращения за медицинской помощью являются острые сердечные симптомы; пациенты доставляются бригадой скорой помощи или госпитализируются по направлению лечащего врача. Больные этой категории могут как иметь чётко идентифицируемые стрессовые триггеры (часто эмоциональные), так и не иметь их.
Вторичный синдром такоцубо — возникает у пациентов, госпитализированных по поводу другого медицинского состояния (хирургического, анестезиологического, акушерского или психиатрического). У этих больных внезапная активация симпатической нервной системы или повышение уровня катехоламинов приводят к возникновению острого синдрома такоцубо как осложнения первичного состояния или его лечения. При лечении необходимо сосредоточиться не только на собственно синдроме такоцубо и его сердечно-сосудистых осложнениях, но и на первичном заболевании, вызвавшем синдром.
Клиническая картина
Клинический пример
Больная А., 64 года
‒ Жгучие боли за грудиной, без иррадиации, волнообразные, в течение дня;
‒ Боли возникли остро после эмоционального стресса (выступление в суде);
‒ Одышка инспираторного характера, возникающая при умеренной физической нагрузке;
‒ Вызвана «Скорая помощь», зафиксировано АД 80/50 мм.рт.ст.;
‒ Госпитализирована в ЦРБ по месту жительства с подозрением на острый инфаркт миокарда;
‒ Болевой синдром был купирован еще на догоспитальном этапе, более не рецидивировал.
Объективное исследование при поступлении:состояние средней степени тяжести, положение активное, сознание ясное, акроцианоз, периферических отеков нет, пульс 76 в минуту, ритмичный, резкое ослабление I тона над верхушкой сердца, грубый систолический шум по левому краю грудины, над лёгкими с обеих сторон выслушивается большое количество влажных мелкопузырчатых хрипов, живот мягкий, безболезненный; ОАК и ОАМ без особенностей.
На ЭКГ: подъём сегмента ST в I, aVL, V2-V6 отведениях, патологические зубцы Q в этих же отведениях (рис. 2).
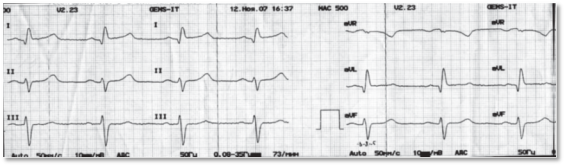
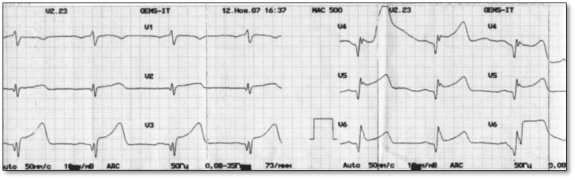
Рис. 2. ЭКГ у больной с синдромом такоцубо в первые часы от начала заболевания
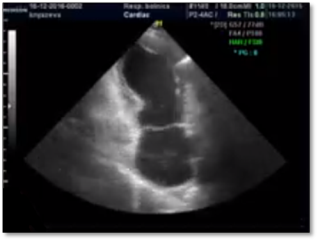
Рис. 3. Эхо-КГ у больной с синдромом такоцубо в первые часы от начала заболевания
Пациентке установлен предварительный диагноз: ИБС. Q-инфаркт миокарда c подъемом ST в переднебоковой стенке. Вечером тоже же дня был выполнен тромболизис капельно в/в 1500000 ЕД стрептокиназы (без осложнений).
В дальнейшем лечение пациентки проводилось по программе ОКС. Между тем, сократимость ЛЖ у больной стала быстро улучшаться, и через 4 дня нарушений локальной кинетики уже не выявляли.
На ЭКГ стала быстро нарастать амплитуда зубца R в отведениях V2-V4 одновременно с исчезновением патологического зубца Q в I, aVL, V2-V4 отведениях и формированием широкого и глубокого отрицательного зубца Т в этих же отведениях.
На Эхо-КГ: полости не расширены, нарушения локальной сократимости нет, ФВ ЛЖ — 69 %, СД в ЛА — 35 мм.рт.ст.
Отсутствовала динамика кардиоспецифических ферментов.
Таким образом, у пациентки с клиникой острой стадии инфаркта миокарда и поздним началом тромболизиса (через 5,5 ч от начала ангинозного приступа) не только произошла нормализация тяжёлых нарушений сократимости ЛЖ, но и зарегистрировано исчезновение (!) уже сформированного патологического зубца Q на ЭКГ при отсутствии значимой динамики кардиоспецифических ферментов. Возникло подозрение на синдром такоцубо и была выполнена коронарография.
Данные коронарографии: правый тип кровоснабжения; ствол проходим, трифуркация ствола, передняя межжелудочковая артерия, интермедиальная артерия, огибающая артерия, правая коронарная артерия — без признаков стенозирования; признаков тромбоза, спонтанных диссекций и осложнённых стенозов нет.
В течение года наблюдения самочувствие пациентки оставалось нормальным. Полное восстановление исходной картины ЭКГ произошло только через 5 месяцев после выписки из стационара.
Диагностика. Диагноз синдрома такоцубо ставится на основании:
‒ клинической картины,
‒ данных ЭКГ,
‒ данных Эхо-КГ,
‒ данных коронарографии.
Таблица 2
Диагностические критерии синдрома такоцубо, предложенные экспертами клиники Мейо
|
Преходящая гипо-, а- или дискинезия средних сегментов ЛЖ как при вовлечении верхушки, так и в его отсутствие; нарушение локальной сократимости миокарда, распространённость которых превышает зону, кровоснабжаемую какой-либо одной коронарной артерией; часто наличие провоцирующего стрессового фактора |
|
|
Отсутствие стенозирующего поражения коронарных артерий или ангиографических признаков острого разрыва атеросклеротической бляшки |
|
|
Впервые резвившиеся патологические изменения ЭКГ (либо подъём сегмента ST, либо инверсия зубца Т) или умеренное повышение уровня кардиоспецифического тропонина в крови |
|
|
Отсутствие феохромоцитомы и миокардита |
Диагностические критерии клиники Мейо ограничены. Здесь самым главным считается второй пункт — отсутствие поражения коронарных артерий. На сегодняшний день данный критерий не совсем правомочен, поскольку описаны случаи развития синдрома такоцубо как ответная реакция на инфаркт миокарда.
Таблица 3
Диагностические критерии синдрома такоцубо Ассоциации специалистов по сердечной недостаточности (2016)
|
Транзиторные патологические движения миокарда стенок ПЖ или ЛЖ, которым часто (но не всегда) предшествует стрессовый триггерный механизм (эмоциональный или физический) |
|
|
Транзиторные патологические движения миокарда обычно не соответствуют зоне кровоснабжения одной коронарной артерии |
|
|
Отсутствие обструкции коронарной артерии, свидетельств отрыва атеросклеротической бляшки, формирования тромба либо прочих патологических состояний, которые могли бы объяснить имеющуюся дисфункцию ЛЖ (гипертрофическая кардиомиопатия, вирусный миокардит) |
|
|
Появление новых обратимых ЭКГ-изменений ( или ↓ сегмента ST от изолинии, БЛНПГ, инверсия зубца T и/или удлинение интервала QT) во время острой фазы (3 мес) |
|
|
Значительное повышение уровня натрийуретического пептида (мозгового натрийуретического пептида или его N-терминального фрагмента ) во время острой фазы заболевания |
|
|
Незначительное повышение уровня сердечного тропонина (т. е. несоответствие между уровнем тропонина и имеющейся кардиальной дисфункцией) |
|
|
Восстановление систолической функции желудочка за 3–6 мес |
Таблица 4
Критерии стратификации риска убольных ссиндромом такоцубо
|
Фактор риска |
Высокий риск |
Низкий риск |
|
Возраст |
≥ 75 лет |
˂ 70 лет |
|
Уровень САД |
≥ 110 мм.рт.ст. |
|
|
Отек легких |
Диагностируется |
Отсутствует |
|
Необъяснимое развитие обморока, желудочковая тахикардия или фибрилляция желудочков |
Диагностируется |
Отсутствует |
|
ФВ ЛЖ |
≥ 45 % |
|
|
Обструкция ВТ ЛЖ |
≥ 40 мм.рт.ст. |
Отсутствует или |
|
Митральная регургитация |
Диагностируется |
Отсутствует |
|
Тромб в области верхушки |
Диагностируется |
Отсутствует |
|
Дефект МЖП или разрыв стенки ЛЖ |
Диагностируется |
Отсутствует |
Лечение. До настоящего времени отсутствуют формальные рекомендации по лечению больных с синдромом такоцубо. Считается, что в острой фазе заболевания показано применение транквилизаторов, если развитию синдрома предшествовал эмоциональный стресс, а также устранение других возможных провоцирующих факторов, например, боли.
Назначаются ингибиторы АПФ, β-дреноблокаторы, антикоагулянты, диуретики, антагонисты кальция.
Если Эхо-КГ не дает убедительных данных, говорящих об обструкции ВТ ЛЖ, можно с осторожностью пробовать лечение инотропными средствами, такими как добутамин и допамин.
Если Эхо-КГ выявит данные об обструкции ВТ ЛЖ, нельзя применять инотропные средства, потому что они могут ухудшить обструкцию. При умеренной и тяжелой обструкции уместно применение β-адреноблокаторов, несмотря на гипотонию. β-адреноблокаторы в таком случае могут улучшить гемодинамику, уменьшая степень обструкции.
В случае отсутствия значимого застоя легких нужно попробовать корригировать гипотонию путем инфузии кристаллоидных растворов.
Независимо от наличия градиента в выходном тракте левого желудочка, при отсутствии эффекта от медикаментозной терапии уместно приступить к интрааортной контрапульсации.
У больных с внутрижелудочковым тромбозом (по данным Эхо-КГ) необходимо проводить антикоагулянтную терапию в течение не менее 3-х месяцев. Продолжительность применения такой антикоагулянтной терапии можно изменить в зависимости от степени восстановления левожелудочковой функции и разрешения тромба.
У больных без тромбоза, но с тяжелой левожелудочковой дисфункцией уместна антикоагулянтная терапия до тех пор, пока не исчезнут признаки акинезии или дискинезии, или в течение 3-х месяцев, в зависимости от того, что наступит первым.
Прогноз. Обратимость синдрома такоцубо — важнейший признак, который помогает отличить его от многих других острых синдромов СН. Временные границы восстановления функции миокарда варьируются в зависимости от тяжести острого эпизода. В качестве ориентира: ФВ ЛЖ обычно восстанавливается через 12 недель. При этом восстановление изменений на ЭКГ может занять до 6–12 месяцев, а в некоторых случаях они могут оставаться патологическими постоянно, например, если возникают рубцовые изменения миокарда.
Возможны осложнения синдрома такоцубо:
‒ острая сердечная недостаточность (12–45 %);
‒ обструкция ВТ ЛЖ (10–25 %);
‒ митральная регургитация (14–25 %);
‒ кардиогенный шок (6–20 %);
‒ фибрилляция предсердий (5–15 %),
‒ желудочковые аритмии (4–9 %),
‒ брадикардия, асистолия (2–5 %);
‒ формирование тромбов (2–8 %);
‒ тампонада сердца (˂ 1 %);
‒ разрыв стенки желудочка (˂ 1 %);
‒ смертность в стационаре (1–4,5 %);
‒ рецидив (5–22 %);
‒ смертность в течение 5 лет (3–17 %).
Факторы развития осложнений:
‒ провоцирующие факторы физической природы;
‒ острое неврологическое или психическое заболевание;
‒ высокая концентрация тропонина;
‒ низкая ФВ в момент госпитализации.
Заключение. Синдром такоцубо представляет собой синдром острой СН, который всё больше привлекает внимание медицинских работников. Многие аспекты этого синдрома недостаточно понятны и не уточнены, а уровень современных знаний недостаточен для того, чтобы создать рекомендации по оптимальному ведению больных. Однако увеличение числа случаев синдрома такоцубо и высокая частота осложнений в период острой фазы заболевания указывает на необходимость усовершенствования тактики ведения больных.
Организация регистров синдрома такоцубо позволит создать инфраструктуру, необходимую для проведения исследований, в частности для разработки новых терапевтических тактик. В отдельных стационарах в год можно наблюдать примерно от 5 до 30 больных с синдромом такоцубо в год, поэтому для получения данных о большем числе больных необходимо создание специальных сетей.
Литература:
Основные термины (генерируются автоматически): синдром, левый желудочек, данные, обструкция ВТ, больной, генетическая предрасположенность, коронарная артерия, острая фаза заболевания, пациент, сегмент.
