Перстневидноклеточный рак желудка
2. Анапалян В.Х. Эндолимфатическая химиотерапия рака желудка: Дис. .канд. мед. наук. Томск, 1988 г.
4. Аруин Л.И., Григорьев П.Я., Исаков В.А., Яковенко Э.П. Хронический гастрит.- Амстердам, 1993.- 362с.
5. Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. М: Триада-Х, 1998. — 496 с. .
7. Балицкий К. П. (под ред.) Механизмы противоопухолевой резистентности. Киев, 1978. — 208 с.
8. Белоус Т.А. Клиническая морфология рака желудка. // Российскийсонкологический журнал. 2001. — №1. — С.46-50.
9. Белоус Т.А. Морфология начального рака желудка. // Росс, онкол. жур.-1998.- №3.- С.38-43.
10. Белоус Т.А., Г.А. Франк, К.К. Пугачев. Начальный перстневидноклеточный рак желудка. // Архив патол.-1995. №3. С.35-40.
11. Белоус Т.А., Литвинова Л.В., Пугачев К.К., Петров А.Н. Прогностическое значение морфологических параметров рака желудка.
13. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. М. — 1982. — С.750.
15. Блохин H.H., Клименков A.A., Плотников В.И. Рецидивы рака желудка. -М. 1981 160с.
17. Бордюшков Ю.Н. Нерешенные вопросы эндолимфатической и эндоликворной терапии опухолей. Сборник научных трудов РНИОИ. Способы и механизмы повышения противоопухолевой защиты в онкологии. 1993. С. 8-16.
18. Борисов В.И. Химиотерапия рака желудка и кишечника. // Росс, онкол. журнал.- 1991.- №1,- С. 56-60.
19. Боровиков В. Искусство: анализа данных на компьютере: для профессионалов. СПб. 2003. — С.688.
20. Бутов КЭШ., Мриль В.Н. Дисплазия эпителия слизистой оболочки желудка при инфильтративномраке//Врач.дело:- 1988.-№10,- С.46-48.
21. Буянов В.М., Данилов К.Ю., Радзиховский А.П. Лекарственное насыщение лимфатической системы. Киев. 1991. С. 135.
22. Василенко И.В., Садчиков В.Д., Галахин К.А. и др. Предрак . и; рак желудка: —Киев, 2001. 232 с.
23. Василенко И.В1, Дикштейн Е.А. Гистогенез рака желудка. // Вопросы? онкологии. -1991. -№6.-С. 643-651.
27. Владимирова Л.Ю. Неоадъювантная химиотерапия на естественных, средах организма с применением пептида эпифиза эпиталамина в комплексном лечении местно-распространенного рака молочной железы. Дисс. . канд. мед. наук. Ростов-на-Дону. 2000.
29. Российский онкологический журнал. 2000. — №4. — С. 7-10.
32. Гавровская Л.К., Гусяков А.К. Содержание биогенных аминов в тканях желудка крыс в течение редуцированной желудочной циркуляции. // Бюллетень экспериментальной биологии и медицины. 1983. №7. С.21-22.
33. Галахин К.А., Курик Е.Г. Лечебный патоморфоз злокачественных опухолей пищеварительного тракта. К.:Книга-Плюс, 2000.
36. Гареев P.A., Ким Т.Д. О проницаемости лимфатических сосудов. // Физиол. журнал СССР им. И.М. Сеченова. 1978. — №7. — 1014-1019.
38. Гарькавцева Р.Ф., Казубская Т.П. Генетика рака желудочно-кишечного тракта. // Жур. Современная онкология 2001, №4, С. 151-153.
41. Вопр. онкологии. 1995. — №2. — С. 117-125.
42. Горошинская И. А. Роль изменения каталитических свойств моноаминоксидазы мозга в ответной реакции организма на экстремальные воздействия. // Вопросы медицинской химии. 1989. -35, 2.-С. 2-10.
48. Деденко И.К. Аутотрансфузии крови и ее компонентов. 1997. С.240
50. Дикштейн Е.А., Василенко И.В. Гистогенез и морфологические особенности рака желудка. // Арх. патол.-1977.-№1.-С.11-17.
51. Дикштейн Е.А., Василенко И.В. Предраковые изменения и гистогенез рака желудка. // Вопросы онкологии.-1978.-Т.24, №7.-С.22-29.
52. Доманин A.A. Морфологические особенности лимфогенного распространения перстневидно-клеточного рака толстой кишщки.
53. Сов.медицина 1991, №12, С.80-81
56. Инструкция по фракционированию консервированной крови на клеточные компоненты и плазму. Приказ №06-14/24 от 11.06.1987.
57. Исаков В.А. Скрининг рака желудка: проблемы и перспективы. // РЖ гастроэнтерологии, гепатотлогии,.-2002.-№3,- С.27-31.
58. Казубская Т.П., Сельчук В.Ю., Белев Н.Ф. Генетические аспекты и прогнозирование рака желудка и ПМЗН. // С. 103.
60. Капуллер JI.JL, Доманин A.A. Перстневидно-клеточный рак толстой кишки. // Проблемы проктологии. Вып.11 Москва, 1990, С. 188-192.
62. Касьяненко И.В., Зиневич А.К., Мороз Т.Д. и соавт. // Вопр.онкол. -1986-№11., С.68-72.
65. Кветной И. М., Левин И. М. Мелатонин и опухолевый рост. // Экспериментальная онкология. 1986. — 8, 4. — С. 11-15.
70. Колесников И.С., Лыткин М.И., Плешаков В.Т. Аутотрансфузии крови и ее компонентов в хирургии. 1979. — С.216.
72. Краевский H.A., Роттенберг В.И. О гистогенезе рака желудка. // Архив патологии. 1980. — №10. — С.3-9.
74. Курский М. Д., Бакшеев Н. С. Биохимические основы механизма действия серотонина. Киев, 1974. — 294 с.
82. Марчук А.И., Петров М.М-. Предоперационная подготовка к гемотрансфузиям. // Вестник службы крови России. 1998. №2. С. 19-21.
86. Монахов Б.В. Современные возможности клинической профилактики и химиотерапииракапищеводаижелудка. // С.317-318.
90. НовиковА.С. Гистоархитектоника адренергических нервных терминалей и их клеточное микр о окружение в тканях желудка при раке и язвенной болезни. Автореф. . дис. канд. мед. наук. Саратов. 1998. С. 23.
91. Оборотова H.A. Направленная доставка противоопухолевых препаратов. // Антибиотики и химиотерапия. 1991. — №10. — С.47-50.
96. Панков А.К. Эндолимфатическая полихимиотерапия злокачественных новообразований. Москва. 1976. — С. 136.
97. Панков А.К., Новодержкин Б.А. Применение аутогемотрансфузий при хирургическом лечении больных злокачественными новообразованиями.
98. Труды 12-го Международного Конгресса по переливанию крови. М. -1972. С. 15-17
100. Юб.Панченков Р.Т., Выренков Ю.Е., Ярема И.В. и соавт. Эндолимфатическая антибиотикотерапия. Москва. 1984: С. 240:
101. Ю7.Печатникова Е.А. Пути лимфогенного метастазирования рака желудка. М. 1967 г.
103. Пожариский Ф.И. О метастатическом раке яичника. М. 1931.
105. ИЗ.Портной Л.М., Дибиров М.П., Лучевая диагностика эндофитного рака желудка. — Мосьсва, 1993- 264 с.,
108. Нб.Пухальская Е. Ч. Серотонин и клеточная пролиферация в норме и при патологии. Автореф. дисс. . доктора мед. наук. М., 1965. — 32 с.
111. И9.райхлин Н.Т., Кветной И.М., Осадчук M.A.APUD система (общепатологические и онкологические аспекты). Обнинск, 1993. 235 с.
112. Райхман Я.Г., Нидюлин В.А. Управление канцерогенной ситуацией и профилактика рака. Элиста: АПП «Джангар», 1999. — 270 с.
114. Роксин Т. Бужар X. Применение лимфографии в клинике. 1976. 139 с.
118. Русанов A.A. Рак желудка. Л.: Медицина, 1979 — С. 232.
119. Садчиков В.Д. Дисплазия покровно-ямочного эпителия слизистой оболочки желудка. // Врач, дело.- 1996.-№10.-С.65-68.
120. Самсонов В.А., Андреева P.M., Румянцева В.В. // Вопросы онкологии. -1983. -№3.- С. 57-61.
121. Сапин М.Р., Борзяк Э.И. Внеорганные пути транспорта лимфы. М. -1982. — С.264.
123. Серов В.В. Клиническая морфология и прогноз рака желудка,-М. :Медицина, 1989.-240С.
124. Серов В.В., Юшков П.В., Иванов П.К. Возможные маркеры прогрессии рака желудка. // Архив патологии. 1996. — №2. — С. 9-12.
126. Сидоренко Ю.С. Аутогемохимиотерапия. Ростов н/Д. 2002 г. — 304 с.
127. Сидоренко Ю.С. Клинико-экспериментальные аспекты эндолимфатической химиотерапии. // Сб. Эндолимфатическая химиотерапия в лечении злокачественных опухолей. 1985. — С.95-104.
128. Сидоренко Ю.С. Способ лечения рака. A.C. №940379 СССР. 1980 г.
129. Сидоренко Ю.С. Творческий поиск в онкологии. Ростов н/Д., 1991.- С. 156.
130. Сидоренко Ю.С. Эндолимфатическая полихимиотерапия в клинике. -Ростов н/Д. 1998. С.288.
131. Сидоренко Ю.С. Эндолимфатическая полихимиотерапия в лечении рака шейки матки; Дис. .канд. мед. наук. Ростов/Дон, 1978 г.
132. Сидоренко Ю.С., Кацман М.В. и др. Значение аутогемохимиотерапии с предварительным облучением в лечении рака яичников. // Вопросы клинической онкологии ‘ и нейроэндокринных нарушений при злокачественных новообразованиях. М., 1982.
134. Сидоренко Ю.С., Ильинская Е.Г. Эндолимфатическая химиотерапия запущенных форм хорионэпителиомы. Эндолимфатическаяполихимиотерапия злокачественных новообразований. Сб. статей / ПодIредакцией проф. Панкова А.К. Москва. 1976. — С. 108-110.
138. Сидоренко Ю. С. Состояние баланса стероидных гормонов у больных местно-распространенным и диссеминированным раком молочной железы. Ростов-на-Дону, 2000. — 252 с.
139. Солдаткина Н.В. Возможности аутогемохимиотерапии в экспериментальной онкологии и изучение некоторых механизмов ее действия. Диссерт . канд.мед.наук. Ростов/Дон. 2000 г.
144. Теппермен Дж., ТепперменХ. Физиология обмена веществ и эндокринной системы. М.: Мир, 1989. — 653 с.
146. Хонелидзе Г.Б., Яковлева И.А., Кощуг Т.Д. и соавт. Клиника и диагностика раннего рака желудка. Кишинев, 1978.
150. Чиссов В.И., Вашакмадзе Л.А. Рак желудка. // Избранные лекции поклинической онкологии. М.:, 2000. — С. 389-420.
152. Шапошников A.B., Неделько А.И., Пантелеева Л.А. Ваготомия в лечении пилородуоденальных язв. Ростов н/Д. — 1989. — С. 191.
155. Шуркус Е.А, Шуркус В.Е. Поясничные лимфопроводящие пути человека. // Рос. онкол. ж. — 1997. — № 6. — С. 39—43.
156. Щепотин И.Б., Эванс С. Р. Т. Рак желудка. Киев, 2000 — 227 с.
157. Юшков П.В. //Архив патол.- 1996, №4, С. 36-38.
158. Юшков П.В. // Архив патол.- 1996, №4, С. 38-40.
159. Юшков П. В. Роль эндокринных факторов в развитии рака желудка. //Архив Патол. 1998. — 3. — С. 67-70.
160. Юшков П. В. Этиология и патогенез рака желудка. //Архив Патол. -1997.- 1.-С. 69-73.
162. Ярсбински М., Влаинац X. Оценка взаимосвязи некоторых бисо-циальных факторов и рака желудка результаты клинико-анатомического исследования в Белграде. //Тер. архив.1989№10 С.40-44.
168. Aranha G.V., Georgen R. Gastric Linitis plastica is not a surgical disease. // Surgery. 1989. — V.106. — 758-763.
169. Arendt J. Melatonin assay in body fluids. //Journal Neural. Transmission. -1978.- 13.-P. 265-278.
173. Balazs A., BlazsekL Control of cell proliferation by endogenous inhibitor. -Akademiai Kiado, Budapest, 1979. 302 p.
180. Basu S., Dasgupta P.S. Role of dopamine in malignant tumor growth. // Endocrine. 2000. — V.12. — N.3. -P.237-41.
189. Broil R. et al. Tumor cell dissemination in bone marrow and peritoneal cavity.
193. Buiatti E., Cipriani F. Etiologacal epidemiology of gastric tumors. // Ann. 1st. Super Sanita.- 1996.- V.32, № 4.- P. 557 571.
211. Cong J.W. Krukenberg tumor of the ovary. // Zhonghua Zhong Liu Za Zhi. -1988. V.10. -N.6. — P.458-61.
212. Correa P. A human model of gastric cancerogenesis. // Cancer Res,-1988.-V.48.- P.3554-3560
213. Correa P. Chronic gastritis: a clinico-pathological classification: // Amer. J. Gastroenterol.- 1991.- V.83.- P.504-509.233.
214. Correa P. Gastric cancer. // Cancer Surveys 1994.- V.20.- P. 55 76.
216. Das U.N. Melatonin in the pathobiology and treatment of cancer. // Cancer, J. -1995.- 8,№3.-C. 103-108.
228. Surgery. 1996. — №12. — P. 1776-1778.
232. Gemma A., Hagiwara K., Ke Y. et al. FHIT mutations in human primary gastric cancer. // Cancer Research. 1997. — V.57. — N.8. — P. 1435-7.
238. Publication of the Federation of American Societies For Experimental Biology. 1992. — V.6. — N.9. — P. 2646-52.
247. Gastroenterology.- 1995.-V.109, №3.-P. 1495-1498.
258. Hyung W.J., Lee J.H., Noh S.H. et al. Early gastric carcinoma with signet ring cell histology. // Cancer. 2002. -№1. — C.78-83.
267. Kim H.K., Heo D.S., Bang Y.J. at al. Prognostic factors of Krukenberg’s tumor. //Gynecologic Oncology.-2001.-V.82. -N.l. -P. 105-9.
280. Journal of Surgery. 1996 — V. 66. — N. 12. — P. 813-815
294. Mackey J.R., Hugh J., Smylie M. Krukenberg tumor complicated by pregnancy. // Gynecologic Oncology. — 1996. V.61. -N.l. -P.153-5.
295. Maehara Y., Sakaguchi Y., Moriguchi S. et al. Signet ring cell carcinoma of the stomach. // Cancer. 1992. — №7. — C. 1645-1650.
298. Matley P.J., Dent D.M., Madden M.V. et al. Gastric carcinoma in young adults. Annals of Surgery. 1988. — V.208. -N.5. -P.593-6.
309. Ming S.C. Gastric carcinoma. A pathobiological classification. // Cancer-1977.-V.39,- P.2475-2485.
317. Msika S. Lymph node excision in cancer of the stomach. // J. Chir. (Paris). -1998.- V.135. -N.4. -P.155-61.
335. Savey L., Lasser P., Castaigne D. at al. Krukenberg tumors. Analysis of a series of 28 cases. // Chirurgia- 1996. V.133. -N.9-10. — P. 427-31.
349. Tahara E. // Ibid. 1990. — V. 116. — P. 121 -131.
357. Tatematsu. M., Ichinose. M., Miki. K. et al. Early gastric carcinoma with signet ring cell histology. // Cancer.-2002. C.78-83
361. Tolba Khaled A. Deliargyris Efthymios N. Cardiotoxicity of cancer therapy. // Cancer Invest. 1999. — 17, № 6. — C. 408-422.
370. Wu Chew-Wun, Chi Chi-Wen, Chang Tai-Gay et al. Sex hormone receptors in gastric cancer. // Cancer. 1990. — 65, 6. — P. 1396-1400.
С. Н. Неред, А. А. Клименков, А. Г. Перевощиков
КЛИНИКО-МОРФОЛОГИЧЕСКИЕ ОСОБЕННОСТИ ПЕРСТНЕВИДНОКЛЕТОЧНОГО РАКА ЖЕЛУДКА
ГУ РОНЦ им. Н. Н. Блохина РАМН, Москва
Клинико-морфологические особенности перстневидноклеточного рака изучены у 372 из 2308 больных раком желудка, оперированных в объеме гастрэктомии или резекции желудка. Перстневидноклеточный рак желудка преобладает у женщин и лиц молодого возраста. Для него характерны высокий процент раннего рака, низкая частота метастазов в лимфатических узлах при опухолях Т1—2, высокая частота метастазирования непосредственно в перигастральную клетчатку, по брюшине и в яичники, низкая частота метастазов в печень. При опухолях Т1—2 выживаемость после хирургического лечения перстневидноклеточного рака лучше, чем при других морфологических формах, и резко ухудшается, если опухоль прорастает серозную оболочку желудка. Лимфодиссекция на уровне D2 не приводит к улучшению отдаленных результатов хирургического лечения перстневидноклеточного рака, что обусловлено тенденцией к преимущественно имплантационному пути распространения этой морфологической формы опухоли.
Ключевые слова: желудок, перстневидноклеточный рак, хирургия, лимфодиссекция.
Перстневидноклеточный рак желудка, являясь одной из разновидностей слизистого рака, характеризуется преимущественно внутриклеточным слизеобразованием. Скопляющаяся в отдельных клетках слизь оттесняет ядро к периферии клетки, сообщая ей характерную перстневидную форму.
В соответствии с последней Международной гистологической классификацией опухолей пищевода и желудка ВОЗ в перстневидноклеточной карциноме преобладающий компонент (более 50% опухоли) представлен изолированными или расположенными мелкими группами опухолевыми клетками, содержащими внутриклеточную слизь. Хотя перстневидные клетки не формируют тубулярных структур, они функционируют как железистые, и в опухоли часто присутствует смешанный железистый компонент, поэтому перстневидноклеточный рак классифицируют как аденокарциному. По классификации Лаурена перстневидноклеточный рак относится к диффузному типу рака желудка. По данным различных авторов, перстневидноклеточный рак составляет 10—20% всех форм рака желудка .
Углубленное изучение перстневидноклеточного рака представляет интерес по следующим причинам: 1) благодаря четким морфологическим критериям он легко может быть выделен в отдельную группу для научного исследования и практического использования; 2) в литературе имеются значительные противоречия в оценке злокачественности этой морфологической формы и отдаленных результатов ее
© Неред С. Н., Клименков А. А., Перевощиков А. Г, 2004 УДК 616.33.-006.6-089
лечения. В нашей стране перстневидноклеточный рак традиционно относят к прогностически неблагоприятной форме с плохими отдаленными результатами. В публикациях японских авторов отдаленные результаты перстневидноклеточного рака практически не уступают таковым при аденокарциноме ; 3) в самом морфологическом строении опухоли также имеются противоречия: выраженное нарушение тканевой структуры сочетается с выраженным слизеобразованием, свидетельствующим, в определенной степени, о сохранении дифференцировки на клеточном уровне.
Материалы и методы
Для изучения клинико-морфологических особенностей перстневидноклеточного рака проведен анализ 2308 больных раком желудка, которым в отделении абдоминальной онкологии РОНЦ им. Н. Н. Блохина РАМН в период 1980— 2002 гг. выполнена радикальная или паллиативная гаст-рэктомия или резекция желудка. Отдаленные результаты хирургического лечения прослежены у 1674 оперированных, в том числе у 283 больных перстневидноклеточным раком, у 1207 — аденокарциномой, у 184 — недифференцированным раком желудка. Выживаемость после хирургического лечения в зависимости от объема лимфодиссекции изучена у 91 больного перстневидноклеточным раком и у 470 больных другими морфологическими формами рака желудка, оперированных в 1994—2002 гг.
Гистологическую структуру опухоли устанавливали в соответствии с Международной гистологической классификацией опухолей пищевода и желудка ВОЗ .
Статистический анализ данных выполнен с помощью программного пакета Statistica for Windows (StatSoft Inc., Версия 5.0). Сравнение полученных значений осуществляли с использованием критерия х2 Пирсона. Кривые выживаемости строили по методу Kaplan—Meyer, достоверность различий показателей выживаемости оценивали по критериям Gehan—Wilcoxon и log-rank.
Результаты и обсуждение
Перстневидноклеточный рак выявлен у 372 (16,1%) из 2308 больных раком желудка. В зарубежной литературе появляются сообщения об увеличении в последние годы доли малодифференцированных форм, в том числе перстневидноклеточного рака, среди всех форм рака желудка, этим объясняется отсутствие улучшения отдаленных результатов, несмотря на совершенствование методов лечения . В нашем исследовании такой тенденции не выявлено. Доля перстневидноклеточного рака среди всех форм рака желудка существенно не менялась на протяжении последних 20 лет и колебалась в пределах 14,7—22,0%.
Анализ распределения больных по полу и возрасту показал, что при перстневидноклеточном и недифференцированном раке преобладают женщины (54,6 и 54,7%), а при аденокарциноме, независимо от степени дифференцировки, — мужчины (58,5%). Соотношение мужчин и женщин, страдающих перстневидноклеточным и недифференцированным раком, составляет 0,8:1,0, среди больных с аденокарциномой — 1,4:1,0 (p=0,0000). Средний возраст больных перстневидноклеточным и недифференцированным раком достоверно меньше, чем при аденокарциноме (53,0 и 52,9 года против 58,8; р=0,0017, р=0,011).
Показатель резектабельности при перстневидноклеточном раке оказался достоверно меньше, чем при аденокарциноме (73,1% против 82,3%, р=0,0000).
Среди всех оперированных в объеме радикальной или паллиативной гастрэктомии или резекции желудка ранний рак обнаружен у 288 больных, распространенный рак — у 2020. Ранние формы наблюдались несколько чаще у больных перстневидноклеточным раком (17,2%), чем у больных аденокарциномой (12,3%, p<0,03) или недифференцированным раком (6,1%, p<0,0004). При распространенном перстневидноклеточном раке, так же как при недифференцированном раке, диффузный тип роста (тип В4 по Borrmann) наблюдался достоверно чаще, чем при аденокарциноме (32,8 и 34,7% против 10,4%, p<0,0000), в том числе низкодифференцированной (15,8%, p<0,000). Полиповидный тип роста (В1 по Borrmann) не встретился ни в одном случае перстневидноклеточного рака.
Значительно реже, чем другие гистологические формы, перстневидноклеточный рак локализовался в проксимальном отделе желудка (5,4% против 16,1% при аденокарциноме, p<0,000; 10,5% при недифференцированном раке, p<0,04). Соответственно, проксимальная резекция желудка составляет лишь 1,3% всех операций по поводу перстневидноклеточного рака. Тотальное поражение желудка при перстневидноклеточном раке наблюдалось в достаточно большом проценте случаев — 15,3%, что достоверно меньше, чем при недифференцированном раке (26,6%, p<0,002), но больше, чем при аденокарциноме (9,2%, p<0,002).
Перстневидноклеточный рак, ограниченный мышечной оболочкой желудка, реже метастазировал в лимфатические узлы, чем опухоли других гистологических форм (11,6% против 19,5% при недифференцированном раке и 17,4% при аденокарциноме). Эти данные согласуются с результатами исследований ряда авторов , показавших, что ранний перстневидноклеточный рак реже дает метастазы в лимфатические узлы, чем другие формы. В случае прорастания серозной оболочки желудка (Т3—4) частота метастатического поражения лимфатических узлов была практически одинакова при различных гистологических формах.
Имеется и другая особенность метастазирования перстневидноклеточного рака: он чаще, чем другие формы, метастази-рует непосредственно в перигастральную клетчатку и клетчатку сальников (20% против 14,7% при недифференцированном раке и 9,9% при аденокарциноме, р<0,03). При этом нередко метастазы в расположенных рядом лимфатических узлах отсутствуют (рис. 1). Этот тип метастазирования не учитывается ни в одной классификации стадий рака желудка, хотя выживаемость при наличии комплексов раковых клеток в клетчатке сальников и метастазов в лимфатических узлах хуже, чем в случаях поражения только лимфатических узлов (3- и 5-летняя выживаемость 12,3 и 12,3% против 38,6 и 26,1% соответственно, р<0,02).
Не менее важной особенностью перстневидноклеточного рака является высокая частота имплантационного метастази-рования. Изучение характера отдаленного метастазирования при паллиативных операциях и у больных с прогрессированием заболевания после радикальных операций показало, что разные морфологические формы рака желудка наряду с общей направленностью широкого лимфорегионарного распространения имеют различные тенденции отдаленного метастазиро-вания (рис. 2). При перстневидноклеточном и недифференцированном раке метастазы по брюшине (65,0 и 60,3% соответственно) отмечены достоверно чаще, чем при низко-
Рисунок 1. Метастазы перстневидноклеточного рака желудка в перигастральную клетчатку.
А. Перстневидные раковые клетки. Б. Лимфатический узел без метастазов, окраска гематоксилином и эозином.
Имплантационные метастазы
Перстневидно- в печени
клеточный рак 65 о
(n=137) D°’°
Недифферен-
Метастазы
,6
11,1
цированный 60,3
рак(n=63)
Аденокарцинома зз,4 p<0,003 29,4 p<0,001
(n=308)
Аденокарцинома
низко дифферен- 47 0 18 6
цированная ’ ’
Аденокарцинома
высоко- и умеренно- 17,3 47,9
дифференцированная
0 10 20 30 40 50 60 70 0 10 20 30 40 50 60 70
Рисунок 2. Характер отдаленного метастазирования различных морфологических форм рака желудка.
Эти данные позволяют осуществлять дифференцированный подход в диагностике распространенности опухолевого процесса у больных раком желудка. Алгоритм обследования больных перстневидноклеточным раком для исключения отдаленных метастазов должен включать обязательную лапароскопию с цитологическим исследованием смывов из брюшной полости, УЗИ малого таза и осмотр гинеколога, а больных аденокарциномой желудка — в первую очередь исследование печени с помощью УЗИ или КТ
Проведенное нами изучение факторов риска метастазов рака желудка в яичниках позволило выявить следующие факторы: возраст больных до 40 лет, значительная исходная распространенность опухоли, наличие перстневидноклеточного рака или присутствие большого количества перстневидных клеток в опухолях, имеющих строение низкодифференцированной аденокарциномы или недифференцированного рака. У всех женщин, оперированных по поводу перстневидноклеточного рака, риск развития метастазов в яичниках достигает 13,6%, а в группе женщин, у которых удалось установить характер прогрессирования болезни, он составляет 35,1%. Высокая частота метастатического поражения яичников при перстневидноклеточном раке является основанием для тщательного гинекологического и ультразвукового исследования яичников в процессе предоперационного обследования и послеоперационного наблюдения у больных с этой формой рака желудка. Наряду с детальной ревизией яичников во время хирургического вмешательства представляется оправданным интраоперационная биопсия яичников у больных перстневидноклеточным раком желудка, особенно в распространенных стадиях, и у лиц молодого возраста, что в перспективе может послужить основанием для решения вопроса о профилактической овариэктомии у этой категории больных. Высокая частота метастазов в яичниках при
перстневидноклеточном раке, преобладание темпов роста метастатической опухоли по сравнению с первичной, преобладание перстневидноклеточного рака у женщин, молодой (репродуктивный) возраст пациенток указывают на возможную гормональную зависимость этой морфологической формы рака желудка.
В общей группе (1674 больных) отдаленные результаты после хирургического лечения перстневидноклеточного рака существенно не отличались от таковых при аденокарциноме и были достоверно лучше, чем при недифференцированном раке (рис. 3, А). Медиана выживаемости, показатели 3-, 5-летней выживаемости составили 34,7 мес, 53,7 и 45,3% при перстневидноклеточном раке; 31,5 мес, 51,7 и 45,3% (p>0,6) при аденокарциноме; 18,0 мес, 38,6 и 31,1% (p<0,0001, критерий log-rank: p<0,0003) при недифференцированном раке. Соотношение стадий болезни в сравниваемых группах существенно не различалось. Важно отметить выраженное различие в выживаемости у больных с опухолями (перстневидноклеточным и недифференцированным раком), относящимися к одному гистологическому типу (диффузный тип) по классификации Лаурена.
Как было показано выше, перстневидноклеточный рак отличается высокой частотой имплантационного метастазирова-ния, поэтому в первую очередь нас интересовали отдаленные результаты с учетом глубины инвазии опухоли, т. к. факт прорастания серозной оболочки желудка имеет решающее значение для реализации имплантационного метастазирования.
Выживаемость Выживаем°сть Выживаемость
Время, мес
Время, мес
В 0 20 40 60 80 100 120 140 160 180 200
Время, мес
Рисунок 3. Выживаемость больных раком желудка после хирургического лечения.
А. Общая группа. Б. При опухоли Т1-2. В. При опухоли Т3-4.
1 — перстневидноклеточный рак; 2 — аденокарцинома; 3 — недифференцированный рак. Здесь и на рис. 4, 5 по оси абсцисс — время после операции, мес; по оси ординат — кумулятивная пропорциональная выживаемость по Kaplan-Meyer; n — число больных.
Анализ отдаленных результатов в зависимости от распространенности опухоли подтверждает достаточно высокие показатели выживаемости у больных перстневидноклеточным раком в начальных стадиях болезни (рис. 4).
Хорошей выживаемостью при начальных стадиях перстневидноклеточного рака и плохой при распространенных объясняются существующие разногласия в оценке злокачественности этой формы опухоли. В Японии, где более половины вновь зарегистрированных случаев относятся к раннему раку, показатели выживаемости после хирургического лечения перстневидноклеточного рака практически не уступают таковым при аденокарциноме. В России и в Европе большинство больных выявляются в распространенных стадиях, отсюда и отношение к перстневидноклеточному раку как к крайне неблагоприятному. Именно при перстневидноклеточном раке в случае прогресса в ранней диагностике рака желудка можно ожидать качественного скачка в улучшении отдаленных результатов хирургического лечения.
Наше исследование не выявило эффективных методов комбинированного лечения перстневидноклеточного рака желудка. Использование предоперационной лучевой терапии (СОД 22—30 Гр, РОД 4—5 Гр) у 34 больных и дополнительной системной химиотерапии (5-FU или ЕАР) у 28 больных не привело к достоверному улучшению отдаленных результатов лечения этой морфологической формы рака желудка.
1,0
0,9
0,8
0,7
_й
g 0,6
І 0,5
I 0,4
m 0,3 0,2 0,1 0,0
Л p<0,00000
! I ■
i»l——
Ia (n=43)
Ib (n=36)
II (n=63)
IIIa (n=65)
IV (n=36) IIIb (n=40)
0 20 40 60 80 100 120 140 160 180 200
Время, мес
Рисунок 4. Выживаемость больных перстневидноклеточным раком желудка после хирургического лечения в зависимости от стадии болезни.
Высокий риск имплантационного метастазирования при перстневидноклеточном раке явился поводом для оценки эффективности D2-лимфодиссекции в этой группе больных, поскольку эффект от удаления регионарных лимфатических узлов может нивелироваться быстрым развитием канцерома-тоза брюшины. Наше исследование показало, что D2-лим-фодиссекция не улучшает показатели выживаемости у больных перстневидноклеточным раком (рис. 5, А), несмотря на явное преобладание поздних стадий в группе с Dl-лимфо-диссекцией. Медиана выживаемости, 3- и 5-летняя выживаемость после D2- и Dl-лимфодиссекций составили 16,4 мес,
44.1 и 44,1%; 25,6 мес, 44,8 и 40,1%, соответственно (p<0,5, критерий log-rank: p<0,8).
В то же время отмечена высокая эффективность расширенных лимфодиссекций при аденокарциноме желудка, отличающейся относительно низкой частотой метастатического поражения брюшины (рис. 5, В). После D2-лим-фодиссекции медиана выживаемости, 3- и 5-летняя выживаемость составили 21,6 мес, 65,9 и 58,8% против 24,3 мес,
52.2 и 42,9% после D1-лимфодиссекции (p<0,03, критерий log-rank: p<0,02), причем улучшение результатов прослеживается при различной степени дифференцировки аденокарциномы и при анализе выживаемости с учетом стадии болезни. Важно отметить, что улучшение отдаленных результатов после расширенной лимфодиссекции наблюдается при аденокарциноме даже в случаях поражения опухолью серозной оболочки желудка (медиана выживаемости, 3- и 5-летняя выживаемость составили 15,4 мес, 49,8 и 42,5% против 18,6 мес, 39,3 и 23,8% после D1-лимфодис-секции, p<0,09, log-rank test: p<0,04).
Выводы
1. Клинико-морфологическими особенностями перстневидноклеточного рака являются преобладание этой формы рака у женщин и лиц молодого возраста, более высокий процент раннего рака, чем при других гистологических формах (17,2 и 11,6% соответственно). При перстневидноклеточном раке отсутствует полиповидный тип (В1 по Borrmann) и наблюдается высокий процент (32,8%) диффузного типа (В4) роста опухоли.
2. Для перстневидноклеточного рака желудка характерны меньшая частота метастазирования в лимфатических узлах, чем при других морфологических формах, если опухоль не прорастает серозную оболочку желудка (11,6 против 19,5% при недифференцированном раке и 17,4% при аденокарциноме).
3. Важной особенностью перстневидноклеточного рака желудка являются высокий процент метастазирования непосредственно в перигастральную клетчатку и клетчатку сальников (20%), высокий процент метастазирования по брюшине (65,0%) и в яичники (13,6%), низкий процент метастазирования в печень (9,6%).
Время, мес
В
Время, мес
Рисунок 5. Выживаемость после операций с D2-лимфодиссекцией при различных морфологических формах рака желудка.
А. Перстневидноклеточный рак. Б. Недифференцированный рак. В. Аденокарцинома.
Б
4. При перстневидноклеточном раке, ограниченном мышечной оболочкой желудка, выживаемость после хирургического лечения лучше, чем при других морфологических формах. Показатели 3- и 5-летней выживаемости составляют 87,9 и 82,4% против 80,6 и 73,4% при аденокарциноме и 73,7 и 55,3% при недифференцированном раке. Если опухоль прорастает серозную оболочку желудка, выживаемость при перстневидноклеточном раке резко ухудшается и различие в выживаемости с другими формами практически исчезает.
5. При перстневидноклеточном раке, в отличие от аденокарциномы желудка, D2-лимфодиссекция не приводит к улучшению отдаленных результатов хирургического лечения, что обусловлено тенденцией к преимущественно им-плантационному пути распространения этой морфологической формы опухоли.
ЛИТЕРАТУРА
1. Белоус Т. А. Клиническая морфология начального рака желудка: Дис… д-ра мед. наук. — М., 1998. — 301 с.
2. Watanabe H., Jass J. R., Sobin L. H. et al. Histological Typing of
Oesophageal and Gastric Tumours (International histological classification of tumours). — 2nd ed. — New York, 1990. — 565 p.
6. Maehara Y., Sakaguchi Y., Moriguchi S. et al. Signet ring cell carcinoma of the stomach // Cancer. — 1992. — Vol. 69, N 7. — P. 1645—1650.
Поступила 01.09.2004
S. N. Nered, A. A. Klimenkov, A. G. Perevostchikov
CLINICOMORPHOLOGICAL FEATURES OF SIGNET-RING CELL CARCINOMA OF THE STOMACH
N. N. Blokhin RCRC RAMS, Moscow
Онкологические заболевания нередко называют чумой XXI века. Действительно, распространенность патологий, к сожалению, растет, и врачи пока не нашли лекарства, которое действовало бы на все виды рака. Среди онкологических заболеваний рак желудка — один из самых распространенных: в год фиксируется около миллиона новых случаев, а смертность от рака желудка превышает 500 тысяч человек в год . Россия входит в число стран, где эта патология диагностируется достаточно часто. Какие симптомы у рака желудка и как его лечить, мы расскажем в статье.
Содержание
Классификация рака желудка
Словом «рак» обозначаются злокачественные новообразования, состоящие из клеток, деление которых происходит бесконтрольно. Такие образования (опухоли) могут проникать в другие органы, давая метастазы, нарушать их работу, приводить к серьезному нарушению функционирования всего организма. Рак желудка может возникать в любом отделе этого органа: пилорическом, кардиальном, на большой и малой кривизне и так далее. Опухоль может поражать как часть желудка, так и весь орган.
Частота возникновения метастазов при этом заболевании превышает 80% . Но на ранних стадиях проявления заболевания можно спутать с другими патологиями, поэтому пациенты нередко не обращают на тревожные симптомы внимания и начинают лечение несвоевременно.
Медицинская статистика
Рак желудка имеет очень широкое распространение и уступает по частоте возникновения только раку органов дыхания (трахеи, бронхов и легких) и раку молочной железы. Согласно статистическим данным за 2017–2018 годы, ежегодно в нашей стране регистрируют около 37 тысяч новых случаев рака желудка, из них в первый год после постановки диагноза умирает почти половина — 47,4% . Это коррелируется с высокой — 39,9% — долей больных, первично выявленных с запущенным опухолевым процессом (IV стадия) . Мужчины страдают от рака желудка чаще женщин.
Перечислим различные существующие сегодня классификации рака желудка.
Международная классификация ВОЗ выделяет несколько разновидностей рака:
- папиллярная аденокарцинома (опухоль из железистого эпителия);
- тубулярная аденокарцинома (опухоль из клеток кубического и цилиндрического эпителия);
- низкодифференцированная аденокарцинома (клетки, образующие опухоль, плохо различаются);
- муцинозная аденокарцинома (опухоль состоит из эпителиальных клеток, которые могут продуцировать слизь);
- перстневидный рак желудка (атипичные клетки быстро распространяются вглубь органа);
- плоскоклеточный рак (развивается из клеток шиповатого слоя эпителия);
- железисто-плоскоклеточный рак (сочетание аденокарциномы и плоскоклеточного рака);
- карциносаркома (достаточно редко встречающаяся опухоль, состоящая из клеток разного вида);
- хориокарцинома (редкая агрессивная форма заболевания, которая характеризуется ранним метастазированием);
- недифференцированный рак (также агрессивная форма заболевания, для которого характерно раннее метастазирование);
- другие формы рака.
В рамках классификации по морфологическому признаку выделяются следующие виды рака желудка:
- ограниченно растущий рак (экзофитная форма). Обычно для этой формы заболевания характерны кровотечения, симптомы интоксикации. Достаточно хорошо поддается излечению;
- инфильтративно растущий рак (эндофитная, диффузная форма). Чаще связан с ростом метастазов, быстрым поражением желудка;
- переходные формы, объединяющие черты перечисленных двух.
Классификацию рака желудка по гистологическому признаку называют также классификацией по Lauren. Фактически она описывает три формы рака желудка:
- кишечный тип. Эта разновидность заболевания подобна раку кишечника. Опухоль напоминает железистую структуру;
- диффузный тип. В опухоли дифференцируются одиночные клетки или небольшие группы клеток с большим содержанием муцина (слизи);
- смешанный тип, для которого характерны черты описанных выше форм рака желудка.
Стадии и симптоматика желудочной онкологии
Если пациенту поставлен диагноз «рак желудка», то следующая задача врача — установить стадию заболевания. Современная медицина выделяет пять стадий.
- Нулевая. Начало процесса перерождения нормальных клеток эпителия в патологические. На этой стадии рак обычно не имеет проявлений, но если заболевание диагностируют, то пациенту рекомендуют оперативное лечение с высокими шансами на полное выздоровление.
- Первая. Врачи отмечают возникновение опухоли с четкими контурами, которая или находится в слизистом слое, или начинает проникать в мышечный. Симптомы: быстрая утомляемость, падение уровня гемоглобина в крови, вздутие живота после еды, отказ от еды, бледность.
- Вторая. На этой стадии опухоль начинает поражать не только оболочки желудка, но и лимфатические узлы. Рак на этой стадии вызывает болезненность желудка, жар, боль при глотании. Необходимо удалять опухоль, но если она находится в районе крупных сосудов, то операция сопряжена с очень большим риском.
- Третья. Опухоль разрастается, затрудняя движение желудка, начинается ее прорастание в соседние органы. Поражается мышечный слой стенки желудка и большое количество лимфоузлов. На этой стадии заболевания происходит резкое расстройство пищеварения, постоянная тошнота сочетается с запорами и диареей, пациент теряет вес.
- Четвертая. Опухоль прорастает в соседние, а также отдаленные органы (в том числе и в головной мозг), поражает большое количество лимфоузлов. На этой стадии рак желудка вызывает постоянные боли, частую рвоту с примесями крови, ощущение тяжести даже при небольших порциях съеденной пищи, накопление жидкости в брюшине. На этой стадии излечение рака невозможно, основная цель лечения — облегчение состояния пациента и предупреждение осложнений.
Диагностика
Мы уже упомянули о том, что рак желудка на начальной стадии не имеет явных симптомов. При этом, чем раньше обнаружена патология, тем выше шансы на успешное излечение. Именно поэтому важно знать о методах диагностики, с помощью которых можно достоверно выявить это опасное заболевание.
Обратите внимание
На ранней стадии заболевание может проявляться таким комплексом симптомов, как быстрое насыщение, снижение интереса к мясной пище, анемия, потеря веса, дискомфортные ощущения в желудке. На более поздних стадиях начинаются боли, постоянная тошнота, кровотечения, изменения стула.
Ассоциация онкологов России разработала рекомендации, в соответствии с которыми основными методами диагностики рака желудка являются следующие:
- Осмотр, сбор анамнеза.
- Эндоскопия верхних отделов ЖКТ, биопсия тканей. В ходе обследования уточняются размеры опухоли, визуализируются ее границы.
- Рентген желудка. Врач может оценить протяженность опухоли, однако не при всех видах рака желудка этот вид диагностики показателен.
- УЗИ или КТ органов брюшной полости. УЗИ — неинвазивный метод диагностики, хорошо переносится пациентами. Позволяет оценить, есть ли метастазы и насколько они распространились.
- Клинический и биохимический анализы крови.
- ЭКГ и обследование грудной полости.
Лечение рака желудка
На сегодняшний день существует несколько методик лечения рака желудка, эффективность которых зависит от стадии заболевания, локализации опухоли, состояния пациента. Расскажем подробнее о каждом из видов лечения.
Оперативное лечение
Операция по удалению части желудка или желудка полностью является самым распространенным методом радикального лечения рака. При этом, если операция проведена вовремя — на ранней стадии рака, — выживаемость составляет более 90% в течение пяти лет . Во время операции удаляется не только часть органа или желудок полностью, но и лимфоузлы — в большом количестве, если есть серьезный риск распространения опухоли.
Медикаментозное лечение
Медикаментозное лечение рака желудка проводится по нескольким направлениям. Во-первых, это обезболивающие препараты, причем на начальных стадиях заболевания не рекомендуется прописывать сильные анальгетики. В противном случае они не будут действовать на более поздних стадиях. В сочетании с анальгетиками могут быть назначены антидепрессанты и нейролептики для усиления эффекта.
Во-вторых, это препараты, которые помогают справиться с неприятными симптомами, такими как тяжесть в желудке, изжога, вздутие, тошнота. Это могут быть ферментные препараты, лекарства против изжоги.
В-третьих, это, собственно, противоопухолевые препараты. К данной группе относятся, в частности, препараты на основе тегафура, капецитабина и другие. Они же оказывают иммуномодулирующее действие.
Химиотерапия
На протяжении довольно длительного времени считалось, что при раке желудка химиотерапия неэффективна. Однако последние исследования показали, что трех- и пятилетняя выживаемость пациентов при применении химиотерапии значительно вырастает .
Чаще всего для лечения рака желудка в рамках химиотерапии применяется 5-фторурацил, который блокирует деление клеток, а значит, и рост опухоли. В последние годы чаще стали использоваться препараты платины в составе комбинированной химиотерапии. Также химиотерапия применяется в сочетании с лучевым лечением.
Лучевая терапия
Как и при лечении других форм рака, при поражении желудка применяется лучевая терапия, которая в данном случае ограничена близким расположением других органов и вариабельным положением желудка. При облучении нужно, чтобы воздействию подвергался весь желудок, но в этом случае в зону облучения попадают, например, почки или сердце. Это осложняет проведение лечения.
Второй непростой момент при проведении лучевой терапии — питание больных. Рак желудка нередко приводит к серьезной потере массы тела, отсутствию аппетита, у больного может развиться анорексия. Лучевая терапия, ухудшающая самочувствие пациента, приводит к еще большему сокращению рациона, поэтому очень важно подобрать для пациента оптимальный режим питания и диету.
Лучевая терапия применяется в сочетании с другими методами. В частности, она может выполняться и во время операции, когда действие пучка частиц наиболее направлено. Такая методика помогает избежать лучевых осложнений.
На заметку!
В России показатель пятилетней выживаемости больных с раком желудка составляет 57,5% (информация по итогам 2018 года) .
Паллиативное лечение
Паллиативное лечение проводится на поздних стадиях рака желудка, чтобы облегчить состояние пациента. Удалить опухоль или избавиться от метастазов на этой стадии, как правило, невозможно, однако можно добиться облегчения состояния пациента. Для этого проводятся паллиативные операции, которые улучшают пищеварение, облегчают прохождение пищи по ЖКТ. Выполняется паллиативное удаление опухоли и метастазов. Это не приводит к излечению от рака, но улучшает качество жизни пациента. Также паллиативные операции по удалению очага опухоли уменьшают ее массу, снижают интоксикацию организма, позволяют провести курс химио- или лучевой терапии, который оказывается более эффективным.
Врачи отмечают, что перспективы пациента с любым видом рака, в том числе раком желудка, зависят от того, на какой стадии заболевания началось лечение. На ранних стадиях возможность благоприятного исхода превышает 80% . Однако многие пациенты обращаются к врачам тогда, когда заболевание уже серьезно сказывается на общем состоянии здоровья, когда пострадал не только желудок, но и лимфатическая система, а также близлежащие органы, что существенно затрудняет лечение. В частности, оперативное вмешательство не дает заметного результата, когда врачи вынуждены назначать симптоматическое, то есть поддерживающее, лечение. Именно поэтому необходимо обращаться к специалистам при появлении первых тревожных симптомов, таких как потеря веса, расстройство аппетита, тошнота, наличие крови в кале и других. В некоторых случаях бывает целесообразно обратиться в зарубежное лечебное учреждение.
Источники:![]()
Получить бесплатную консультацию
Ведущие специалисты Центра ответят на ваши вопросы.
Получить консультацию
Узнать цену
Услышав в свой адрес диагноз «рак желудка», важно понять, что хоть это серьезное жизненное испытание, но при верной диагностике, при своевременности обращения к специалистам, при качественном лечении заболевания можно вернуться к полноценной жизни.
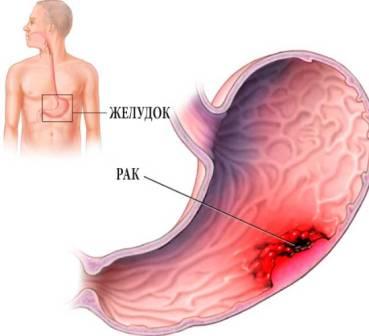
Что такое рак желудка?
Это злокачественная опухоль, растущая из слизистой оболочки – самого внутреннего слоя стенки желудка. Именно этот слой контактирует с пищей и желудочным соком.
Как и любая другая злокачественная опухоль, он отличается постепенным, но неумолимым ростом и, при достижении определенной фазы своего развития, может давать метастазы – вторичные опухолевые узлы в других органах (печень, легкие, кости, лимфатические узлы, яичники и так далее).
Рак желудка опасен не только тем, что, в процессе своего роста, истощает силы организма человека (это черта всех злокачественных опухолей), но и тем, что может привести к серьезным и угрожающим жизни осложнениям, даже находясь в стадии, поддающейся лечению.
Наиболее часто этими осложнениями являются:
- кровотечение из опухоли,
- перфорация опухоли (то есть разрыв ее с образованием сквозного отверстия в брюшную полость)
- перекрытие (стеноз) выходного или входного отделов желудка с развитием серьезных нарушений питания.
Среди всех разновидностей опухолей желудка рак встречается наиболее часто. Около 90-95% всех опухолей желудка являются злокачественными.
Таким образом, любое опухолевидное поражение стенки желудка, а тем более его слизистой оболочки – это очень серьезное подозрение на рак желудка, требующее тщательного, своевременного и полноценного обследования.
Статистика
Рак желудка – один из самых распространенных видов опухолевого поражения органов человека. Болезнь эта занимает 6-ю строчку в структуре заболеваемости злокачественными заболеваниями в мире. В Республике Беларусь рак желудка в структуре онкологических заболеваний занимает 4-е место у мужчин и 6-е место у женщин.
Свыше 780 тысяч человек в мире ежегодно умирает от рака желудка. Говоря о мировой статистике смертности из-за злокачественных образований, следует отметить, что лишь рак легкого и толстого кишечника опережает раковые опухоли желудка.
Классификация рака желудка
У болезни существует несколько классификаций. Согласно международной, принятой Всемирной организацией здравоохранения (ВОЗ), рак желудка подразделяется на две категории: распространенный и ранний.
В первой половине ХХ века начали использовать морфологическую классификацию по анатомическому признаку:
- первый вид рака желудка (Тип 1) – полиповидный или грибовидный – в форме гриба, бляшки, полипа – отчетливо отделяется от здоровой ткани и имеет ножку;
- второй вид рака желудка (Тип 2) – экзофитный изъязвленный или блюдцеобразный у такого рака желудка края приподняты, а границы четко очерчены. Этот тип заболевания – деструктивная стадия грибо- и полиповидного рака;
- третий вид рака желудка (Тип 3) – язвенно-инфильтративный, у такого рака нет четкого отграничения от стенки желудка, как у первого вида;
- четвертый вид рака желудка (Тип 4) – диффузно-инфильтративный, у такого рака стенки органа утолщаются, в результате чего желудок выглядит как толстостенная трубка;
- пятый вид рака желудка (Тип 5) – неклассифицируемые опухоли желудка.
В следующей классификации всего два вида:
- рак желудка кишечного типа,
- рак желудка диффузного типа.
Название первого говорит о том, что он напоминает опухоли кишечника. Раковые ткани представляют собою резко очерченные железистые структуры из цилиндрического эпителия. Для болезни такого типа характерна стадийность. Развивается болезнь под воздействием окружающей среды, неправильного образа жизни и питания. Влияет на развитие рака желудка и наличие бактерии H. Pylori.
Причиной возникновения второго вида может быть наличие в организме дефектного гена. Особенностью данного типа поражения является многоочаговость опухоли. Болезнь развивается быстро, агрессивно. Требуется срочное хирургическое лечение рака желудка данного типа.
Выделяют и третий вид – смешанного типа, где присутствуют признаки обоих, перечисленных выше.
По гистологическому типу классификации, принятому ВОЗ в 2010 году, опухоли желудка делятся на следующие разновидности:
- Аденокарцинома
— папиллярная
— тубулярная
— муцинозная
— некогезивная (перстневидноклеточная)
— смешанная - Железистоплоскоклеточный рак
- Медуллярная карцинома
- Плоскоклеточный рак
- Гепатоидная аденокарцинома
- Недифференцированный рак
- Нейроэндокринная опухоль G1 (карциноид)
- Нейроэндокринная опухоль G2
- Нейроэндокринная карцинома
- Мелкоклеточный нейроэндокринный рак
- Крупноклеточный нейроэндокринный рак
- Смешанная железисто-нейроэндокринная карцинома
Стоящая на первом месте аденокарцинома – самый распространенный и агрессивный вид рака желудка. Успешное лечение аденокарциномы желудка возможно только при ранней диагностике. Лишь в этом случае возможна высокая выживаемость (до 90%). Поражает болезнь железистый эпителий органа. При диагнозе «аденокарцинома желудка» хирургическое лечение – по сути, единственная возможность полного излечения, поскольку аденокарцинома желудка относится к опухолям малочувствительным к химиотерапии.
Лечение других редко встречающихся гистологических разновидностей рака желудка принципиально мало отличается от лечения аденокарциномы, так как во всех случаях на первом этапе рассматривается вопрос о хирургическом лечении. Большую роль гистологический вариант опухоли играет в первую очередь для планирования лекарственного лечения, то есть химиотерапии, так как разные варианты опухоли отличаются своей чувствительностью к химиопрепаратам.
Стадии рака желудка
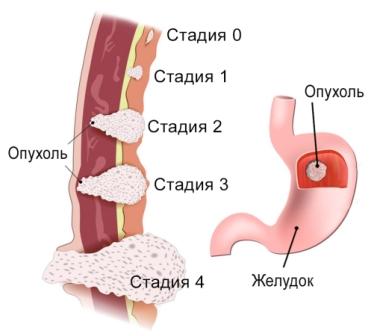
Степень поражения органа раковыми клетками чаще всего устанавливают после проведения оперативного вмешательства. Чтобы оценить стадию заболевания, учитывают несколько факторов:
- глубина поражения желудочной стенки;
- поражены ли метастазами лимфоузлы, расположенные непосредственно около желудка;
- есть ли метастазы в отдаленных лимфоузлах и/или других органах.
0 стадия — патология в клетках выявляют в самом поверхностном слое слизистой желудка.
1 стадия — опухоль проникает в единичные лимфоузлы, а также в мышечный слой стенки желудка.
2 стадия — раковые клетки поражают внешний слой желудочной стенки и большее количество лимфатических узлов –На этом этапе отдаленных метастазов (то есть опухолевых очагов в других органах и/или отдаленных лимфоузлах) еще нет.
3 стадия — распространение злокачественной опухоли на самый наружный – серозный слой стенки желудка. Раковые клетки поражают близлежащие внутренние органы брюшной полости и также поражают лимфатические узлы.
4 стадия – последняя – диагностируется, если у пациента есть метастазы в отдаленных лимфоузлах и/или других органах.
Симптомы
Первые признаки зарождающейся болезни незаметны. Пациента могут беспокоить периодические болевые ощущения и легкий дискомфорт в области желудка, тошнота, потеря аппетита, рвота, слабость, изжога.
На более позднем этапе развития онкологии появляются кровотечения, отрыжка, изменение стула и его цвета (при хроническом подтекании крови из желудка, кал становится черным), потеря веса, чувство переполненности желудка, постоянная тошнота, желтушность кожных покровов и глаз.
Диагностика рака желудка
Эффективность лечения рака желудка зависит от своевременности обнаружения развивающейся опухоли. Диагностика рака желудка включает в себя два вида:
- первичная;
- уточняющая.
Первичное обследование
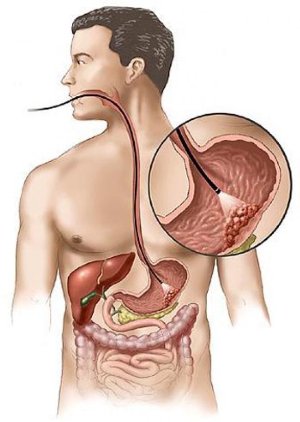
К методам первичной диагностики при раке желудка относится (первичная диагностика позволяет определить факт наличия опухоли):
- Эзофагогастродуоденоскопия (ЭГДС) с прицельной биопсией (взятие кусочков ткани для последующего гистологического исследования). Она позволяет подтвердить либо опровергнуть диагноз, определить тип раковых клеток, увидеть изменения в слизистой.
Уточняющая диагностика
После подтверждения факта наличия опухоли в желудке назначается уточняющая диагностика, которая позволяет определить распространенность имеющейся опухоли. В нее могут входить такие методы обследования, как:
- Компьютерная томография органов брюшной и грудной полостей, полости таза с внутривенным контрастированием сосудов при необходимости – метод позволяет оценить характер распространения опухоли, вовлечение смежных органов, крупных сосудов и пр.;
- Позитронно-эмиссионная томография всего тела метод, включающий в себя компьютерную томографию и одновременной введение в сосудистое русло радиоактивного препарата, по свечению которого, более достоверно определяется характер распространения опухоли (данный метод имеет ряд ограничений в отношении рака желудка, так как данный тип опухоли относится к опухолям плохо накапливающим радиоактивный препарат (фтордезоксиглюкозу);
- Ультразвуковое исследование органов брюшной полости и забрюшинного пространства используется для обнаружения границ опухоли, ее прорастания в близлежащие лимфоузлы и органы, распространения метастаз, наличия в брюшной полости асцитической (метастатической) жидкости и др.;
- Эндоультрасонография желудка соединяет в себе два метода: ЭГДС и УЗИ и позволяет произвести оценку врастания опухоли в глубину желудочной стенки изнутри полости желудка. Метод особо актуален в случаях раннего рака желудка, так как именно в таких случаях возможно выполнение удаления образования сразу во время ЭГДС без обширных оперативных вмешательств.
- Рентгеноскопия пищеварительного тракта с барием. Контрастное вещество помогает увидеть границы новообразования в желудке, определить степень сужения желудка опухолью, наличие кишечной непроходимости при метастатическом поражении стенок кишечника и пр.;
- Лапароскопия под наркозом через проколы помогает определить стадию болезни и обнаружить места расположения метастазов, которые не видны при КТ и ультразвуковом исследовании.
Функциональная диагностика
Проводится после уточняющей диагностики и ставит перед собой задачу определить возможно ли проведение планируемого противоопухолевого лечения у конкретного пациента. Спектр обследований разнится у каждого конкретного пациента, но обычно включает: анализы крови, ЭКГ, оценка дыхательных резервов, ЭХО-КГ (ультразвуковое исследование сердца), ХМ-ЭКГ (24-часовое мониторирование ЭКГ), УЗИ сосудов шеи и нижних конечностей и многие другие.
Методы лечения рака желудка
Где лечить рак желудка — за границей или в Беларуси – решать пациенту.
В белорусских центрах работают высококвалифицированные онкологи. Если вовремя диагностировать и лечить рак желудка в Беларуси, то можно добиться высокой выживаемости.
К основным методам лечения рака желудка относятся хирургический, лекарственный и лучевой.
Хирургический метод
Самое распространенное радикальное лечение – это хирургическое удаление рака желудка. Минск – это город, где подобные операции проводят на регулярной основе. Этот метод применяют на разных стадия лечения онкологических заболеваний.
В начальной стадии развития болезни возможно применение эндоскопического лечения, то есть удаления опухоли посредством эндоскопа во время ЭГДС, либо удаления лишь небольшого участка желудочной стенки с опухолью во время операции, сохраняя при этом орган.
На более поздних стадиях развития болезни объем вмешательства будет иным: удаляют либо часть желудка (резекция) либо весь орган (гастрэктомия). Помимо удаления самого органа с опухолью обязательному удалению подлежат и окружающие желудок лимфоузлы.
На 4-й стадии болезни возможности хирургического лечения сводятся к уменьшению страданий пациента. Выполняют операции для установки питательных трубок (для кормления), устранения явлений непроходимости и лишь при непосредственной угрозе жизни пациента (кровотечение или распад опухоли, ввиду которых пациент погибнет без лечения в течение часов или дней) проводят операции по удалению желудка с опухолью.
Химиотерапия (лекарственная терапия)
Такое лечение в Республике Беларусь назначают после операции на желудке для закрепления результатов хирургического лечения и отдаления сроков возможного возврата болезни. Проводят такую терапию курсами (обычно два или три) и иногда в сочетании с лучевой терапией.
При проведении лечения могут использовать одновременно несколько лекарств. Их вводят внутривенно. Различные лекарственные препараты по-разному воздействуют на раковые клетки, не давая им делиться и уничтожая. Стоимость химиотерапии при раке желудка во многом зависит от количества назначенных препаратов.
Отдельного внимания при распространенном раке желудка заслуживает перфузионная термохимиотерапия, которая проводится сразу после операции после удаления опухоли в условиях операционной. В брюшную полость на несколько часов вводится разогретый раствор химиопрепаратов. Такое лечение позволяет значительно уменьшить вероятность возврата болезни в брюшной полости.
Лучевая терапия
Суть метода в том, что пациент подвергается облучению ионизирующим излучением. Это позволяет замедлить рост опухоли и убить ее клетки. Лучевая терапия рака желудка в Республике Беларусь проводится по показаниям после операции в сочетании с химиотерапией.
Специалисты используют два вида лучевой терапии:
- дистанционную;
- брахиотерапию.
В первом случае при помощи специального оборудования луч воздействует на опухоль, проходя через здоровые органы и ткани. Во втором – в злокачественное новообразование вводится катетер, игла, струна либо зерно, наполненное радиоактивными веществами.
Прогноз заболевания
Успех лечения зависит во многом от ранней диагностики заболевания и выбора подходящих методов терапии.
Немаловажно и общее состояние здоровья человека, ведь есть факторы, приводящие к развитию болезни: злоупотребление спиртными напитками, нездоровый образ жизни, наследственность.
Успех лечения зависит и от выявленной стадии онкологии. На начальной фазе процент выживаемости достигает 70-80%, на второй – 50-60%. На третьей и четвертой процент выживаемости еще ниже. Поэтому так важно вовремя обратиться к врачу при возникновении жалоб на здоровье.
Прейскурант цен
* Примечание:
Цены указаны для иностранных граждан. Граждане Республики Беларусь могут получить медицинские услуги без взимания платы.
*Цены ориентировочные, т.к. расчет за услуги производится в бел. руб. *Ознакомиться со всеми видами услуг и точными ценами можно на странице
| Вид медицинского исследования | Цена, RUB | Цена, USD |
|---|---|---|
|
Эзофагогастродуоденоскопия |
5744 | |
|
Гематологические исследования |
||
|
Определение скорости оседания эритроцитов |
191 | |
|
Для негематологических заболеваний (единичное) |
766 | |
|
Подсчет миелограммы |
5234 | |
|
Исследования с использованием гематологических анализаторов автоматических, с дифференцировкой лейкоцитарной формулы |
957 | |
|
Биохимические исследования |
||
|
Определение калия, натрия и хлора посредством автоматических анализаторов (единичное) |
765 | |
|
Определение показателей кислотно-основного состояния крови посредством автоматических анализаторов (единичное) |
574 | |
|
Исследование биопсийного и операционного материала (за 1 номер исследования) |
1787 |
Операции на желудке
* Примечание:
Цены указаны для иностранных граждан. Граждане Республики Беларусь могут получить медицинские услуги без взимания платы.
*Цены ориентировочные, т.к. расчет за услуги производится в бел. руб. *Ознакомиться со всеми видами услуг и точными ценами можно на странице
| Вид медицинского исследования | Цена, RUB | Цена, USD |
|---|---|---|
|
Гастрэктомия |
185106 | |
|
Субтотальная резекция желудка |
149999 | |
|
Проксимальная резекция желудка |
162765 | |
|
Секторальная резекция желудка |
102127 | |
|
Экстирпация резецированного желудка |
197871 | |
|
Резекция резецированного желудка |
162765 | |
|
Обходной гастроэнтероанастомоз с межкишечным соустьем |
102127 | |
|
Диагностическая лапаротомия |
60638, | |
|
Гастрэктомия |
185106 |