Осумкованный плеврит
The paper considers differential diagnosis of pleural exudates, presents a stepped scheme of etiological diagnosis of exudate in terms of the capacities of a multidisciplinary hospital, gives an algorythm of a physician’s actions while diagnosing the exudate, lists all main causes of abnormal accumulation of fluid in the pleural cavity.
С.Л. Маланичев, Г.М. Шилкин.
Отделение пульманологии СПГМ и М, Москва
S.L. Malanichev, G.M. Shilkin
Departament of Pulmonology, SPHWM, Moscow
Несмотря на богатый опыт, накопленный отечественной и зарубежной медициной по диагностике, тактике ведения и лечения экссудативных плевритов, они по-прежнему остаются проблемой в плане установления их этиологической принадлежности.
Плевральный выпот — это скопление патологической жидкости в плевральной полости при воспалительных процессах в прилежащих органах или листках плевры или же при нарушении соотношения между коллоидно-осмотическим давлением плазмы крови и гидростатическим давлением в капиллярах.
Симптоматика плеврального выпота разнообразна и во многом определяется патологическим процессом, вызвавшим его, и количеством жидкости в плевральной полости. Основными симптомами плеврального выпота являются сухой кашель, одышка и чувство тяжести на пораженной стороне. Плевральные или ноющие боли в грудной клетке говорят о воспалительном процессе в париетальной плевре, хотя получены убедительные данные о наличии «неспецифических ноцицепторов» в легких и других органах и их важной роли в возникновении висцеральной боли (А. Malliani, F. Lombardi, 1982; H. Blumberg и соавт., 1983). Небольшой плевральный выпот не оказывает значительного влияния на функцию легкого и может не давать клинической симптоматики.
Установление наличия плеврального выпота с помощью физикальных методов обследования, как правило, не вызывает затруднений. Укорочение легочного тона, ослабление голосового дрожания и дыхания на пораженной стороне с большой степенью вероятности свидетельствуют о наличии значимого количества жидкости в плевральной полости.
Следующим этапом является рентгенологическое исследование, позволяющее уточнить наличие, локализацию выпота и состояние органов средостения. Локализация выпота не имеет решающего значения, хотя правосторонняя локализация более характерна для застойных выпотов. При массивных выпотах важно обращать внимание на положение средостения. При опухоли или инфильтративном процессе в средостении оно будет зафиксировано. Смещение в сторону выпота указывает на то, что поражено легкое на стороне выпота и смещение происходит из-за его гиповентиляции или ателектаза.
|
Причины плеврального выпота |
|||
|
Основные |
Менее частые |
||
| Транссудаты | Сердечная недостаточность | Нефротический синдром Цирроз Перитонеальный диализ Микседема |
|
| Экссудаты воспалительные(инфекционные) | Парапневмонический выпот Туберкулез |
Поддиафрагмальный абсцесс Вирусная инфекция Грибковые поражения |
|
| Экссудаты воспалительные (неинфекционные) |
Эмболия легочной артерии | Коллагенозы Панкреатит Реакция на лекарства Асбестоз Синдром Дресслера Синдром «желтых ногтей» |
|
| Опухолевый экссудат | Метастазы рака Лимфома |
Мезотелиома Синдром Мейгса |
|
| Гемоторакс | Травма | Спонтанный (нарушения гемостаза) |
|
| Хилоторакс | Лимфома Карцинома Травма |
Лимфангиолеомиоматоз | |
При массивном плевральном выпоте, как правило, выроятно метастатическое поражение плевры, что, однако, встречается и при застойных выпотах, реже при туберкулезных. Во всех случаях затемнения заднего реберно-диафрагмального синуса или нечеткости контура диафрагмы следует прдположить наличие выпота в плевральной полости.
Иногда по неизвестным причинам значительное количество жидкости скапливается над нижней долей легкого, не переходя в реберно-диафрагмальный синус. Такой тип скопления называется наддиафрагмальным, или базальным, плевральным выпотом.
|
Исследование плевральной жидкости |
||
|
Транссудат |
Экссудат |
|
| Внешний вид жидкости | Прозрачная | Прозрачная, мутная, кровянистая |
| Белок Абсолютное количество |
<30 г/л | >30 г/л |
| Соотношение плевральная жидкость/ плазма | < 0,5 | >0,5 |
| ЛДГ Абсолютное количество Соотношение плевральная жидкость/плазма |
<200 ЕД/л <0,6 |
>200 ЕД/л >0,6 |
| Уровень глюкозы | >3,33 ммоль/л | Вариабелен, чаще <3,33 ммоль/л |
| Лейкоциты(полиморфноядерные) | <50% | Обычно > 50% при остром воспалении |
| Количество эритроцитов | < 5000 в 1 мл | Вариабельно |
Рентгенологически определяется высокое стояние купола диафрагмы, а в случае левосторонней локализации нижняя граница легкого расположена дальше, чем обычно, от воздушного пузыря в желудке. Клинико-рентгенологически заподозрить базальный выпот важно, так как это является показанием для обследования больного в положении лежа.
Возможно атипическое расположение выпота в силу изменения эластической тяги пораженного участка легкого. Атипическое скопление жидкости свидетельствует о том, что помимо воспаления плевральных листков имеется заболевание паренхимы.
В результате спаечного процесса жидкость может осумковаться в любом месте между париетальной и висцеральной плеврой или в области междолевых щелей. Чаще всего это связано с острыми бактериальными инфекциями. Осумкованная жидкость в междолевых щелях обычно видна в боковых проекциях и напоминает двояковыпуклую линзу.
Иногда для дифференциации осумкованного плеврального выпота, ателектаза и инфильтрата легочной ткани можно использовать УЗИ, которое также может помочь в определении места торакоцентеза при осумкованных и небольших выпотах.
При наличии горизонтального уровня жидкости на рентгенограммах проводится дифференциальная диагностика между осумкованным пиопневмотораксом, гидропневмотораксом и периферическим абсцессом легкого. Горизонтальный уровень жидкости в плевральной полости свидетельствует о наличии воздуха.
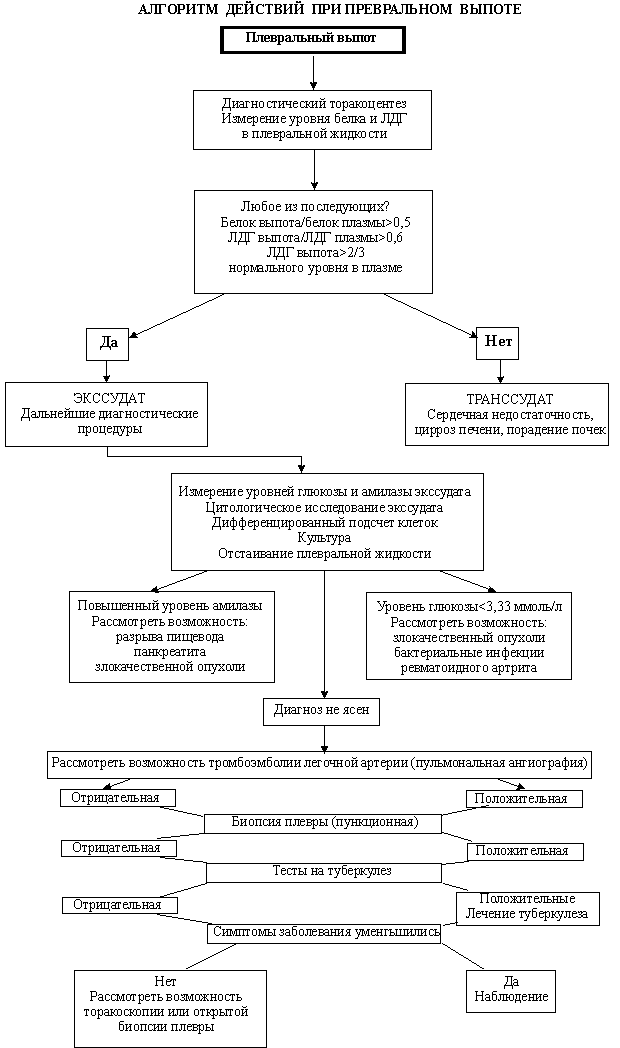
Следующим, пожалуй самым важным, этапом диагностики является торакоцентез, который выполняется для дифференциации экссудативного и транссудативного выпота, исследования клеточного состава плевральной жидкости и оценки состояния легкого.
Диагностический торакоцентез показан больным, у которых толщина слоя жидкости на рентгенограммах в положении лежа на боку больше 10 мм или имеется осумкованный плевральный выпот, выявленный с помощью УЗИ (Р.У. Лайт , 1986).
В зависимости от цвета, прозрачности, относительной плотности, биохимического и цитологического состава выделяют два вида плевральных выпотов — экссудат и транссудат. Помимо этого в плевральной полости возможно скопление крови (гематоракс) и лимфы (хилоторакс).
Транссудат представляет собой прозрачную, желтоватого цвета жидкость с относительной плотностью 1,015, низким содержанием белка (менее 20 г/л) и отсутствием наклонности к свертыванию при длительном стоянии. Для транссудата характерна низкая, менее 1,6 ммоль/(л.г), активность лактатдегидрогеназы (ЛДГ), отношение ЛДГ выпота к ЛДГ сыворотки крови ниже 0,6, отношение белка выпота к белку сыворотки крови ниже 0,5 ( В.Г.Григорян и соавт., 1986).
Накопление транссудата в плевральной полости называется гидротораксом.
Большинство транссудатов и некоторые экссудаты прозрачны, соломенно-желтого цвета, невязкие и не имеют запаха.
Повышенная вязкость плевральной жидкости свидетельствует о повышенном содержании гиауроновой кислоты, что встречается у больных с мезотелиомой плевры.
Красноватая или коричневатая плевральная жидкость свидетельствует о наличии в ней крови, соответственно свежей или длительно находившейся там.
Мутный плевральный выпот, имеющий молочную окраску, свидетельствует о наличии хилоторакса. Иногда хилезный выпот может быть принят за эмпиему плевры. Центрифугирование жидкости из плевральной полости вносит ясность. Хилезный выпот остается мутным.
Хотя вид плевральных выпотов и не имеет решающего диагностического значения, тем не менее после разграничения их на экссудат и транссудат можно представить примерный спектр этиологической принадлежности.
I. Транссудативные плевральные выпоты
1) застойная сердечная недостаточность;
2) тромбоэмболия легочной артерии;
3) нефротический синдром (гломерулонефрит, липоидный нефроз, амилоидоз почек и др.);
4) цирроз печени;
5) микседема.
II. Экссудативные плевральные выпоты
Вследствие новообразований
1) первичная опухоль плевры (мезотелиома);
2) метастатические опухоли;
3) лейкозы.
Вследствие инфекционных заболеваний
1) туберкулез;
2) бактериальные инфекции;
3) грибковые инфекции;
4) паразитарные инфекции.
Вследствие заболеваний желудочно-кишечного тракта
1) ферментогенные (панкреатогенные);
2) внутрипеченочный или поддиафрагмальный абсцесс.
Вследствие диффузных заболеваний соединительной ткани
1) ревматизм;
2) ревматоидный артрит;
3) системная красная волчанка.
Вследствие других заболеваний и состояний
1) постинфарктный синдром Дресслера;
2) синдром Мейгса;
3) синдром «желтых ногтей» (врожденная гипоплазия лимфатической системы; характерны утолщенные и искривленные ногти желтого цвета, первичный лимфатический отек, реже экссудативный плеврит, бронхоэктазы),
4) лекарственная аллергия;
5) асбестоз;
6) уремия;
7) травмы грудной клетки;
8) гематоракс;
9) хилоторакс.
Следующий этап — исследование клеточного состава плевральной жидкости. Геморрагический экссудат содержит значительную примесь свежих и измененных эритроцитов, и трактовка его с диагностической точки зрения представляет наибольший интерес. По данным И.Б. Леви, А.А. Литвинова (1976), при геморрагических выпотах опухолевые процессы диагностируют у 71% больных, а при прогрессировании опухолевого процесса геморрагический выпот может встречаться у 78% больных.
Присутствие нейтрофилов в плевральной жидкости, клеток, включающихся в реакцию на острое воспаление, характерно для пневмонии, поддиафрагмального абсцесса. Если они составляет более 20% всего клеточного состава, то это является показательным для ранних стадий туберкулеза.
Присутствие 6 — 10% эозинофилов достаточно для диагностики эозинофильного выпота. Эозинофильный экссудат может встречаться при пневмониях, диффузных заболеваниях соединительной ткани, глистных инвазиях, грибковых заболеваниях, травмах (П.Г. Калмыков, Г.С. Первомайский, 1979; I.F.Beekman и соавт., 1974).
Наличие эозинофилов в парапневмоническом выпоте является хорошим прогностическим признаком. Такой выпот редко инфицируется. В большинстве случаев эозинофилия плевральной жидкости обусловлена присутствием воздуха или крови в плевральной жидкости (Р.У. Лайт , 1986).
Если в экссудативном плевральном выпоте более 50% лимфоцитов, это важный диагностический признак, позволяющий предположить наличие у больного туберкулеза или злокачественного заболевания.
Обнаружение клеток мезотелия в плевральной жидкости может иметь некоторое диагностическое значение. Присутствие мезотелиальных клеток для туберкулезных и парапневмонических выпотов нехарактерно.
Наибольшее число мезотелиальных клеток наблюдалось при инфаркте легкого, сердечный и почечной недостаточности (W. Matzel, 1970).
Макрофаги, базофилы и плазматические клетки, выявленные в плевральной жидкости, диагностического значения не имеют.
Использующиеся методики определения белков плевральной жидкости, таких как карциноэмбриональный антиген, орозомукоид, имеют диагностическое значение; однако использование их возможно далеко не в каждой лаборатории.
Биопсия плевры показана с целью диагностики злокачественного или туберкулезного плеврального выпота. Для получения патологического материала используют три вида биопсии плевры: торакоскопическую, операционную и пункционную. Гистологическое исследование биоптатов париетальной плевры позволяет верифицировать диагноз у 60-93% больных туберкулезным и 70% больных метастатическими плевритом (Н.С.Тюхин и соавт., 1984).
Торакоскопия применяется у тех больных, у которых в результате бронхоскопии, проведения анализа плевральной жидкости и биопсии плевры этиология плеврального выпота остается неясной.
Сканирование легких рекомендуется больным с плевральным выпотом, этиология которого не установлена после выполнения первоначальных диагностических исследований для исключения тромбоэмболии ветвей легочной артерии.
На основании опыта наших предшественников, данных литературы и собственной практики мы попытались коротко изложить основные моменты подхода к установлению этиологической принадлежности плеврального выпота.
Однако, несмотря на обилие методов, установление этиологической принадлежности плеврального выпота представляет определенную трудность и в известной степени зависит от опыта, интуиции практического врача и диагностических возможностей лечебного учреждения.
Литература:
Нет никакого сомнения в том, что типичная и единая клинико-лучевая картина плеврального выпота (ПВ) маловероятна. Подобное «откровение» может ошеломить молодого коллегу, но не весьма опытного специалиста, имеющего близкое отношение к данной патологии. И как это становится ясно с годами, разнообразие ПВ может обусловливаться таким процессом, как осумкование с особенностью расположения, распространенности, генеза, течения и лечения.
Классификация осумкованных плевритов (ОП) по локализации:
В то же время мы должны понимать, что плеврит – это не нозология, а клинико-рентгенологический синдром для обозначения последствий любого патологического процесса, протекающего с поражением плевры, появлением осумкования, плевральной болью, трением листков плевры и др. В зависимости от локализации осумкования, формы и стадии развития симптомы могут различаться. Междолевые ОП редко проявляют признаки, возможно, потому, что они часто развиваются при сердечной недостаточности, и тогда этот процесс является не плевритом, а осумкованным ПВ.
Французский клиницист Лассега (XIX в.) утверждал: «Плеврит – это не есть заболевание плевры». То есть плеврит как таковой – это типичный симптом инфекции или инфаркта легких, но может развиваться при злокачественном новообразовании, системных заболеваниях соединительной ткани.
Если говорить более широко о плевральной транссудации или экссудации, то уместно применять понятие ПВ, который может быть осложнением более 70 заболеваний, его частота занимает 3,3% в структуре заболеваемости. При этом следует помнить, что при транссудате нет патологии плевры (сердечная, почечная и печеночная недостаточность, саркоидоз, гипотериоз), а при экссудате – есть.
ПВ встречаются у 5-10% больных терапевтического профиля, может встречаться на стыке специальностей, характерны частые диагностические ошибки из-за однотипности реакции плевры. Однако аккумуляцию гнойного экссудата (эмпиема) или крови в виде гемоторакса следует считать отдельными состояниями.

Рис. 1. Компьютерная томография органов
грудной клетки (КТ ОГК): а – осумкованный паракостальный плеврит справа; б – массивное скопление жидкости у наружной части грудной клетки

Рис. 1. Компьютерная томография органов
грудной клетки (КТ ОГК): а – осумкованный паракостальный плеврит справа; б – массивное скопление жидкости у наружной части грудной клетки
Не будет ошибкой сказать, что ОП, как полные, так и неполные, – это непревзойденные «художественные полотна» в лучевом изображении и не менее загадочные – в клиническом. Диагностическое впечатление от этих «полотен» очень сильное, порой по закону контрастов (рис. 1, 2), так как клиническое понимание ОП зависит от их расположения, степени отграничения и времени его возникновения. Более того, в поисках ПВ при паракостальном осумковании приходится порой проводить неоднократные плевральные пункции, которые не всегда дают положительный результат, так как «организация выпота преобладает над экссудацией».

Рис. 2. Паракостально, широким основанием к грудной стенке примыкает полуовальная фокусная тень, образующая «тупые углы»

Рис. 2. Паракостально, широким основанием к грудной стенке примыкает полуовальная фокусная тень, образующая «тупые углы»
Итак, осумкование – один из возможных вариантов эволюции острого серозного (экссудативного) парапневмонического плеврита, туберкулеза, перисцисуритов, осложнений спонтанного и лечебного пневмоторакса, операции по поводу резекции легкого, травмы грудной полости . Следует, правда, отметить, что развитие ОП возможно двумя путями: при наличии старых сращений плевры, когда содержимое образуется между этими спайками и не сообщается с остальной плевральной полостью; второй вариант развития – плеврит, который осумковывается по мере своего формирования и скопления выпота, ограничивась новыми сращениями.

Рис. 3. КТ ОГК: левое легкое уменьшено в объеме с замещением паренхимы фиброзной тканью с множественными осумкованными полостями, заполненными воздухом; средостение смещено влево; правое легкое увеличено с множественными субплевральными гиподенсивными тонкостенными полостями и перифокальными линейными фиброзными тяжами

Рис. 3. КТ ОГК: левое легкое уменьшено в объеме с замещением паренхимы фиброзной тканью с множественными осумкованными полостями, заполненными воздухом; средостение смещено влево; правое легкое увеличено с множественными субплевральными гиподенсивными тонкостенными полостями и перифокальными линейными фиброзными тяжами
Основой процесса отграничения является отложившийся на плевральных листках фибрин, организующийся благодаря его высокой пластичности. Сложный ход плевральной капиллярной щели, охватывающей все легкое и проникающей между его долями до места отхождения долевых бронхов, способствует осумкованию выпота. Листки прорастают соединительной тканью, развиваются сращения, захватывающие большую или меньшую поверхность плевральной полости. Со временем вновь образованная соединительная ткань приводит к развитию плеврогенного склероза (цирроза) легкого, фиброторакса у места осумкования (рис. 3).
В отличие от плевральных шварт (наслоений), признаками ОП является резко ослабленное дыхание и снижение голосового дрожания. Поэтому при наличии у больного «плевральных наслоений», длительного субфебрилитета и указания в анамнезе на лечение с использованием искусственного пневмоторакса или экономной резекции, перенесенного экссудативного плеврита, а также спонтанного пневмоторакса следует произвести плевральную пункцию, которая обычно противопоказана при ателектазе. Нами неоднократно подтверждалось, что диагноз осумкованной эмпиемы может быть поставлен только после пункции плевры .
Осумкование экссудата отнюдь не означает, что всасывание не происходит, хотя интенсивность его уменьшается, а иногда может и вовсе прекратиться. В одних случаях всасывание экссудата продолжается, и организм избавляется от него, плевральные листки сближаются и срастаются. На них остаются отложения фибрина, сращения различной протяженности, в большей или меньшей мере нарушающие функцию легкого.
В условиях длительной этиотропной и патогенетической терапии наблюдается инволюция и того процесса, который был первопричиной развития экссудативного плеврита (пневмония, бугорковая диссеминация, абсцесс и др.).
Таким образом, перспектива эволюции, например, парапневмонического ПВ, может быть малоутешительна (отсутствие своевременного лечения и торакоцентеза) и при полном его развитии имеет три стадии, которые не четко отграничены, так как постепенно переходят одна в другую .
Первая стадия называется экссудативной стадией и характеризуется быстрым накоплением стерильной жидкости в плевральной полости в ответ на воспаление плевры. Это результат процесса, протекающего в легких и ведущего к увеличению проницаемости капилляров висцеральной плевры. То есть имеется переход воспалительного отека с легочной ткани на плевру. На этой стадии формирования парапневмонического плеврита сколько-нибудь значительной инвазии в плевральную полость инфекционного агента, являющегося возбудителем пневмонии, обычно не происходит и экссудат может оставаться стерильным. Плевральная жидкость на этой стадии заболевания характеризуется низким числом лейкоцитов и уровнем лактатдегидрогеназы (ЛДГ), содержание же глюкозы и величина рН находятся в пределах нормы . Как правило, в этих случаях ПВ клинически себя никак не проявляет и диагностируется только при рентгенологическом исследовании, при котором чаще обнаруживают небольшую облитерацию реберно-диафрагмального синуса.
Если на данной стадии заболевания, не осложненного ПВ, начать адекватную антибиотикотерапию, то объем ПВ перестанет увеличиваться и не будет необходимости в дренировании.
При отсутствии этиотропной антибиотикотерапии бактерии из близлежащего легочного инфильтрата могут проникнуть в плевральную жидкость, и тогда наступает вторая, осложненная, фиброзно-гнойная стадия поражения плевры. Эта стадия характеризуется накоплением плевральной жидкости с большим количеством полиморфноядерных лейкоцитов, бактерий и детрита. Одновременно висцеральная и париетальная плевра пораженного участка покрываются сплошной пленкой фибрина. Для этой стадии характерно образование спаек и осумкование выпота. Безусловно, эти спайки предотвращают распространение эмпиемы, но одновременно затрудняют дренирование плевральной полости. По мере прогрессирования процесса рН плевральной жидкости и содержание в ней глюкозы снижаются, а уровень ЛДГ увеличивается .
Последняя, третья стадия называется стадией организации. В этот период наблюдаются пролиферация фибробластов и выход их в экссудат с париетальной и висцеральной плевры. В результате образуется неэластическая оболочка, называемая плевральной швартой. Эта неэластическая шварта покрывает легкое, и оно перестает функционировать. На данной стадии экссудат становится густым, и если лечение больного не проводится, то может произойти спонтанное дренирование гнойной жидкости через грудную стенку или в легкое с образованием бронхоплеврального свища (рис. 4).

Рис. 4. Морфологическая схема осумкованного гнойного плеврита

Рис. 4. Морфологическая схема осумкованного гнойного плеврита
В лучевом изображении плевриты также имеют три вида: диафрагмальный, диафрагмально-костальный и тотальный плеврит.
Эмпиема вообще и осумкованная в частности может образоваться не только в ходе процесса в легких, например, в результате послеоперационной инфекции . Небольшой процент эмпием является результатом плохой стерильности во время проведения торакоцентеза. Почти всегда инфицируются ПВ, связанные с перфорацией пищевода. Эмпиема часто образуется и у больных с ПВ ревматоидной этиологии. Полагают, что развитие эмпиемы при этом связано с образованием бронхоплеврального свища через некротизированные субплевральные лимфатические узлы . Таким образом, осумкованные (частично или ограниченно) эмпиемы образуются в небольшой (остаточной) плевральной полости, когда плевральные листки предварительно срослись между собой на большом протяжении или же при быстрой облитерации полости плевры под влиянием воспалительного процесса, до того момента, пока накопилось большое количество экссудата. Осумкованные эмпиемы чаще встречаются в тех случаях, когда развиваются на почве существующего до того экссудативного плеврита, когда гнойный процесс передается по соседству (без прорыва) из легких к плевре или при остаточных плевральных полостях по различным причинам.
Вследствие указанного процесса в зависимости от расположения возможно образование междолевого плеврита, парамедиастинального (между внутренней поверхностью легкого и средостением), костального, апикального и базального (диафрагмального) плеврита. По мнению клиницистов, междолевой и медиастинальный плевриты представляют наибольшее своеобразие течения и трудности для диагностики. В литературе приводятся различные схемы междолевых ОП без указаний особенностей их этиологии, частоты локализации в тех или иных участках междолевых щелей. И если в прошлом в большинстве случаев описывали выпот, осумкованный в нижней части главной междолевой щели, то в 1980 г. Л. С. Розенштраух и соавт. констатировали, что из 5 000 исследований они ни в одном из случаев не наблюдали изолированного интерлобита подобной локализации. В настоящее время, однако, диагностика междолевого плеврита при правильно проведенном лучевом исследовании не представляет трудности (рис. 5).
Рис. 5. Междолевой плеврит справа: прямая и правая боковая проекция
Рис. 5. Междолевой плеврит справа: прямая и правая боковая проекция
Междолевые ОП чаще всего можно ошибочно принять за ателектаз или пневмонию средней доли. Для их дифференцирования принимают во внимание, прежде всего, основное заболевание, которое вызвало появление гнойного плеврита (абсцесс, эхинококкоз, туберкулезная каверна). Рентгенологическое исследование в боковом или в лордотическом положении Флейшнера дает при междолевых выпотах веретенообразную, линейную или клиновидную тень с заостренными контурами и резко очерченными границами с обеих сторон. При ателектазе тень однородна, треугольной формы, вершиной упирается в гилюс (корень). Соседние легочные поля более прозрачны и являются выражением компенсаторной эмфиземы. Средостение, правда, не всегда, смещено в сторону ателектаза. Бронхоскопия и КТ ОГК устанавливают полную обтурацию бронха (туберкулез, карцинома). Доля легкого уменьшена в объеме.
При пневмонии средней доли прослушивается характерное бронхиальное дыхание с соответствующей крепитацией в зависимости от фазы пневмонии. Рентгенологическая картина почти не отличается от картины при ателектазе. Однако при пневмонии объем легочной доли не уменьшен, а даже может быть увеличенным, что объясняется экссудативным легочным процессом. Диагностическая трудность преодолевается надежнее всего после быстрого рассасывания пневмонического инфильтрата.
В спорных случаях сомнения разрешаются боковой томографией, КТ ОГК и УЗИ.
Рентгенологическая картина костального ОП вначале часто повторяет картину свободного костального экссудативного плеврита. Разницей является положение верхней его границы, которая принимает более отвесное направление. Контуры этой границы становятся значительно более четкими. Боковая проекция указывает, что жидкость большей частью собирается в задних или задне-боковых участках грудной клетки.
На рентгенограммах в этих положениях больных видно, что передняя граница тени теряет вогнутое очертание и приобретает вид почти прямой линии. Кроме того, для дифференцирования костального ОП следует исходить из трех условно типичных видов плевритов, которые характерны для свободного скопления жидкости в плевральной полости: тотальный, субтотальный и малый (рис. 6).
Рис. 6. А – осумкованный плевральный экссудат; б – правосторонний экссудативный плеврит (сзади), хорошо выражена линия Дамуазо; в – правосторонний диафрагмальный плеврит, фиксация внутренней половины диафрагмы; г – плеврогенный цирроз левого легкого с резким спадением грудной клетки (фиброторакс) и смещением сердечно-сосудистой тени влево, высокое стояние диафрагмы; д – оcyмкованный левосторонний паракостальный плеврит, диафрагмальная спайка; е – междолевой ОП справа; ж – искусственный пневмоторакс справа с полным разрешением процесса; з – двусторонний пневмоторакс: «висячие» корни
Рис. 6. А – осумкованный плевральный экссудат; б – правосторонний экссудативный плеврит (сзади), хорошо выражена линия Дамуазо; в – правосторонний диафрагмальный плеврит, фиксация внутренней половины диафрагмы; г – плеврогенный цирроз левого легкого с резким спадением грудной клетки (фиброторакс) и смещением сердечно-сосудистой тени влево, высокое стояние диафрагмы; д – оcyмкованный левосторонний паракостальный плеврит, диафрагмальная спайка; е – междолевой ОП справа; ж – искусственный пневмоторакс справа с полным разрешением процесса; з – двусторонний пневмоторакс: «висячие» корни
В этой связи нельзя не согласиться с рентгенологами, у которых существует другая точка зрения, заключающаяся в том, что костальные ОП могут вызывать большие дифференциально-диагностические затруднения, так как они дают разнообразную рентгенологическую картину . На обычной рентгенограмме ОГК осумкованный ПВ, в том числе костальный, похож на массу, снижающую прозрачность и прилежащую к плевре, а бронхи у таких больных не просматриваются .
Понижение прозрачности легочного поля наблюдается и при плащевидном (костальном) плеврите, что обусловлено не только фибринозными массами, но и уменьшением объема легкого и уплотнением его паренхимы в связи с наличием воспалительного процесса. При таких плевритах изменения нередко переходят с медиастинальной плевры на перикард, в результате чего развивается сухой или выпотной, в основном фибринозный перикардит. При благоприятном течении фибринозные массы полностью рассасываются и прозрачность легочного поля восстанавливается (рис. 7).
Рис. 7. Плащевидный плеврит окружает все легочное поле, заходит обычно в междолевую щель, покрывает верхушку и медиастинальный край легкого. Примерно в трети случаев плеврит бывает парциальным
Рис. 7. Плащевидный плеврит окружает все легочное поле, заходит обычно в междолевую щель, покрывает верхушку и медиастинальный край легкого. Примерно в трети случаев плеврит бывает парциальным
Верны ли, а точнее, однозначны ли эти версии, судить нетрудно, так как правы могут быть все, что зависит от профессионализма и той или иной клинико-рентгенологической ситуации. В действительности не так уж важно, что именно говорят спикеры, но важно понимать патофизиологические механизмы образования плеврального осумкования и его клинико-рентгенологического представления.
Во всяком случае, несомненно, что костальные ОП по своему характеру часто являются гнойными, поэтому точная локализация их имеет значение для уточнения точки для торакоцентеза. В этой связи рентгенолог должен давать исчерпывающие данные о локализации костальных ОП, что требует зачастую неоднократного многоосевого исследования или УЗИ, хотя у некоторых больных пневмонией уже при первичной диагностике (возможно, запоздалой) может наблюдаться осумкованный ПВ. В то же время у многих больных с обширным рентгенологическим осумкованием ПВ практически нет и он не гнойный.
Возвращаясь к костальной локализации осумкования, следует отметить, что версия во всех ее частях соответствует действительности, так как в результате сращений между листками плевры выпот может оказаться осумкованным у внутренней поверхности ребер в любом отделе плевральной полости. Тут же следует отметить, что костальные ОП располагаются чаще всего вдоль латеральной или задней стенки грудной клетки.
Так или иначе, но ОП, и гнойные в частности, диагностировать непросто. Поэтому следует понимать, что осумкованная эмпиема представляет собой остаточную камеру, заполненную экссудатом после обычного плеврита, течение которого закончилось неполной облитерацией плевры . В то же время гнилостный плеврит не склонен к осумкованию.
Часто по обычной обзорной передне-задней рентгенограмме ОГК трудно дифференцировать осумкованный ПВ и инфильтраты в периферических отделах паренхимы легкого. Именно в этот момент врач должен вспомнить аксиому: если рентгенограмма выглядит непонятно – думайте о поражении плевры. С большей определенностью эту дифференциально-диагностическую проблему может разрешить УЗИ, с помощью которого выявляется осумкованный ПВ объемом даже 5 мл.
Пристеночно расположенные ограниченные эмпиемы иногда трудно отличить от легочного абсцесса, расположенного на периферии. В некоторых случаях оба заболевания могут существовать одновременно. При эмпиеме отсутствует мучительный кашель, сопровождаемый выделением большого количества гнойной, зловонной мокроты, характерной для абсцесса легкого. Тень при осумкованной эмпиеме имеет форму удлиненного элипса, но может быть и овальной. Она всегда располагается пристеночно, не отделяясь от грудной стенки при вращении больного во всех направлениях (полипозиционно). Внутренняя стенка полости имеет резкие очертания и выпячивается к легкому. При абсцессе легкого тень кругловатая или овальная, с толстыми стенками и горизонтальным уровнем жидкости. При вращении больного она всегда остается в ткани легкого. Исключительно трудно дифференцировать ограниченную гнойную полость с бронхоплевральной фистулой от пристеночно расположенного абсцесса легкого или от большой туберкулезной каверны. Ранее торакотомия в состоянии была решить эту диагностическую задачу, но сегодня дело облегчает КТ ОГК.
При распознавании парамедиастинальной эмпиемы используют основной признак: при рентгенологическом исследовании и КТ ОГК тень сохраняет свою связь со средостением при всех положениях больного. Тень бывает треугольной или элипсовидной формы, с ясно ограниченными и выпуклыми внешними границами. При пневмомедиастинуме тень слегка перемещается латерально и остается между легким и органами средостения. Однако сегодня такой инвазивный метод, как пневмомедиастинум, может быть заменен более информативным – КТ ОГК. И действительно, КТ ОГК дает наиболее точную как качественную, так и количественную характеристику ПВ. Наличие возможности проведения денситометрии, то есть измерения плотности различных структур, в значительной степени облегчает дифференциальную диагностику ПВ от других патологических процессов, так как плевральная жидкость имеет определенные денситометрические показатели (OHU ± 1,8 HU), которые существенно отличаются от плотности мягкотканых структур (> 35MU).
Значительные диагностические трудности возникают при наличии осумкованных (капсулированных, ограниченных) междолевых плевритов. Характер диагностических ошибок междолевых плевритов несколько иной, более разнообразен и зависит от того, в какой из междолевых щелей расположен осумкованный экссудат. Без рентгенологического обследования нельзя диагностировать осумкованный междолевой плеврит, его можно только подозревать, так как рентгенологическая картина плевритов отражает полную картину локализации процесса, его распространенность, колическтво ПВ, состояние легких и смещение ОГК.
Наиболее выраженную рентгенологическую картину дает правосторонний междолевой плеврит, осумкованный в передней междолевой щели.
Осумкованная эмпиема верхушки легкого возникает чаще всего после коллапсотерапии, после внеплеврального пневмоторакса или после частичной резекции верхней доли легкого. В этих случаях диагноз установить нетрудно. Если эмпиема верхушки является следствием других причин, ее можно часто спутать с абсцессом или раком верхней доли. Дифференциальный диагноз этих состояний основывается на том, что эмпиема связана с грудной стенкой, выпячивается к легкому, границы ее четко очерчены. При продолжительном наблюдении легочное затемнение не нарастает, за исключением тех случаев, когда увеличивается количество экссудата. При неясных случаях необходима паренхиматозная биопсия и плевральная пункция, которую производят в I или II межреберном пространстве сзади, на уровне spinae scapulae, между лопатками.
Базальная (диафрагмальная) эмпиема иногда трудно отличима от поддиафрагмального абсцесса. Одним из наиболее надежных способов распознавания их в недавнем прошлом был диагностический пневмоторакс. Если тень остается над диафрагмой, дело касается плевральной эмпиемы, если же тень находится под диафрагмой – имеется поддиафрагмальный абсцесс, который на сегодня должен быть выявлен при УЗИ и КТ ОГК .
Дифференциально-диагностическое значение имеет одновременное наличие сращений в области френико-костального синуса соответствующей стороны, что говорит в пользу ОП, который может прорываться в бронх с последующим самоизлечением. При серозном ОП возможно рассасывание экссудата. Остающиеся на месте выпота шварты дают слабые тени с нерезкими очертаниями. Клинические проявления отсутствуют.
Однако осумкование следует подозревать и в том случае, если через 48 ч после начала соответствующей антибиотикотерапии клиническое состояние больного не улучшается. При выявлении путем УЗИ одной осумкованной полости следует произвести УЗИ всего гемиторакса, так как часто встречаются множественные осумкования. После выявления осумкованного ПВ больному следует сразу же произвести торакоцентез, поскольку, если сделана отметка границы осумкованного ПВ на коже и больной отправлен в палату, с тем чтобы позднее произвести плевральную пункцию, то граница плевральной жидкости по отношению к коже больного может измениться, когда больной примет другое положение. При обнаружении нескольких осумкованных полостей следует произвести диагностическую пункцию во всех участках с аспирацией из них жидкости, так как последняя по своему составу может быть неодинаковой в различных полостях .
Все формы ОП сопровождаются лихорадкой, плевральными болями и другими общими расстройствами, менее выраженными по сравнению с общим диффузным поражением правой и левой плевры. Ввиду нечеткости местных симптомов при ОП может создаться неясная клиническая картина общей инфекции. Это лишний раз подтверждает необходимость широкого применения рентгенологического исследования ОГК (КТ) и УЗИ плевральных полостей у всех лихорадящих больных с неясным источником лихорадки.
Несмотря на грубое морфологическое поражение плевры при осумковании, врач должен смотреть на этот процесс со всесторонней терапевтической корректностью: один неосторожный шаг – и вы можете потерять не только плевру, но и легкое. ОП туберкулезной этиологии могут длиться годы и даже десятилетия при относительном клиническом благополучии, аналогично – и междолевые осумкования различного генеза. Серозный экссудат со временем в результате жировой дистрофии клеточных элементов трансформируется в так называемый холестериновый. Количество холестерина в экссудате при этом не зависит от его уровня в крови. В анализах пунктата, полученного из таких полостей, кроме большого количества холестерина обнаруживают жирно перерожденные лейкоциты.
Лечебные мероприятия в отношении ОП:
- общая тактика лечения основывается, во-первых, на:
- лечении основного заболевания:
- при наличии выпота, видимого на рентгенограмме и УЗИ, высотой 10 мм и более показаны плевроцентез, эвакуация жидкости (с ее последующим цитологическим, бактериологическим и биохимическим исследованиями) и введение фибринолитических средств в плевральную полость;
- обезболивающие мероприятия;
- бинтование грудной клетки эластическими бинтами;
- парацетамол 0,65 г 4 раза в сутки;
- при отсутствии эффекта, сильной боли и сухом кашле – кодеин 30 мг/сут;
- лечении основного заболевания:
- лечение плеврита, осложнившего пневмонию, проводят антибактериальными препаратами: фторхинолоны (левофлоксацин) или защищенные β-лактамы (амоксициллин + клавулановая кислота, ампициллин + сульбактам) в сочетании с макролидами.
Исходы парапневмонических ПВ и эмпием плевры – полная ремиссия (80%), частичная ремиссия (10%) и развитие осложнений (10%). Осложнениями эмпиемы плевры являются: переход в хроническую форму, развитие бронхоплевральных и плеврокожных свищей; флегмона стенки грудной клетки; развитие гнойного перикардита или сепсиса. К поздним осложнениям длительно существующей эмпиемы плевры относят формирование пиоторакс-ассоциированной злокачественной лимфомы. Как правило, после перенесенной эмпиемы плевры практически у каждого больного сохраняются выраженные плевральные изменения с последующим прогрессированием процесса в плеврогенный цирроз.
Список литературы
1. Семененков Ю. Л., Горбулин А. Е. Плевриты. Киев: Здоров’я, 1983.184 с.
3. Лайт Р. У. Болезни плевры. Пер. с англ. Е. Федорова. Медицина, 1986. 187 с.
4. Ходош Э. М. Этиология плеврального выпота: диагностический алгоритм. Пульмонология. 2008. № 5. С. 114-118.
7. Фанарджян В. А. Рентгенодиагностика. Государственное издание медицинской литературы, 1951.572 с.
Осумкований плеврит
Е.М. Ходош
Харківська медична академія післядипломної освіти, Міська клінічна лікарня № 13 Харківської міської ради
Резюме
Осумкований плеврит відноситься до найбільш важких форм плевритів, що вимагає негайного лікування. При його наявності хвороба може призвести до деформуючого бронхіту, бронхоектазів, бронхіального свищу, плеврогенного цирозу і серцево-легеневої недостатності.
Ключові слова: плеврит, плевральний випіт, осумкування, транссудат, ексудат, емпієма.
Encysted pleurisy
E.M. Khodosh
Kharkiv Medical Academy of Postgraduate Education, Kharkiv City Clinical Hospital № 13
© РУСЕЦКАЯ М.О., 2011
ИЗМЕНЕНИЕ ЛАБОРАТОРНЫХ ПОКАЗАТЕЛЕЙ ПРИ ОСТРОМ, ПОДОСТРОМ И ХРОНИЧЕСКОМ ПЛЕВРИТАХ
РУСЕЦКАЯ М.О.
У О «Витебский государственный ордена Дружбы народов медицинский университет»,
кафедра госпитальной хирургии
Резюме. Эмпиема плевры — наиболее тяжелое осложнение пневмонии, развивающееся при инфицировании парапневмонического плеврита. Социальную значимость заболеванию придают длительные сроки госпитализации пациентов, высокий уровень инвалидности, высокий уровень потери трудоспособности пациентов. В представленной статье рассмотрены результаты обследования 99 пациентов, находившихся на лечении в отделении торакальной хирургии ВОКБ с ноября 2008 по июль 2011 года по поводу острого, подострого и хронического воспалительного процесса плевры. Все пациенты разделены на три группы: первая группа — лица с острым процессом (пара- и метапневмонический плеврит), вторая группа — лица с подострым процессом (плеврит в стадии организации), третья группа—лица с хроническим течением заболевания (фиброторакс). Проанализированы основные показатели общего и биохимического анализов крови (эритроциты, гемоглобин, лейкоциты, лейкоцитарная формула, СОЭ, глюкоза, мочевина, креатинин, билирубин, АсТ, АлТ, общий белок). Предпринята попытка установить взаимосвязь между степенью хронизации плеврита и изменением лабораторных показателей крови. Определены характерные лабораторные изменения у пациентов с подострым и хроническим вариантами течения воспаления плевры.
Ключевые слова: лабораторные анализы, острый, подострый, хронический воспалительный процесс.
При любом патологическом процессе, протекающем в организме, даже бессимптомном, наблюдаются изменения лабораторных данных, полученных от пациентов. Именно обнаружение изменений в общем и биохимическом анализах крови, анализах мочи позволяют своевременно заподозрить
Адрес для корреспонденции: 210020, г.Витебск, пр.Победы, д.5/2, кв.153. Тел.моб.: +375 (29) 714-62-
00, e-mail: marinarusetska@mail.ru -РусецкаяМ.О.
наличие заболевания и вовремя начать дообследование и лечение пациента.
В начальной стадии воспаления отмечаются минимальные значения лейкоцитоза с его последующим возрастанием, увеличение количества моноцитов. Увеличение количества моноцитов является одним из лабораторных признаков тяжело протекающих инфекционных процессов, в частности сепсиса. Процент нейтрофилов нормализуется или снижается за счет увеличения относительно-
го числа лимфоцитов. Сдвиг формулы влево увеличивается за счет появления юных форм, что является свидетельством активации иммунной системы. Прогностически неблагоприятным является усиление сдвига лейкоцитарной формулы влево, особенно на фоне увеличения количества юных форм нейтрофилов с продолжением возрастания лейкопении. Как правило, подобные состояния возникают при высокой патогенности возбудителя.
При дальнейшем течении заболевания с тенденцией к выздоровлению в общем анализе крови отмечаются снижение общего числа лейкоцитов с нормализацией количества ней-трофилов, уменьшением юных форм в лейкоцитарной формуле на фоне сохранения высокого относительного содержания лимфоцитов.
Повышение СОЭ указывает на увеличение соотношения в плазме крови белковых частиц крупных размеров (глобулинов) и мелких размеров (альбуминов). Защитные антитела относятся к классу глобулинов, поэтому их количество в ответ на попадание в организм вирусов, бактерий, грибков и т. д. резко возрастает, что сопровождается изменением соотношения белков крови .
При наличии тяжелого гнойного процесса развиваются токсические нефропатия и гепатит, что проявляется образованием в организме цитокинов, (интерлейкин-1, фактор некроза опухоли-а). Последние оказывают токсическое воздействие на почечную и печеночную паренхиму. Об этом свидетельствуют изменения в биохимических анализах крови и общем анализе мочи. Так, по данным Л.В. Рудницкого, продолжительное обнаружение мочевины на уровне 7,0 ммоль/л расценивается как проявление почечной недостаточности. Тот же автор указывает, что значения креати-нина у женщин выше 0,088 мкмоль/л можно расценивать как проявление почечной недостаточности . Появление в общем анализе мочи белка, гиалиновых цилиндров, эритроцитов у лиц, не имевших в анамнезе нефро-логической патологии, также может расцениваться как проявление почечной недостаточности. Повышение уровня печеночных трансаминаз, щелочной фосфатазы, у-ГТП, би-лирубинемии свидетельствует о развитии ток-
сического гепатита, что часто расценивается как хронический гепатит .
В то же время, данных о характере изменений в лабораторных данных, позволяющих дифференцировать острый, подострый и хронический воспалительные процессы плевральной полости, в доступной литературе нами не выявлено.
Цель работы — изучить изменения лабораторных показателей у пациентов с острым, подострым и хроническим воспалением плевры и определить клиническое значение этих изменений.
Методы
Проанализированы истории болезней 99 пациентов, находившихся на лечении в отделении торакальной хирургии Витебской областной клинической больницы по поводу воспалительных заболеваний плевры с ноября 2008 г. по июль 2011 г.
Все пациенты разделены на три группы: первая группа — лица с острым процессом (пара- и метапневмонический плеврит), вторая группа — лица с подострым процессом (плеврит в стадии организации), третья группа — лица с хроническим течением заболевания (фиброторакс). Характер плеврального содержимого подтвержден морфологическими исследованиями.
В общем анализе крови анализировали количество эритроцитов, лейкоцитов, гемоглобина, палочкоядерных и сегментоядерных ней-трофилов, моноцитов, лимфоцитов, эозинофи-лов, СОЭ. В биохимическом анализе крови изучали уровень мочевины, креатинина, общего белка, глюкозы, АсТ, АлТ, билирубина.
При анализе уровней мочевины и креа-тинина использовали литературные данные о том, что длительное обнаружение мочевины на уровне 7,1 ммоль/л и выше может свидетельствовать о наличии почечной недостаточности. При определении креатинина у лиц женского пола верхней границей нормы считали значение 0,088 мкмоль/л .
Статистическая обработка данных проводилась при помощи программного обеспечения Stati stica 6.0, StatSoft, Inc. с применени-
ем методов описательной статистики (медиана, квартили). При анализе в группах сравнения качественных критериев, которые можно представить в виде таблиц сопряженности 2 СЕ, при наличии хотя бы в одной ячейке частоты равной или меньшей 5, использовали непараметрический двухсторонний точный критерий Fisher. Уровень значимости p принимали равным 0,05. При значениях p<0,05 различия между исследуемыми показателями считали статистически значимыми.
Результаты и обсуждение
Из анализируемых показателей общего анализа крови статистически значимые отличия получены при изучении уровня лейкоцитов, лимфоцитов, моноцитов и СОЭ.
У пациентов первой группы с острым течением процесса уровень лейкоцитов был ниже по сравнению с пациентами второй и
третьей групп. Аналогичная картина отмечена при изучении СОЭ: у пациентов первой группы данный показатель был ниже (р<0,05) по сравнению с пациентами третьей группы.
У пациентов второй (с подострым течением процесса) и третьей группы (с хроническим течением процесса) лимфоцитопения встречалась достоверно чаще (р<0,05), чем у пациентов первой группы. Статистически значимое увеличение уровня моноцитов (р<0,05) отмечено во второй и третьей группах пациентов по сравнению с первой группой. После завершения острого процесса (I группа), различия в показателях лейкоцитов, лимфоцитов, моноцитов и СОЭ, становятся недостоверными, то есть данные показатели позволяют выделить только острый процесс и не позволяют дифференцировать между собой подострый и хронический.
Динамика изменения показателей общего анализа крови отражена в таблице 2.
В биохимическом анализе крови статистически значимо выше был уровень мочевины у пациентов первой группы по сравнению в пациентами второй (р<0,05) и третьей групп
Распределение пациентов по полу
Таблица 1
Нозология
Пол I группа II группа III группа
Мужской 7 31 42
Женский 11 1 7
Всего 18 32 49
Анализ показателей общего анализа крови
Таблица 2
Наименование Группы пациентов
показателя I группа II группа III группа
Лейкоциты 7,75 5,55-9,27 13,6* 10,2-16,5 10,7* 8,7-13,8
Лимфоциты 22,5 18,3-29,8 17* 11-23 19* 10,5-24
Моноциты 4,5 2-6,8 6,5* 4-13,5 7* 4-9,25
СОЭ 19,5 47 55,5*
13,8-37,3 37-63 47-63,7
Примечания: * — статистически значимое отличие от первой группы пациентов (р , <0,05)
Таблица 3
Анализ биохимических показателей крови
Наименование Группы пациентов
показателя I группа II группа III группа
Мочевина 7,3 5,7-7,5 5,3* 4,5-6,4 5,4* 4,2-6,5
Креатинин 0,09 0,084-0,098 0,084* 0,078-0,093 0,081* 0,071-0,087
Примечания: * — статистически значимое отличие от первой группы пациентов (рИзЫг <0,05).
Повышение мочевины в биохимическом анализе крови возможно связано с тем, что пациенты первой группы поступали в стационар, как правило, спустя 2-3 недели с момента начала заболевания, вследствие чего были выявлены лабораторные признаки токсической нефропатии. У пациентов второй и третьей групп ее развитие купировалось при стационарном лечении. Это же можно сказать и в отношении изменений уровня креатинина.
Нормализация уровней мочевины и кре-атинина у пациентов второй и третьей групп объясняется проведением интенсивной комплексной терапии и купированием явлений токсической нефропатии, приводящей к почечной недостаточности.
У пациентов второй и третьей групп по данным анализов наблюдалось более тяжелое и длительное течение заболевания по сравнению с пациентами первой группы, о чем свидетельствовали увеличение количества лейкоцитов, лимфоцитопения, моноцитоз и СОЭ. Повышение уровня мочевины и креа-тинина может свидетельствовать о наличии острой почечной недостаточности, что в свою очередь говорит об остром процессе, протекающем в плевральной полости.
Таким образом, показатели мочевины и креатинина достоверно отличаются у первой группы пациентов по сравнению с пациентами второй и третьей групп. По остальным биохимическим показателям не получено достоверных отличий во всех трех группах.
Заключение
1. Исследование анализов крови у пациентов с острым, подострым и хроническим воспалительным процессом в плевральной полости свидетельствует о выраженной раз-нонаправленности изменений на разных стадиях развития процесса.
2. Достоверные изменения выявлены в снижении уровня лейкоцитов, лимфоцитов, СОЭ у пациентов с подострым и хроническим течением заболевания. Достоверное увеличение мочевины у пациентов с острым течением заболевания. Достоверных отличий в результатах анализов при переходе подострой стадии в хроническую не выявлено.
3. Данные общего и биохимического анализов крови не позволяют дифференцировать между собой острый, подострый и хронический воспалительный процессы плевры, а позволяют лишь заподозрить переход острого процесса в хронический.
Литература
1. Караулов, А. В. Клиническая иммунология и аллергология / А. В. Караулов. — М.: Мед. информ. агентство, 2002. — 272 с.
2. Костюченок, Б. В. Раны и раневая инфекция: хирургический сепсис / Б. В. Костюченок, А. М. Свету-хин. — М.: Медицина, 1981. — 351 с.
3. Рудницкий, Л. В. О чем говорят анализы / Л. В. Рудницкий. — СПб.: Питер, 2008. — 146 с.

