Линкомицин при пародонтозе
Опубликовано в журнале:
Детский Доктор «» № 4’99
Антибактериальная терапия Н.В. Белобородова
Московская детская городская клиническая больница N13 им. Н.Ф. Филатова
В статье изложена позиция автора по проблеме наиболее рационального подхода к использованию инъекционных и пероральных форм антибиотиков у детей. Показано (в тот числе и на основании данных автора), что нередко без должных оснований используется инъекционный путь введения антибиотиков при лечении часто встречающихся инфекционных заболеваний (острые бактериальные инфекции органов дыхания и др.), а также применяются антибиотики, спектр действия которых не включает наиболее распространенных возбудителей указанных заболеваний. Приводятся конкретные рекомендации по оптимизации эмпирической антибактериальной терапии.
Наиболее распространенными заболеваниями у детей, как известно, являются заболевания носоглотки и верхних дыхательных путей (отит, сипусит, фарингит, бронхит, пневмония), а также инфекции кожи и мягких тканей. В связи с этим особое внимание должно быть уделено рациональному применению антибиотиков, так как они являются этиотропными препаратами и назначаются наиболее часто. Правильный выбор антибиотика определяет эффективность лечения, элиминацию возбудителя и быстроту выздоровления. Антибиотик наиболее эффективен при назначении в начале заболевания, поэтому он чаще всего выбирается эмпирически, без данных микробиологического исследования. При нерациональном выборе «стартового» антибиотика течение инфекционного процесса затягивается, могут развиться осложнения или суперинфекции, потребоваться повторные курсы лечения или госпитализация.
Не секрет, что болезненность инъекции антибиотиков относится к факторам, травмирующим неустойчивую и ранимую психику малыша. В дальнейшем это может обусловить ряд нежелательных особенностей поведения «трудного ребенка». Большинство наших малышей помимо всех неприятностей, связанных с болезнями, обречены уже с самого раннего детства на испытание сомнительного «удовольствия» от внутримышечных инъекций. В то же время эта процедура настолько болезненна, что даже многие взрослые мужчины с трудом на нее соглашаются, а некоторые отказываются вообще.
Между тем у маленького ребенка никто не спрашивает, согласен ли он лечиться таким образом. Защитить малыша не могут и любящие родители, так как они абсолютно беспомощны перед аргументами участкового педиатра, такими как: ребенок заболел повторно, он ослаблен, температура высокая, таблетки не помогают, показаны инъекции антибиотика. Иногда даже создается впечатление, что не важно, какой антибиотик применять, — главное, чтобы в инъекциях, так как это надежно и эффективно!
Мы должны признать, что находимся в плену у давным-давно сформировавшихся представлений, которые сегодня абсолютно не соответствуют реальности. Однопременно мы вводим в заблуждение родителей, ослепленных страхом за ребенка и практически не имеющих права голоса. Не пользуемся ли мы беспомощностью маленьких страдальцев, у которых нет иных аргументов, кроме огромных глаз, заполненных слезами? Мы нынуждены их обманывать («Не будет больно!»). Вот они и вырастают запуганными, недоверчивыми, сжимающимися в комочек при одном только виде белого халата. Разве может быть добром то, что больно?! А ведь это не только больно, но еще и небезопасно. Постинъекционные инфильтраты и абсцессы сегодня выглядят безобидными осложнениями по сравнению с трансинфузионными инфекциями — гепатитом, СПИДом и др.
Безусловно, всем этим можно было бы пренебречь, если бы цель оправдывала наши действия, 0днако это не так. Приведем всего два наиболее распространенных заблуждения.
Серьезную инфекцию можно вылечить только инъекциями. Но эффект лечения зависит не от способа введения препарата, а от спектра его активности и соответствия особенностям возбудителя. Так, например, пенициллин, ампициллин или оксациллин не будут эффективны ни в таблетках, ни и инъекциях, если инфекция дыхательных путей вызвана микоплазмами (нужны макролиды) или микрофлорой, продуцирующей ферменты беталактамазы (нужны ко-амоксиклав или цефалоспорины 2-го поколения). По той же причине не помогут и инъекции кефзола или цефамезина. Ребенок может в конце концов выздороветь сам, вопреки лечению, мобилизовав свои защитные силы, но рецидив инфекции высоковероятен. Тогда что же, снова инъекции?
При внутримышечном введении препарат действует эффективнее. Это заявление было справедливо много лет назад, до появления современных пероральных детских форм антибиотиков с всасываемостью до 90-95%. Многочисленными исследованиями и клиническим опытом доказано, что при приеме внутрь современные антибиотики создают достаточно высокие концентрации во всех тканях и органах, многократно перекрывая минимальные подавляющие концентрации для основных патогенов. Таким образом, по фармакокинетическим параметрам они не уступают инъекционным формам, зато по спектру действия имеют существенные преимущества в отношении многих современных возбудителей.
Кроме того, ряд препаратов, показанных в том числе при пневмонии, существует вообще только в пероральной форме (например, новые макролиды — азитромицин, рокситромицин и др.) и с успехом применяются во всем мире. Более того, в подавляющем большинстве западноевропейских стран инъекции в амбулаторной практике — крайняя редкость. Инъекции на дому касаются лишь серьезных заболеваний, которые долечиваются амбулаторно после предшествующей госпитализации (например, бактериального эндокардита и др.). Что касается инфекций дыхательных путей и ЛОР-органов, тем более у детей, то при лечении применяются только пероральные антибактериальные препараты, в том числе и в условиях стационара. В наиболее тяжелых случаях у детей, госпитализированных в состоянии выраженной интоксикации, отказывающихся от еды, при неукротимой рвоте применяют принцип ступенчатой терапии, когда на 2-3 дня назначается инфузионная внутривенная терапия, более щадящая, чем внутримышечная, а затем, по мере стабилизации состояния, — детские пероральные формы антибиотика. Тем самым избегают неоправданного стресса и никому не нужной боли.
А что у нас? По данным выборочного исследования, в Москве инъекции антибиотиков назначаются детям в 56% случаев при бронхите, в 90-100% случаев при пневмонии. В стационаре при лечении инфекций ЛОР-органов у маленьких детей также преобладают инъекционные антибиотики (до 80-90%).
Нельзя не сказать и о еще более опасной тенденции, характеризующей отечественную практику амбулаторной антибиотикотерапии. Кроме широкого использования инъекций часто назначаются инъекционно антибиотики, не предназначенные для лечения инфекций дыхательных путей и ЛОР-органов. Более того, не просто не показанные, но и запрещенные! Речь идет, прежде всего, о двух препаратах — гентамицине и линкамицине.
Общеизвестно, что аминогликозиды предназначены для лечения грамотрицательных инфекций в условиях стационара под тщательным лабораторным контролем в связи с потенциальной ото- и нефротоксичностью, а у нас гентамицин нередко назначает участковый педиатр. При этом не учитывается, что гентамицин (как и все остальные аминогликозиды) не включает в спектр своей активности пневмококки. Поэтому он никогда и нигде не предлагался как препарат для лечения амбулаторных инфекций дыхательных путей и ЛОР-органов. Видимо, это не случайно, ведь не могут же педиатры лечить вопреки здравому смыслу, если нет результата. Гентамицин приобрел популярность, когда в России среди патогенов, вызывающих заболевания дыхательных путей, распространились штаммы гемофильной палочки, устойчивые к ампициллину, но чувствительные к гентамицину. Эмпирически педиатры стали назначать аминогликозиды на дому, хотя есть более рациональное решение проблемы — применение пероральных «защищенных» пенициллинов (амоксициллин с клавулановой кислотой) и цефалоспоринов 2-го поколения.
Линкомицин — препарат с очень узкими показаниями и невысокой эффективностью — должен назначаться в стационаре лишь в случае микробиологически подтвержденной чувствительности к нему выделенного возбудителя, в частности стафилококка, и не подходит для амбулаторной практики, где лечение всегда проводится эмпирически. Бездействуя на пневмококк, он вообще не включает в спектр активности гемофильную палочку. Кроме того, линкомицин обладает еще одним существенным недостатком: у него наиболее выражено свойство подавлять необходимую ребенку бифидо- и лактофлору, приводить к дисбиозам и нарушению колонизационной резистентности желудочно-кишечного тракта. (В этом отношении с ним сходны лишь клиндамицин и ампициллин.) Понять, почему многие российские педиатры назначают детям гентамицин и линкомицин на дому несложно: врачи предпочитают инъекции пероральным препаратам, так как обеспечить правильную кратность введения бета-лактамных антибиотиков (пенициллинов или цефалоспоринов) 3-4 раза в день амбулаторно невозможно из-за организационных трудностей. На Западе считают неоправданной расточительностью, чтобы процедурная медсестра 4 раза в день посещала пациента на дому и делала инъекции. Нам для детей ничего не жалко, но медсестер не хватает. Педиатры пришли к компромиссному решению: назначать инъекции тех антибиотиков, которые можно вводить всего 2 раза в день, т.е. линкомицина и гентамицина. В результате проигрывает ребенок: ему больно, а лечение малоэффективно и небезопасно.
При выборочном исследовании, проведенном автором, оказалось, что среди 108 детей, госпитализированных в стационар с инфекцией дыхательных путей (38 — с бронхитом, 60 — с пневмонией), 35% составили дети раннего возраста. При тщательном опросе родителей выяснено, что почти 90% детей прежде получали антибиотики, причем в амбулаторных условиях с наибольшей частотой назначались следующие препараты. (См. табл. 1.)
Таблица 1. Частота применения некоторых антибиотиков в амбулаторной практике
| Препарат | Частота применения у детей, % |
| Пенициллин | 68 |
| Ампицилин | 60 |
| Линкомицин | 18 |
| Гентамицин | 10 |
В отношении препаратов, перечисленных в табл. 1, необходимо отметить следующее.
- Пенициллин и ампициллин неактивны в отношении многих современных возбудителей респираторных инфекций, так как разрушаются ферментами бактерии.
- Линкомицин вообще не включает в спектр активности гемофильную палочку, а гентамицин не действует на пневмококк.
- Ампициллин и линкомицин известны как препараты, подавляющие бифидо- и лактофлору, с самым высоким показателем развития дисбиоза у маленьких детей.
- Гентамицин — потенциально нефротоксичный аминогликозид, никогда не должен применяться в амбулаторных условиях, так как требует лабораторного мониторинга в стационаре.
Нет сомнения, что в каждом конкретном случае эти препараты назначались с благими намерениями, но первое последствие нерационального применения антибиотиков — повторное и тяжелое заболевание, потребовавшее госпитализации, — налицо. Отдаленные последствия вообще неясны: у скольких детей в будущем проявятся недостатки слуха, нарушения функции почек или хронический дисбактериоз, никто нс анализировал.
Почему же у нас сложилась такая порочная практика, когда дети с раннего возраста не только получают болезненные и ненужные инъекции, но и антибиотики им вводят не те, которые нужно и можно? Причина, по-видимому, в том, что у нас в стране политика антибиотикотерапии, в том числе в амбулаторной педиатрии, всегда складывалась стихийно, в годы лекарственного дефицита, и законодательно никем не регулировалась. В западных странах в отличие от России существуют и постоянно обновляются документы, регламентирующие правила антибиотикотерапии.
Исторически сложилось так, что для наших врачей и пациентов в прежние (доперестроечные) годы были недоступны «защищенные» пенициллины и цефалоспорины 2-го поколения. Когда участились инфекции, вызванные бета-лактамазопродуцирующей флорой, и «таблетки» действительно стали неэффективными, все надежды стали связывать только с инъекциями. Но, как уже было сказано, не имея возможности обеспечить нужную кратность введения бета-лактамных антибиотиков, стали отдавать предпочтение антибиотикам с 2-кратным режимом дозирования, несмотря на недостатки в их спектре и побочные эффекты.
Дорогие педиатры! Давайте оставим все проблемы в прошлом и констатируем тот факт, что сегодня наши маленькие пациенты живут в новой России, в новых условиях, где мы не можем пожаловаться на недостаток информации или недостаток лекарств. Теперь у нас есть все условия и возможности лечить детей не хуже, чем за рубежом. На отечественном рынке представлены антибиотики и европейских, и американских фармацевтических компаний. Остается только отказаться от старого представления о преимуществах инъекций и в каждом конкретном случае сделать правильный выбор детской формы перорального препарата. Актуальность изложенной проблемы не вызывает сомнений, так как нерациональная антибиотикотерапия неблагоприятно отражается на состоянии здоровья детей и дальнейшем их развитии. Поэтому в 1998 г. на базе Детской клинической больницы им. Н.Ф. Филатова (главный врач Г.И. Лукин) по инициативе отдела медицинской помощи детям и матерям (начальник отдела В.А. Прошин) Комитета здравоохранения Москвы создан Кабинет рациональной антибиотикотерапии. В Кабинет нередко направляются пациенты с последствиями неадекватной и избыточной терапии антимикробными препаратами в раннем возрасте, что приводит к их аллергизации, дисбиотическим нарушениям, развитию синдрома лихорадки неясной этиологии и другим заболеваниям.
Первоочередная задача Кабинета — оптимизация антибактериальной терапии в амбулаторной педиатрической практике. Было предложено запретить участковым педиатрам использовать инъекции гентамицина и линкомицина. Кроме того, разработаны методические указания, ориентированные на эффективные и безопасные пероральные антибиотики при инфекциях дыхательных путей и ЛОР-органов у детей. Эти указания для краткости сведены в таблицы. (См. табл. 2-4.)
Таблица 2. Современные пероральные антибиотики для амбулаторной терапии респираторных инфекций у детей
| Группа | Подгруппа | Химическое название | Торговое название детской пероральной формы |
| Бета-лактамные антибиотики — пенициллины | Пенициллины | Феноксиметилпенициллин | Оспен, Фау-пенициллин |
| Полусинтетические пенициллины | Оксациляин, Ампицилпин | Оксациляин, Ампициллин | |
| «Защищенные» пенициллины — комбинированные с клавулановой кислотой | Амоксициллин/клавуланат, или ко-амоксиклав | Амоксиклав, Аугментин | |
| Бета-лактамные антибиотики — цефалоспорины | Цефалоспорины 1-го поколения | Цефадроксил, Цефалексин | Дурацеф, Цефалексин |
| Цефалоспорины 2-го поколения | Цефуроксим, Цефаклор | Зиннат, Цеклор | |
| Макролиды | Макролиды | Азитромицин, Рокситромицин, Эритромицин | Сумамед, Рулид, Эритромицин |
Таблица 3. Дифференцированный подход к стартовому выбору антибиотика при респираторных инфекциях у детей в зависимости от локализации процесса
| Фарингит, Тонзилит | Отит, синусит | Бронхит | Пневмония | |
| Обычный ребенок | Пенициллины | Цефалоспорины 1-го поколения | Макролиды | Цефалоспорины 1-2-го поколения |
| Часто болеющий peбенок из группы риска | Полусинтетические или «защищенные» пенициллины | «Защищенные» пенициллины | Азитромицин | Цефалоспорины 2-го поколения |
Таблица 4. Алгоритм выбора препарата при затяжном и рецидивирующем течении респираторных инфекций носоглотки и дыхательных путей у детей в зависимости от предшествующей антибиотикотерапии
| Фарингит, Тонзилит | Отит, синусит | Бронхит | Пневмония | |
| Предшествующий антибиотик | Рекомендуемый антибиотик | |||
| Оспен, Фау-пенициллин | Полусинтетические или «защищенные» пенициллины | Полусинтетические или «защищенные» пенициллины | Макролиды | Цефалоспорины 1-2-го поколения |
| Оксациляин, Ампициллин | Цефалоспорины 1-2-го поколения | Макролиды, цефалоспорины 1-го поколения или «защищенные» пенициллины | Макролиды | Цефалоспорины 2-го поколения |
| Амоксиклав, Аугментин | Фузидин (Исключить грибы!) | Фузидин (Исключить грибы!) | Макролиды | Макролиды или цефалоспорины 2-го поколения |
| Дурацеф, Цефалексин | «Защищенные» пенициллины | «Защищенные» пенициллины | Макролиды | «Защищенные» пенициллины или цефалоспорины 2-го поколения |
| Зиннат, Цеклор | Фузидин (Исключить грибы!) | Фузидин (Исключить грибы!) | Макролиды | Макролиды |
| Сумамед, Рулид Эритромицин | Цефалоспорины 1-2-го поколения | «Защищенные» пенициллины | «Защищенные» пенициллины | Цефалоспорины 2-го поколения или «защищенные» пенициллины |
Для практики очень важно, чтобы большинство пероральных детских форм антибиотиков (цефалоспорины, макролиды, «защищенные» пенициллины) были включены в Перечень бесплатных или льготных препаратов, как это разумно сделано в Москве. Необходимо отметить, что внедрение предложенных рекомендаций сулит не только детскую благодарность, но и существенные выгоды в экономическом отношении. Зарубежные работы и наши рандоми-зированные сравнительные исследования, проведенные в реальных российских условиях, доказали, что применение на первый взгляд более дорогих импортных препаратов (современных макролидов, пероральных цефалоспоринов, «защищенных» пенициллинов) в конечном итоге дает существенный экономический эффект за счет качества лечения, сокращения длительности курсов, отсутствия дополнительных расходов, связанных с инъекциями, госпитализацией, осложнениями и т.п. . При правильном целенаправленном назначении пероральных препаратов по сравнению с традиционными парентеральными (в условиях стационара) экономия достигает 15-25%.
Таким образом, в настоящее время существует реальная возможность практически полностью отказаться от инъекций антибиотиков в амбулаторных условиях в связи с широким выбором пероральных детских форм современных антибиотиков, которые в большинстве случаев эффективнее традиционных парентеральных. В стационаре современным щадящим режимом для детей следует считать так называемую ступенчатую терапию, когда в первые дни при тяжелом состоянии ребенка ему назначается инъекционный антибиотик, а через 2-3 дня переходят на пероральную детскую форму препарата .
С целью повышения уровня знаний врачей-педиатров в области современных возможностей рациональной антибиотикотерапии уже второй год в Москве функционирует постоянно действующая школа-семинар, организованная Кабинетом рациональной антибиотикотерапии при ДГКБ им. Н.Ф. Филатова. Число слушателей школы нарастает от семинара к семинару, и мы считаем целесообразным рекомендовать такую форму информационной помощи педиатрам и в других регионах России.
Призываем организаторов здравоохранения, администраторов и практикующих врачей не только в Москве, но и в других регионах России объявить войну консерватизму и присоединиться к движению под лозунгом «Счастливое детство — без инъекций!»
Литература
К антибиотикотерапии я прибегаю не часто, стараюсь сначала испробовать для лечения более щадящие методы. Но есть такие случаи, когда без антибиотика не обойтись.
С антибиотиком Доксициклин я сталкивалась дважды: первый раз я принимала его при заболеваниях кожи, второй раз совсем недавно после удаления зуба мудрости.
Доксициклин — это антибиотик достаточно старый. Страшно сказать — он был изобретен в далеком 1966 году, примерно спустя 20 лет после открытия первого антибиотика (пенницилин G). С тех пор много воды утекло, микроорганизмы уже тыщу раз приспособились и стали намного живучее. И я не понимаю каким чудом этот антибиотик еще работает. Но работает ведь!
Доксициклин отзывы
Доксициклин относится к антибиотикам тетрациклинового ряда и имеет широкий спектр действия и спектр показаний.
Расскажу подробней об антибиотике и его характеристиках, а также какие побочные эффекты я заметила.
- Место покупки: любая аптека города
- Стоимость: около 10 грн
- Производитель: Борщаговский ХФЗ
- Количество капсул: 10 шт.
Упаковка: небольшая картонная пачка, в которой содержится пластинка с капсулами, а также подробная инструкция по препарату.
По обеим сторонам упаковки содержится информация о производителе, а также условия отпуска препарата.
На торце упаковки указаны дата изготовления и конечный срок годности препарата.
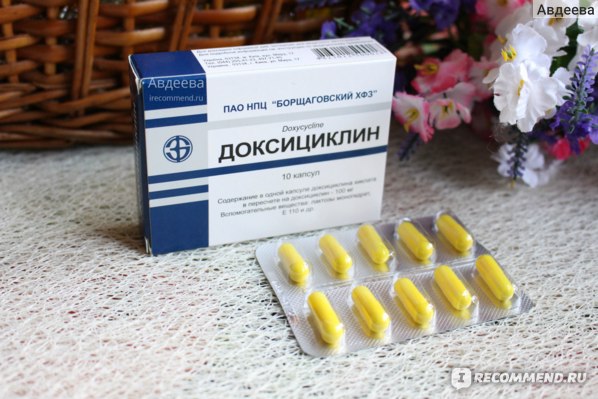
Капсулы находятся в алюминиевой пластинке. Каждая капсула имеет желатиновую оболочку желтого цвета, внутри находится порошок белого цвета.
Для тех, кто не может в силу каких-либо причин глотать большие капсулы, хочу предостеречь — не делите капсулы, содержимое нейтрализуется соляной кислотой внутри желудка, вы просто не получите эффекта от антибиотика!
Желатиновая оболочка кишечнорастворимая, она защищает содержимое капсулы и доставляет непосредственно в место назначения.
Доксициклин отзывы Доксициклин отзывы
Доксициклин быстро всасывается, следовательно, быстро начинает работать. Прием пищи не влияет на всасываемость препарата, так что можно не делать привязки к еде.
Показания:
инфекции дыхательных путей и ЛОР-органов, мочеполовой системы, желчевыводящих путей и желудочно-кишечного тракта, инфекционные заболевания глаз, профилактика послеоперационных гнойных осложнений
Побочные действия:
Возможно: тошнота, рвота, анорексия, боли в животе, диарея, аллергические реакции в виде отека, зуда, кожной сыпи (в сиропе могут содержатся сульфиты, которые могут вызывать аллергические реакции вплоть до анафилаксии и тяжелых приступов бронхиальной астмы), головокружение, потливость
Из побочных действий могу отметить только легкое расстройство ЖКТ. Это не смертельно, всё прошло сразу же после прекращения приема препарата. Препараты для нормализации флоры кишечника я не принимала, после прекращения приема антибиотика стул стал прежним.
Противопоказания:
Повышенная чувствительность к тетрациклинам; беременность (вторая половина); лактация; детский возраст до 9 лет; порфирия; тяжелая печеночная недостаточность; лейкопения
Применение:
Внутрь, у взрослых и детей старше 12 лет с массой тела более 45 кг средняя суточная доза — 200 мг в первый день (делится на 2 приема — по 100 мг 2 раза в сутки), далее по 100 мг/сут.
ВАЖНО! После приема Доксициклина, а также всех его аналогов, включая известный антибиотик Юнидокс Солютаб, нельзя лежать в течение получаса.
Оба раза я принимала утром и вечером по 1 капсуле, продолжительность терапии составляла 5 дней. Т.е. одной упаковки мне хватало на курс лечения.
Хочу добавить, что перед применением Доксициклина я сдавала кровь на чувствительность к антибиотикам — это нужно сделать обязательно, чтобы не принимать препарата наобум, который вам вовсе не сможет помочь.
Впервые я его принимала для лечения фурункулеза, эффект был временным, но золотистый стафилококк вообще попробуй чем-то убить))
Далее для этой цели к Доксициклину я уже не прибегала, а принимала более новые сильные антибиотики.
Второй раз я принимала Доксициклин совсем недавно — пару месяцев назад, после удаления зуба мудрости. Кроме антибиотика мне назначили местное лечение гелем Метрогил-дента.
Антибиотик снял воспаление, не дал развиться бактериальной инфекции. Пяти дней лечения вполне хватило.
Доксициклин отзывы
Нужно помнить, что бесконтрольный прием антибиотиков кроме вреда вам ничего не принесет! Антибиотики назначаются только вашим лечащим врачом и после сдачи теста на чувствительность к антибиотику.
Не покупайте антибиотики сами в аптеках, не спрашивайте совета фармацевтов, тем более не покупайте антибиотики по рекомендации соседки/подруги!
Имея фармацевтическое образование и проработав несколько лет в аптеке, хочу поделиться полезной информацией ↷
Информация, которая пригодится вам при антибиотикотерапии
1. НЕТ самолечению! Антибиотик назначает только специалист — врач.
2. Чтобы понять подойдет вам тот или иной препарат, необходимо сдать тест на чувствительность к антибиотику (чаще берут кровь, но можно также сдать и любой другой биоматериал: слюна, моча, мазок слизистых и т.д.). Во-первых, это нужно, чтобы удостовериться является ли бактерия причиной инфекции, поскольку если это грибок или вирус, то антибиотик на них не подействует, а во многих случаях даже усугубит ситуацию; во-вторых, зная какой тип бактерии вызвал вашу болезнь, врач легко подберет индивидуально под вас препарат.
Даже если вы болели в прошлом году ангиной и вам помог антибиотик, то нет гарантии, что при таком же диагнозе вам он поможет снова!
3. Нет бесконтрольному приему антибиотика! Пока вы точно не знаете диагноз, не принимайте антибиотик. Знаю очень многие пытаются вылечить простуду тем, что с первых дней принимают антибиотик. Это в корне неверно! Тем самым вы мешаете организму самому победить инфекцию, возбудителем которой является вирус.
4. Не принимайте антибиотик для профилактики! В моей практике были и такие случаи и, к сожалению, они часты. Нет смысла принимать антибиотик в профилактических целях, этим самым вы навредите своему организму и когда вы заболеете этот антибиотик вам уже не поможет.
5. Прием антибиотиков лучше сопровождать приемом препаратов для нормализации микрофлоры кишечника (пребиотики + пробиотики), а также гепатопротекторов. Нужно помнить, что при антибиотикотерапии ослабевает иммунитет (помним, что 70% иммунитета — в кишечнике, полезная флора убита), может развиться на этом фоне грибок, отсюда молочница, особенно если речь идет об антибиотике широкого спектра действия.
6. Нельзя прекращать прием антибиотика, не пройдя курс лечения! Если вы спустя пару-тройку дней заметите улучшение состояния решите «не травить организм химией», то, поверьте, этим вы сделаете только хуже, ведь есть такое понятие как резистентность. Не убитые бактерии окрепнут, мутируют, приобретут устойчивость и в следующий раз этот антибиотик вам уже не поможет!
7. Нельзя превышать дозы антибиотика (и уменьшать тоже). Принимаем антибиотик только согласно инструкции, если даем антибиотик ребенку, то рассчитываем правильно дозировку исходя из веса ребенка.
УДК 616-089-06-022-085.281 DOI: 10.21626/vestnik/2018-3/12
ЭКСПЕРИМЕНТАЛЬНОЕ ОБОСНОВАНИЕ ВОЗМОЖНОСТЕЙ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ ИНФЕКЦИОННЫХ ОСЛОЖНЕНИЙ
ХИРУРГИЧЕСКОЙ ПАТОЛОГИИ
© Иванов Д.А.1, Калуцкий П.В.2, Дубровин Г.М.3, Медведева О.А.2
1 Лыткаринская городская больница, Лыткарино, Московская область; 2 кафедра микробиологии, вирусологии, иммунологии, 3 кафедра травматологии и ортопедии Курского государственного медицинского университета, Курск
E-mail: IvanovDA2001@mail.ru
С целью исследования синергетического эффекта было изучено влияние сочетанного применения кровезаменителя перфторан и антибиотиков линкомицин, ципролет и цефотаксим на уровень их минимальной подавляющей концентрации (МПК) и минимальной бактерицидной концентрации (МБК) в опытах in vitro с помощью метода разведений в агаре с использованием коллекционных штаммов Staphylococcus aureus АТСС 25923, Bacillus subtilis АТСС 6633, Escherichia coli АТСС 25922, Pseudomonas aeruginosa АТСС 27853, Proteus vulgaris АТСС 4636 и Candida albicans NCTC 2625. Установлено, что перфторан не оказывает антибактериального действия в отношении исследуемых штаммов. Введение в питательную среду комбинации перфторана и антибактериальных препаратов снижает МПК и МБК. Этот эффект наиболее выражен при комбинировании перфторана с цефотаксимом — снижение МПК в 8-32 раза, а МБК в 4-64 раза. У ципролета и линкомицина этот эффект наблюдался в отношении отдельных культур и не более чем в 2-4 раза. Обнаруженный эффект объясняется вступлением факультативных анаэробов в фазу вегетации, что снижает их устойчивость к действию антибактериальных препаратов.
Ключевые слова: гнойные осложнения в хирургии, антибиотики, перфторан, цефотаксим, линкомицин, ципролет.
EXPERIMENTAL GROUNDS FOR POSSIBILITIES OF IMPROVING ANTIBACTERIAL THERAPY
Keywords: purulent complications in surgery, antibiotics, Perftoran, Cefotaxime, Lincomycin, Tsiprolet.
Прогноз восстановления строения и функции органов и тканей организма человека при различного рода хирургической патологии и/или травме связан как со степенью тяжести самой патологии, так и с объемом и тяжестью осложнений самого оперативного вмешательства, а также осложнений, возникающих на этапах послеоперационного периода. И одним из самых прогностически неблагоприятных является присоединение инфекции .
Традиционно в этом случае применяется комплекс мероприятий, таких как: обеспечение оттока раневого содержимого различными способами с одновременным использованием антисептиков, проточное дренирование, местное воздействие на рану различными способами (физиотерапевтиче-
ские методы, аэрация раны, местное применение лекарственных средств). В последнее время с развитием иммунологии кроме уже рутинных методов, связанных с введением человеческого иммуноглобулина, получают развитие методики стимуляции иммунного ответа пациентов. Но успешность лечения инфекционных осложнений при хирургической патологии по-прежнему сильно зависит от общей реактивности организма, а также от свойств микрофлоры, вызвавшей инфекционное осложнение. Поэтому определяющее значение в тактике ведения таких пациентов приобретает эффективная и рациональная антибио-тикотерапия. Во-первых, это назначение антибиотиков широкого спектра действия на начальном этапе лечения до момента получения информации
о чувствительности высеянных из отделяемого из раны микроорганизмов к антибактериальным препаратам. Далее — индивидуальный подбор наиболее эффективных для данного набора микроорганизмов антибактериальных препаратов . Как раз последний этап такой тактики лечения и вызывает на практике наибольшие затруднения вследствие повышения резистентности микроорганизмов к антибактериальным препаратам и уже поэтому — фактического дефицита эффективных антибиотиков «резерва».
И если методы местного лечения можно совершенствовать (разработка новых эффективных систем приточно-аспирационного дренирования раны, применение систем капельного орошения, использование аэрированных растворов антисептиков, применение новых антисептиков, новых и ранее известных физиотерапевтических факторов изолированно и в сочетании друг с другом и т.д.) , то создание новых антибактериальных препаратов существенно затруднено. Поэтому одним из перспективных направлений повышения эффективности антибактериальной терапии следует считать изучение синергетического эффекта препаратов разных групп. Учитывая известную зависимость скорости деления микробов от концентрации кислорода непосредственно в поврежденных тканях, одним из перспективных направлений является изучение синергетического эффекта уже известных антибактериальных препаратов и лекарственных веществ, способных участвовать в переносе кислорода непосредственно в тканях. К последним относятся т.н. перфторированные углеводороды, представителем которых является разрешенный к применению кровезаменитель с газотранспортной функцией перфторан (ПФ) . Его влияние на процессы регенерации различных тканей ранее изучались, в том числе и нами, и в том числе в условиях экспериментального септического воспаления . Но степень выраженности синер-гетического эффекта с антибактериальными препаратами ранее не изучалась.
Поэтому целью нашей работы было исследование in vitro синергетического эффекта трех наиболее часто применяемых в практике травматологической клиники антибактериальных препаратов линкомицин (ЛИ), ципролет (ЦИ), цефотак-сим (ЦФ) и ПФ для обоснования рациональной и эффективной антибактериальной терапии инфекционных осложнений в хирургической и травматологической практике.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Проведен анализ информационных материалов микробиологической лаборатории управления Роспотребнадзора по Курской области за 2008-2014 годы о составе микрофлоры, высеваемой из отделяемого ран пациентов хирургических и травматологических отделений больниц г. Курска. На базе лаборатории кафедры микробиологии, вирусологии, иммунологии Курского государственного медицинского университета методом серийных разведений была изучена антимикробная активность чистого ПФ в отношении тест-штаммов микроорганизмов, используемых для оценки антимикробного действия препаратов: Staphylococcus aureus АТСС 25923, Bacillus subtilis АТСС 6633, Escherichia coli АТСС 25922, Pseudomonas aeruginosa АТСС 27853, Proteus vulgaris АТСС 4636 и Candida albicans NCTC 2625. Определяли минимальную подавляющую концентрацию препаратов (МПК) и минимальную бактерицидную концентрацию (МБК) наиболее распространенных в практике лечения хирургической инфекции препаратов: линкоми-цин (ЛИ), ципролет (ЦИ) и цефотаксим (ЦФ), чистого ПФ, а также указанных антибиотиков в сочетании с ПФ. В каждом случае проводили 10 наблюдений, по результатам которых определяли кратность изменения МБК и МПК между группами с чистыми антибиотиками и их соче-танным применением с ПФ. Определяли широту доверительного интервала (t) для p<0.05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
На первом этапе исследования было установлено, что препарат ПФ не имеет бактериостатиче-ской и бактерицидной активности в отношении всех исследованных штаммов микроорганизмов Staphylococcus aureus АТСС 25923, Bacillus subtilis АТСС 6633, Escherichia coli АТСС 25922, Pseudomonas aeruginosa АТСС 27853, Proteus vulgaris АТСС 4636 и Candida albicans NCTC 2625.
На втором этапе исследований in vitro исследовали активность широко используемых в хирургической и травматологической практике препаратов ЛИ, ЦИ и ЦФ в сочетании с ПФ в отношении вышеуказанных коллекционных штаммов. Следует отметить, что штамм Candida albicans был исключен из исследования, так как исследуемые препараты не являются противогрибковыми.
Было установлено, что минимальная подавляющая концентрация препарата (МПК) ЛИ в со-
четании с ПФ снижалась только в отношении грамположительных микроорганизмов — S. aureus и B. Subtilis, для P. aeruginosa и E. coli значение уровня МПК не изменилось, а для P. vulgaris МПК возросла при сочетанном применении ЛИ и ПФ в 2 раза. Следует отметить, что для S. aureus и B. Subtilis МБК ЛИ при его комбинации с ПФ снижалась в 4-8 раз.
Применение ЦИ в сочетании с ПФ не влияло на активность антибиотика в отношении P. vulgaris, S. aureus, B. subtilis — мы наблюдали значения МПК как и в случае применения только ЦИ. Но для P. aeruginosa мы зарегистрировали уменьшение уровня МПК в 2 раза, а для E. coli — в 32 раза (табл. 1). Для P. vulgaris и B. subtilis МБК ЦИ и сочетания ЦИ и ПФ не различались (табл. 2).
Одновременное внесение в питательную среду ЦИ и ПФ вызывало уменьшение МБК в отношении P. aeruginosa и S. aureus в 2 раза, а E. coli -в 8 раз. Статистически значимых отличий между сравниваемыми группами по МБК для большин-
ства штаммов не выявлено (табл. 2).
В наибольшей степени оказалось эффективным сочетанное применение ПФ и ЦФ, при котором МПК снижалась для всех культур микроорганизмов, использованных в эксперименте (табл. 1). Так, в отношении P. aeruginosa, P. vulgaris и S. aureus это было восьмикратное снижение МПК, для B. subtilis — 16-кратное, а для E. Coli МПК уменьшилась в 32 раза. Такой же эффект при сочетанном применении ПФ и ЦФ установлен при определении МБК (табл. 2). Для P. aeruginosa установлено 4-кратное уменьшение МБК, в отношении P. vulgaris, S. aureus и B. subtilis — 16-кратное, а для E. coli МБК уменьшилась в 64 раза.
Таким образом, в опытах in vitro установлено, что введение в питательную среду ПФ не оказывает антибактериального действия в отношении вышеперечисленных коллекционных штаммов микроорганизмов. Но при введении в питательную среду комбинаций ПФ и исследуемых антибиотиков наблюдается уменьшение МПК и МБК.
Таблица 1
Минимальная подавляющая концентрация линкомицина, ципролета, цефотаксима и их комбинации с перфтораном
Микроорганизм Л Л+ПФ ЦИ ЦИ+ПФ ЦФ ЦФ+ПФ
Номер группы сравнения 1 2 3 4 5 6
P. aeruginosa АТСС 27853 1:200 1:200 1:25600 1:512003 1:200 1:16005
P. vulgaris АТСС 4636 1:25 1:50 1:12800 1:12800 1:3200 1:256005
B. subtilis АТСС 6633 1:400 1:6400х 1:25600 1:25600 1:3200 1:512005
S. aureus АТСС 25923 1:200 1:800х 1:3200 1:3200 1:6400 1:512005
E. coli АТСС 25922 1:100 1:100 1:400 1:128003 1:6400 1:2048005
Примечание: надстрочными индексами отмечены статистически значимые отличия между сравниваемыми группами.
Таблица 2
Минимальная бактерицидная концентрация линкомицина, ципролета, цефотаксима и их комбинации с перфтораном
Микроорганизм Л Л+ПФ ЦИ ЦИ+ПФ ЦФ ЦФ+ПФ
Номер группы сравнения 1 2 3 4 5 6
P. aeruginosa АТСС 27853 Отсутствует Отсутствует 1:1600 1:3200 1:100 1:4005
P. vulgaris АТСС 4636 Отсутствует Отсутствует 1:6400 1:6400 1:1600 1:256005
B. subtilis АТСС 6633 1:100 1:800х 1:25600 1:25600 1:3200 1:512005
S. aureus АТСС 25923 1:50 1:200х 1:800 1:1600 1:6400 1:256005
E. coli АТСС 25922 Отсутствует Отсутствует 1:200 1:16003 1:3200 1:2048005
Примечание: надстрочными индексами отмечены статистически значимые отличия между сравниваемыми группами.
Этот эффект наиболее выражен в комбинации ПФ и ЦФ, где отмечено максимальное снижение МПК (от 8 до 32 раз). Также в этом случае наблюдали 4-64-кратное снижение МБК в отношении всех изученных тест-штаммов микроорганизмов. Другие два препарата (ЦИ и ЛИ) в сочетании с ПФ демонстрировали снижение МПК и МБК только в 2-4 раза. По нашему мнению, си-нергетические возможности ПФ в сочетании с антибиотиками можно объяснить тем, что он способствует транспорту кислорода по градиенту его парциального давления из атмосферного воздуха в питательную среду, тем самым повышая в ней содержание кислорода. Очевидно при превышении некоего порогового значения парциального давления кислорода в питательной среде, факультативные анаэробы начинают использовать аэробный тип дыхания и вступают в фазу вегетации, оказываясь в этот момент более чувствительными к антибактериальным препаратам. Эта гипотеза подтверждается тем, что в эксперименте in vitro был установлен предел снижения МПК и МБК для всех исследуемых антибиотиков, а конкретное значение такого предела связано как с уменьшением концентрации самого антибактериального препарата, так и с уменьшением концентрации ПФ в питательной среде.
ЛИТЕРАТУРА / REFERENCES
3. Зюзя Е.В., Калуцкий П.В., Иванов А.В. Влияние сочетанного применения кровезаменителя перфто-ран и антибиотика цефотаксим на состояние иммунологических показателей периферической крови в условиях моделирования инфицированной раны и воздействия на организм постоянного магнитного поля // Вестник новых медицинских технологий. Электронное издание. — 2013 — № 1. -С. 80. .