Кровотечения у детей
Учебно-методическое пособие для вузов
В.П. Обрядов, В.В. Паршиков, Н.В. Козулина
2007 год
В пособии представлены аспекты современной диагностической тактики, дифференциальной диагностики и лечения всех основных заболеваний, сопровождающихся появлением крови в стуле, основанные на современных литературных данных и результатах наблюдений авторов.
Пособие поможет студентам 5—6-х курсов педиатрического и лечебного факультетов подготовиться к практическим занятиям по детской хирургии, а также будет весьма полезным для врачей-педиатров и хирургов, в том числе общего профиля.
Содержание
- Предисловие
- Введение
- Общие принципы диагностики заболеваний, сопровождающихся кровотечением из нижних отделов желудочно-кишечного тракта
- Патологии — причины кровотечений из нижних отделов желудочно-кишечного тракта
- Врожденные аномалии кишечника
- Гиполазия легких (недоразвитость легких)
- Массированное легочное кровотечение
- Конгенитальная диафрагмальная грыжа
- Эзофагеальная атрезия и трахеоэзофагеальная фистула
- Кистозный аденоматоидный порок развития
- Хронические легочные заболевание у новорожденных
Предисловие
С проблемой кровотечений из нижних отделов пищеварительного тракта, без сомнения, встречается каждый детский врач.
Предлагаемое пособие объединяет разрозненные сведения о причинах кровотечений из нижних отделов пищеварительного тракта у детей и рассматривает алгоритм действий при подозрении на данную патологию.
Особенно важно, что авторы освещают не только экстренные ситуации, в которых требуется неотложная хирургическая помощь, но и случаи хронической или рецидивирующей патологии, когда родители больного ребенка обращаются в первую очередь к педиатрам — гастроэнтерологам, участковым врачам. Кроме того, данное пособие будет полезно и хирургам общего профиля, и врачам-терапевтам, поскольку рассматриваются заболевания, сопровождающиеся появлением крови в стуле, более характерные для взрослых пациентов, однако причины этих патологий следует искать в детском возрасте.
Пособие является необходимым дополнением к основному учебному материалу при изучении хирургических дисциплин студентами 5—6-х курсов педиатрического и лечебного факультетов, а также будет весьма полезным в практической работе врачей разных профилей как педиатрической, так и лечебной сети.
Введение
Среди патологических состояний кишечника у детей весьма широкое распространение имеют заболевания, ведущим симптомом которых является выделение крови со стулом. О кровотечениях из нижних отделов желудочно-кишечного тракта принято говорить в тех случаях, когда их источник располагается в кишечнике дистальнее связки Трейтца. Данная патология составляет примерно 20% всех кровотечений из гастроинтестинального тракта. Они могут быть острыми и хроническими, массивными и скрытыми. Кровотечения несколько чаще встречаются у пациентов мужского пола.
Кровотечения из нижних отделов желудочно-кишечного тракта являются одним из наиболее грозных осложнений заболеваний органов пищеварения. Своевременная диагностика основана на знании возможных причин возникновения данной патологии, что в свою очередь позволяет выбрать правильную тактику дальнейшего лечения больного.
Топическая диагностика этого осложнения представляет значительные трудности и является одним из препятствий к своевременному радикальному лечению.
У 5—10% детей с кровотечением из нижних отделов желудочно-кишечного тракта, поступающих в стационар, причину геморрагии выявить так и не удается, несмотря на проведение комплексного инструментального обследования.
Общие принципы диагностики заболеваний, сопровождающихся кровотечением из нижних отделов желудочно-кишечного тракта
В диагностике заболеваний, сопровождающихся появлением крови в стуле, важное место отводится тщательному сбору анамнеза и выявлению клинических проявлений. Уже на этом этапе можно предположить наличие у больного определенной нозологической формы.
Однако основными и решающими методами являются инструментальные исследования — эндоскопическое и рентгенологическое. В ряде случаев, при определенных заболеваниях, они оказываются недостаточно информативными, и тогда возникает необходимость проведения ангиографии, диагностической лапароскопии и даже лапаротомии в комплексе с интраоперационной трансиллюминацией кишечной стенки. Эти манипуляции чаще применяются при таких трудно диагностируемых заболеваниях, как ангиодисплазии.
На первом этапе обследования необходимо уточнить следующие наиболее информативные в клиническом отношении моменты: возраст ребенка, начало заболевания (острое или постепенное), течение болезни (острое, хроническое, рецидивирующее), общее состояние больного, наличие болевого синдрома (см. таблицу).
Особенности возникновения и течения заболеваний
с симптомом крови в стуле
|
Нозологическая форма |
Возраст больного | Начало заболевания | Течение болезни | Общее состояние |
Болевой синдром |
| Дивертикул Меккеля | Любой | Острое | Острое | Тяжелое | Выраженный, нелокализованный |
| Сосудистая патология | Любой | Острое | Рецидивирующее | Тяжелое | Нет |
| Полипы | Чаще 3—6 лет | Острое | Хроническое, рецидивирующее | Не страдает | Нет |
| Геморрой | Старший | Постепенное | Рецидивирующее | Не страдает | В заднем проходе |
| Анальные трещины | Чаще младший | Острое | Рецидивирующее | Не страдает | В заднем проходе |
| Опухоли | Чаще старший | Постепенное | Хроническое | Страдает в поздних стадиях | Присутствует в поздних стадиях |
| Системные болезни | Старший | Постепенное | Рецидивирующее | Страдает значительно | Связан с основной болезнью |
| Неспецифический язвенный колит | Любой | Постепенное, 2—6 мес | Рецидивирующее | Страдает значительно | По ходу толстой кишки |
| Болезнь Крона | Чаще старший | Постепенное | Прогрессирующее | Страдает значительно | Без определенной локализации |
| Инвагинация | Ранний, 4—10 мес | Внезапное | Острое | Признаки кишечной непроходимости | Выражен, волнообразный |
Основной, часто решающей для диагностики, является характеристика кишечного кровотечения. При источниках кровотечения, расположенных в подвздошной кишке, кровь выделяется, в зависимости от интенсивности кровотечения, в значительно измененном виде, в проксимальных отделах толстой кишки — в малоизмененном виде, сохраняя свои как макро-, так и микроскопические признаки. Чем дистальнее по ходу кишечника находится источник кровотечения, тем меньше степень изменений выделенной крови.
Характер заболевания также определяет вид и количество кровянистых выделений.
Неспецифический язвенный колит, болезнь Крона (в фазе обострения), дивертикул Меккеля и высокорасположенные гемангиомы сопровождаются большим количеством примесей темной крови в стуле.
Опухолевые процессы при распаде чаще характеризуются выделением темной крови в небольшом количестве, если не поражены достаточно крупные сосуды.
При полипах темная или алая кровь присутствует в кале в виде полосок и поверх кала в виде лужицы. При самоампутации полипа возможно обильное кровотечение из сосудов ножки и появление в кале кроме головки полипа еще и сгустков крови.
При анальных трещинах и геморрое кровь видна как прожилки в кале, капельки или лужицы алого цвета, чаще поверх кала.
При аллергических и системных заболеваниях в значительной степени могут варьировать как объем кровотечения, так и качественная характеристика выделившейся крови.
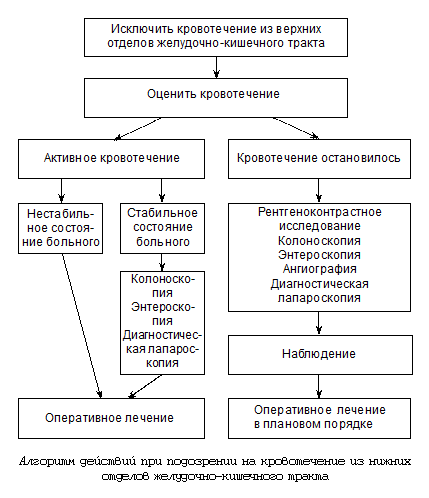
Основные этапы ведения больного с кровотечением из нижних отделов желудочно-кишечного тракта могут быть представлены в виде алгоритма (см. рисунок).
Патологии — причины кровотечений из нижних отделов желудочно-кишечного тракта
Симптом появления крови в кале объединяет различные по генезу заболевания:
- врожденные аномалии кишечника (дивертикулы, дубликатуры);
- аноректальные заболевания (трещина заднего прохода, геморрой, выпадение прямой кишки);
- опухоли кишечника (доброкачественные и злокачественные);
- сосудистую патологию (гемангиомы, ангиодисплазии);
- системные заболевания (лимфофолликулярная гипер-плазия, аллергия на молоко, системные заболевания соединительной ткани и сосудов — системная красная волчанка, дерматомиозит, склеродермия, узелковый периартериит, геморрагический васкулит);
- воспалительные заболевания неясной этиологии (неспецифический язвенный колит, болезнь Крона);
- приобретенные заболевания — инвагинация кишечника.
Кроме того, необходимо отметить и ряд чрезвычайно редких причин появления крови в стуле, таких как прорыв в просвет кишечника врожденных аневризм крупных сосудов, расположенных вне кишечной стенки, ожоги толстой кишки, инородные тела и травмы.
Врожденные аномалии кишечника
Дивертикулы кишечника — ограниченные выпячивания стенки кишки, состоящие из всех слоев последней (истинные дивертикулы) или только из слизистого и подслизистого слоев (ложные дивертикулы). Дивертикулы встречаются на всем протяжении кишечной трубки, в толстой кишке их локализация в детском возрасте относительно редка.
Свертываемость крови у детей поддерживается в норме «факторами свертывания». Этих факторов очень много и функции их различны, факторы свертывания могут повышаться или понижаться, и то и другое отклонение от нормы – плохо.
Основные показатели свёртываемости крови и особенности их у детей
Главным анализом, определяющим состояние крови и способность её к образованию тромбов, является коагулограмма. Этот анализ может включать в себя внушительное количество показателей, но в основном определяются только необходимые для врача результаты.
В большинстве случаев свертываемость определяется при необходимости оперативных вмешательств. Для этого исследуются уровень тромбоцитов, определяется длительность кровотечения и время свёртывания.
Уровень тромбоцитов в общем анализе крови
- период новорожденности 100-420·10⁹/л;
- от 1 месяца и до года 150-350·10⁹/л;
- после года 180-320·10⁹/л.
Когда тромбоциты опускаются ниже 100·10⁹/л, возникает угроза кровотечений, а при уровне в 50·10⁹/л, нужно быть крайне осторожным, так как при небольшой травме остановить кровь крайне тяжело и без переливания тромбоцитарной массы практически невозможно.
Длительность кровотечения и время свёртываемости
Также довольно простые и информативные методы определения свёртываемости крови у детей.
норма длительности кровотечения у ребёнка составляет 2-4 минуты;
время свертываемости показывает за сколько образуется кровяной сгусток, оно колеблется в пределах 2-5 минут.
Если вышеперечисленные факторы выходят за пределы нормы, то необходимо дополнительное исследование остальных показателей свёртываемости крови.
Протромбиновое время и протромбиновый индекс
Данный показатель характеризует начальные фазы свертываемости, и позволяет выявить гемофилию, ДВС синдром. Нормы у ребёнка:
- новорожденные 14-18 сек;
- дети до 6 лет 13-16 сек;
- 7-12 лет 12-16 сек;
- Старше 12 лет 11-15 сек.
Протромбиновый индекс представляет собой соотношение идеального протромбинового времени и результата пациента в процентах, норма которого вне зависимости от возраста ребенка составляет 70-100%.
Тромбиновое время
Раскрывает последнюю стадию свёртываемости крови – реакцию между фибриногеном и тромбином. Норма составляет 25-31 сек.
Уровень фибриногена
Белок фибриноген, образующийся в печени, является первым фактором свёртывания крови. Норма у ребенка:
- Дети до года 1,25-3 г/л;
- Старше года 2-4 г/л.
Снижение его уровня может возникать при патологиях печени, злокачественных заболеваниях крови, приёме некоторых препаратов. А повышение количества фибриногена происходит при воспалительных процессах и стрессе.
Активированное частичное тромбиновое время
АЧТВ один из наиболее значимых показателей коагулограммы, который расскажет, насколько быстро может образоваться фибриновый сгусток. В зависимости от лаборатории и используемых реактивов норма может отличаться и должна уточняться непосредственно там.
Антитромбин III
Физиологический антикоагулянт, угнетающий некоторые факторы свёртываемости и тромбин. Норма у ребенка:
- до года 45-80%
- до 10 лет 65-100%
- до 16 лет 80-100%
- старше 16 лет 75-125%
Повышение его уровня происходит при тяжёлых воспалительных заболеваниях, недостатке витамина К, а также при лечении гормональными противовоспалительными препаратами.
Наиболее частые патологии, при которых свертываемость меньше нормы
Существует ряд заболеваний, приводящих к нарушению свертываемости. В основной массе это наследственные заболевания, за ними по численности идут аутоиммунные болезни, а также сильные воспалительные процессы печени.
Гемофилия А, В и С
Лидирующее место в мире занимает гемофилия. Это наследственное заболевание, которое характеризуется дефицитом VIII, IX, XI факторов свертывания. В результате чего могут снизиться практически все показатели коагулограммы. Заболевание наследственное и болеют им преимущественно лица мужского пола.
Болезнь Виллебранда проявляется менее опасной кровоточивостью, чем гемофилия, иногда это заболевание называют «псевдогемофилия» и сосудистая гемофилия. Встречается у 1 из 10000 новорожденных. Болеют как мальчики, так и девочки, болезнь проявляется кровотечениями из носа, десен, у 65% девочек болезнь проявляется маточными кровотечениями в подростковом возрасте.
Тромбоцитопения
Чаще всего возникает при аллергических реакциях, приёме нестероидных противовоспалительных препаратов, аутоиммунных заболеваниях, химиотерапии.
Передозировка лекарственными препаратами
Наиболее частой причиной нарушения свертываемости крови является передозировка парацетамолом и ацетилсалициловой кислотой. При этом падает уровень тромбоцитов и возникают подкожные кровоизлияния, желудочные кровотечения, если не прекратить приём препарата, то возможны кровоизлияния в мозг.
Заболевания печени
Острые и хронические гепатиты, а также циррозы приводят к нарушению выработки некоторых факторов свертывания и в результате возникают кровотечения.
ДВС синдром
Наиболее опасное состояние, которое характеризуется снижением всех факторов свёртывания вплоть до их полного отсутствия. Развивается при тяжёлых бактериальных инфекциях, в большинстве случаев является осложнением сепсиса, тяжёлых травм и ожогов.
Наследственные нарушения свертывания, которые проявляются склонностью к тромбозам
Антифосфолипидный синдром: в крови детей обнаруживают антифосфолипидные антитела, волчаночный антикоагулянт. Болезнь проявляется эпизодами тромбоэмболий. Незавидна судьба девочек при этом синдроме. Им редко удается стать матерью. Молодые женщины с антифосфолипидным синдромом страдают хроническим невынашиванием.
Фактор Лейдена, дефицит Протеина C и S, дефицит антитромбина, мутации протромбина, гипергомоцистеинемия, повышенный уровень липопротеина, факторов VIII, XI все эти наследственные состояния (обозначенные общим названием – ТРОМБОФИЛИИ), могут привести к тромбозам. Правда у детей тромбозы встречаются гораздо реже, чем кровотечения. Для того чтобы у ребенка возник тромбоз, необходимы дополнительные условия – тяжелая болезнь, длительный постельный режим, внутривенные инъекции через венозный катетер и подобные условия.
Злокачественные заболевания крови, лейкоз, нефротический синдром часто осложняются тромбоэмболиям.
Если в семье кто-то из родственников умер от тромбоза, то не исключено, что и ребенок может иметь наследственные патологические гены.
В целом, в последние десятилетия частота тромбозов среди детей растет, это связано и с изменением питания, и с малой подвижностью современных детей.
Своевременное исследование крови на свертываемость помогает выявить скрытые формы заболеваний и предпринять их раннее лечение.
Вернуться к списку публикаций…
Гиполазия легких (недоразвитость легких)
Для адекватного развития легких плод должен иметь возможность совершать дыхательные движения и перемещать столб амниотической жидкости вверх и вниз по трахее и главным бронхам. Следовательно, гиполазия может возникать по следующим причинам:
- недостаточность дыхания плода (нейромышечные расстройства);
- невозможность расширять легкие (диафрагмальная грыжа, плевральный выпот);
- недостаток ликвора (маловодие) из-за почечных нарушений или нарушений шейки мочевого пузыря или продолжительной пункции околоплодного пузыря.
Младенцы с гипоплазией легких могут одновременно иметь нарушения лица и контратуры конечностей. Плацента со стороны плода должна быть внимательно исследована на amnion nodosum , который предполагает тяжелое маловодие, главным образом, синдром Поттера.
Клинические признаки
У младенцев с самого рождения развивается тяжелый респираторный дистресс с заметной гипоксией, гиперкапнией и метаболическим ацидозом. Частым осложнением является пневмоторакс. Легкие очень жесткие и движения грудной клетки очень маленькие при искусственной вентиляции. На рентгене грудной клетки диагностика гипоплазии легких может быть затруднена. Тяжелая гипоплазия легких несовместима с жизнью, а менее тяжелые формы вносят свой вклад в хроническую зависимость от вентилятора и бронхо-легочную дисплазию.
Массированное легочное кровотечение
Массированное легочное кровотечение у новорожденных имеет характерное клиническое проявление в форме сердечно-сосудистого коллапса, и связанного с ним излития из трахеи и рта окрашенной кровью жидкости. Состояние обычно фатально и встречается приблизительно в 1 случае на 1000 родов. Оно описано в связи с тяжелой родовой асфиксией, гипотермией, маленьким сроком беременности при рождении ребенка, расстройствами коагуляции и конгенитальным сердечным заболеванием. Сообщалось о легочном кровотечении, последовавшем после терапии экзогенным сурфактантом. В большинстве случаев вероятной причиной предполагался геморрагический отек легких.
Лечение
Лечение такое же, как при респираторном дистрессе (см. след. пуьликации). Однако особенное ударение необходимо сделать на следующем:
- реанимация сердечно-сосудистого коллапса восполнителями объема, такими как белки плазмы;
- лечение отека легких фруземидом и, возможно, морфином
- коррекция расстройств свертываемости крови
- если необходима искусственная вентиляция, для снижения кровотечения следует применять высокое ПДКВ.
Конгенитальная диафрагмальная грыжа
Обычно грыжа бывает заднелатерального типа (Bochdalek); 80% встречаются с левой стороны. Она образуется через дефект в диафрагме в результате устойчивого плевроперитонеального канала, обусловленного недостаточностью компонентов мускулатуры. Благодаря дефекту в диафрагме абдоминальные структуры проникают в грудную клетку, обуславливая образование грыжи. Затем происходит гипоплазия или компрессия легкого на стороне грыжи со смещением средостения к контрлатеральной стороне. Иногда имеет место гипоплазия контрлатерального легкого. Младенцы с большой диафрагмальной грыжей имеют после рождения быстро прогрессирующую дыхательную недостаточность с устойчивым цианозом. Менее острая диафрагмальная грыжа может проявиться уже в детском отделении, и сопровождаться респираторным дистрессом. Также при рутинном исследовании случайно может быть обнаружена ‘декстрокардия’ или ладьевидный живот. На аускультации легких, звуки живота могут быть слышны на пораженной стороне, если газ проникает в желудочно-кишечный тракт. При нормальном давлении легкие не будут адекватно раздуваться.
Диагноз
Большинство случаев сейчас диагностируются внутриутробно рутинным акушерским УЗИ при 17-19 неделях беременности или последующим исследованием на многоводие. Диагноз диафрагмальной грыжи подтверждается рентгеном грудной клетки. На таком рентгеновском снимке виден кишечник, заворачивающийся петлей в грудную клетку (рис. 10.9).
Рис. 10.9. Рентген грудной клетки показывает левостороннюю диафрагмальную грыжу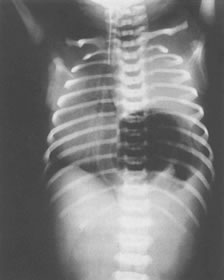
Если рентген сделан вскоре после рождения, возможно, будет затруднительно определить, находится ли кишечник в грудной клетке, особенно если в желудочно-кишечном тракте немного воздуха. Рентген должен проводится с рентгеноконтрастным катетером в желудке и должен включать брюшную полость, чтобы показать малое количество абдоминального газа. Более редкая форма диафрагмальной грыжи развивается через антеромедиальный дефект, ниже грудины (тип Morgagni ). В этом случае она обычно содержит часть толстой кишки. Как правило, симптоматика при этом отсутствует, и патология часто обнаруживается на латеральном рентгене грудной клетки.
Лечение
Если имеются подозрения на конгенитальную диафрагмальную грыжу, должен быть введен желудочный зонд (orogastric tube), и абдоминальная составляющая, находящаяся в грудной клетке, аспирируется, свободная от газа и секреции. Если ребенку требуется вспомогательная вентиляция, то она должна проводиться через эндотрахеальную трубку и никогда – с помощью мешка или маски, поскольку это может увеличивать растяжение кишечника внутри грудной клетки. Должны предприниматься меры по предотвращению разрыва контрлатерального легкого, поскольку жизнь ребенка почти исключительно зависит от вентиляции этого легкого. В соответствии с первичным диагнозом, необходимо стабилизировать состояние ребенка и вызвать детского хирурга для оперативного лечения. В более тяжелых случаях хирургическое вмешательство часто откладывается на 3-7 дней для обеспечения максимальной стабилизации состояния младенца, часто с помощью высокочастотной осциляторной вентиляции. Операция состоит из редукции абдоминальной составляющей, закрытия диафрагмального дефекта и коррекции любой мальротации кишечника.
Легочная гипертензия является обычным осложнением тяжелой диафрагмальной грыжи и, как правило, развивается вслед за послеоперационным «медовым» периодом, равным 24-48 часов. На третьи сутки у младенца развивается тяжелая гипоксия с право-левым шунтом. Для уменьшения риска осложнений рекомендуется плановая гипервентиляция, а для снижения алкалоза (рН<7.5) — инфузия бикарбоната натрия. Сульфат магния, простоциклин или толазолин может иметь значение, но вдыхаемая закись азота не имеет длительного благоприятного воздействия (см. стр. 200). В более тяжелых случаях может быть необходимым продолжение послеоперационной анестезии с параличом мышц на момент возвращения из операционной. Экстракорпоральная мембранная оксигенация имеет минимальную пользу в этом состоянии.
Прогноз
Прогноз зависит от степени легочной дисплазии и времени проявления патологии. Младенцы с респираторным дистрессом в первые 6 часов имеют высокую смертность (около 70%) , для тех, у кого она проявилась между 6 и 24 часами прогноз намного лучше (уровень смертности 10-15%). Маловероятно, что более позднее проявление респираторного дистресса связано с легочной дисплазией, и в этом случае прогноз очень благоприятный. Признаки неблагоприятного прогноза включают многоводие, устойчивый повышенный уровень РСО2 при среднем давлении в дыхательных путях > 20 см вод. ст. и гипоксия, требующая легочных вазодилатоторов.
Эзофагеальная атрезия и трахеоэзофагеальная фистула
Эзофагеальная атрезия является конгенитальной аномалией, при которой обычно полностью перекрыт просвет пищевода, в результате чего пищевод имеет форму слепого верхнего кармана. Это часто связано трахеоэзофагеальной фистулой. Наиболее часто встречаются случаи, когда верхняя часть пищевода заканчивается слепым концом (верхний эзофагеальный карман), а его нижняя часть поднимается из трахеи, выше ее киля (рис. 10.10с). Другие варианты встречается намного реже.
Рис. 10.10. Варианты трахео-эзофагеальной фистулы с или без эзофагеальной атрезией.
Тип С ответственен за 85% случаев, остальные типы в равной степени редки. 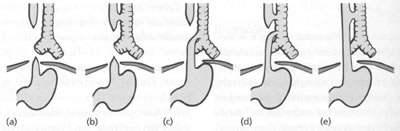
Клинические признаки
Многоводие у матери встречается в 60% случаев и в огромной степени ответственно за высокую частоту преждевременных рождений. Эзофагеальная атрезия связана с избыточной продукцией слюны и слизи, а также с высокой частотой аспирационной пневмонии. Если младенец накормлен, молоко аккумулируется в верхнем кармане и сливается в трахею. Аспирация желудочного содержимого и желчи в бронхиальное дерево приводит к легочным осложнениям с коллапсом и пневмонией. Абдоминальное растяжение происходит из-за прохождения воздуха вниз через фистулу в желудок и может развиваться очень быстро.
Возможно наличие сосуществующих конгенитальных аномалий, и они могут быть большими или незначительными. Большие аномалии включают заболевания сердца, интерстициальную атрезию, неперфорированный анус (атрезия заднего прохода) и аномалии почек. VACTERL -связь является термином, часто используемым для описания аномалий. Эта аббревиатура состоит из следующих слов : Vertebral (Позвоночный), Anal (Анальный), Cardiac (Сердечный), Tracheal (Трахеальный), ‘Esophagus’ (Пищеводный), Renal (Почечный) и Limb (Относящийся к конечностям). Наиболее важным аспектом эзофагеальной атрезии является то, что она должна быть распознана как можно скорее после рождения, предпочтительно до первого кормления, так чтобы свети к минимуму вероятность возникновения легочных осложнений. Каждому ребенку должна вводиться назогастральная трубка размером 5 через каждую ноздрю вниз в желудок вскоре после рождения. Этим методом еще до кормления может быть обнаружено большинство случаев эзофагеальной атрезии и хоанальной атрезии. Если это не практикуется, эзофагеальная атрезия в общем случае может быть распознана по избыточной секреции или цианозу и кашлю, сопровождающему кормления. Точный диагноз определяется в том случае, если невозможно провести твердый рентгеноконтрастный катетер номер 10 в желудок в связи с тем, что он задерживается на расстоянии примерно 10 см от уровня губ. Как только катетер прошел настолько далеко, насколько возможно, должен быть проведен рентген шеи и верхней части груди для подтверждения того, что он был заблокирован из-за непроходимости на этом уровне. Ренген абдоминальной области должен проинспектировать желудок на наличие газа, а с помощью ренгена грудной клетки можно оценить области спадения (коллапса). Воздух является хорошей контрастной средой в верхнем кармане. Обычно нет необходимости вводить рентгеноконтрастную среду в верхний карман для подтверждения диагноза, но если это сделано, необходимо использовать нераздражающее вещество, такое как метризимид. Для фистулы Н-типа, которая проявляется рецидивирующей аспирацией или инфекциями, радиологический диагноз может быть затруднен. Киноконтрастный глоток обычно может подтвердить диагноз.
Лечение
Младенец с эзофагеальной атрезией и трахеоэзофагеальной фистулой должен получать уход, находясь в положении лежа на спине и с приподнятым на 60° головным концом для того, чтобы избежать стекания желудочного содержимого в легкие через фистулу. Должна быть начата внутривенная инфузия и коррекция электролитов и глюкозы крови ребенка для подготовки его к операции. Операция должна проводиться детским хирургом как только ребенок адекватно реанимирован и его состояние стабилизировано. Если имеет место значительная аспирационная пневмония, то потребуются антибиотики. Операция включает разделение трахеоэзофагеальной фистулы и по возможности анастомоз двух сегментов пищевода. Иногда атретический сегмент является слишком длинным, чтобы позволить наложить первичный анастомоз, поэтому требуется эксплантация (выворачивание наружу) цервикальной части пищевода, как эзофагостомия, и желудка, как гастростомия. Определяющая операция должна проводиться в более поздние сроки.
Ребенка с цервикальной эзофагостомией необходимо стимулировать к практике сосания плацебо при одновременном гатростомическом кормлении. Часто возникают осложнения и последствия хирургического вмешательства , которые включают громкий кашель с металлическим оттенком, связанный с сосуществующей трахеомалацией, эзофагеальный стеноз, нарушение анастомоза из-за медиастинита, рецидив трахеоэзофагеальной фистулы и гастроэзофагеальный рефлюкс.
Долевая эмфизема
Конгенитальная долевая эмфизема является редкой аномалией, развивающейся из-за хрящевого дефицита долевого бронха. Эта патология наиболее часто поражает левую верхнюю долю (50%), правую среднюю долю (24%) или правую верхнюю долю (18%), и часто связана с конгенитальным заболеванием сердца (30%), таким как тетралогия Фаллота, заболевание вентрикулярной перегородки или полная аномалия венозного дренажа легких. Развитие респираторного дистресса часто происходит скрыто и незаметно, обычно в течении 2-3 недель и обусловлено коллапсом легких вокруг перераздутой доли. Средостение смещается и стенка грудной клетки выпирает над пораженной областью. Звуки дыхания ослаблены и тоны перкуссии становятся гиперрезонантными. Как только поставлен точный диагноз, в общем случае требуется лобэктомия. Приобретенная долевая эмфизема может быть вторичной по отношению к внешней или внутренней бронхиальной обструкции такой, как закупорка слизью. Этот тип эмфиземы должен лечиться консервативно физиотерапией и постуральным дренажем.
Кистозный аденоматоидный порок развития
Кистозный адемотоидный порок развития (КАПР) является редким кистозным повреждением, более часто встречающимся у мальчиков и часто обнаруживаемым на УЗИ в антенатальном периоде. Это гематомное повреждение может быть связано с многоводием, водянкой плода, преждевременными родами и мертворождением. Имеется три различных типа. Тип I КАПР (70%) представляет собой единичную или множественные кисты, заключенные в одной доле; Тип II КАПР (18%) состоит из множественных кист среднего размера, при этом в 50% таких случаев наблюдаются и другие аномалии; Тип III КАПР (10%) представляет собой грубые повреждения с равномерно распределенными небольшими кистами. Это одно из редких состояний, которое в отдельных случаях лечится хирургией плода.
Хронические легочные заболевание у новорожденных
Хроническое неонатальное заболевание легких обычно определяется как возникающее у преждевременно рожденных младенцев с признаками паренхимального заболевания легких на радиографии грудной клетки, которым требуется увеличение подачи кислорода во вдыхаемой смеси в течение более, чем 28 дней, для поддержания напряжения кислорода >60 мм рт.ст. Sherman et al. (1988) предположил, что для младенцев с очень низким весом при рождении (ОНВР) необходимость в кислороде свыше 36 недель постменструального периода матери является лучшим прогностическим признаком будущих легочных нарушений, чем потребность в кислороде свыше 28 дней с момента рождения.
Классификация различных типов хронического неонатального заболевания легких запутанна. Имеются отдельные единицы, такие как бронхолегочная дисплазия (БЛД), но многие описанные разновидности перекрываются, а у некоторых недоношенных младенцев представлены такие легочные изменения, которые не укладываются ни в одну описанную схему. В таблице 10.4 перечислена классификация хронического неонатального заболевания легких.
Таблица 10.4. Классификация
хронических легочных заболеваний новорожденных
Бронхолегочная дисплазия
Синдром Вильсона-Микити
Хроническая легочная недостаточность новорожденных
Рекуррентная аспирация:
Фарингеальная несогласованность
Гастро-эзофагеальный рефлюкс
Трахео-эзофагеальная фистула
Интерстициальные пневмонии:
Цитомегаловирус
Candida albicans
Chlamidia
Pneumocyst carinii
Ureaplasma urealyticum
Хронический отек легких из-за лево-правого шунта
Рахит недоношенных
Раньше хроническое неонатальное заболевание легких было редким явлением, но с увеличением частоты выживаемости среди чрезвычайно недоношенных младенцев это состояние становится более частым. Приблизительно 80% младенцев с весом при рождении от 501 до 750 г являются зависимыми от кислорода на 28 день; это же касается 40% младенцев с весом при рождении 751-1000 г; и 13% для тех, кто весит 1001-1500 г.
Бронхолегочная дисплазия
Это состояние обычно связано с фазой излечения (выздоровления) от тяжелого РДС, но иногда осложняет аспирацию мекония, легочное кровотечение, тяжелую неонатальную пневмонию или даже рецидивирующее апноэ. Это состояние также называется respirator lung , oxygen — toxic lung (легкое, поврежденное токсическим воздействием кислорода) и болезнь Нортвэя (Northway et al. 1967).
ЭТИОЛОГИЯ
БЛД возникает у 5% младенцев с очень низким весом и имеет многочисленные этиологические факторы. Частота связана с тяжестью РДС и степенью недоношенности. Это состояние описано только у младенцев, которые получали вентиляцию положительным давлением (этот термин используется для включения давления вдоха, давления выдоха, соотношения вдоха/выдоха и частоты) и имели объемную травму на легком. Напряжение вдыхаемого кислорода более 60% в течение длительного периода времени оказывается необходимым условием развития этого состояния, но не является его причиной. Другими вероятными факторам являются интерстициальная эмфизема и отек легких. Роль гастро-эзофагеального рефлюкса с рецидивирующей аспирацией и инфекционных агентов, таких как Ureaplasma urealyticum , не выяснена.
КЛИНИЧЕСКИЕ ПРИЗНАКИ
Младенцы, у которых развилась БЛД, имеют устойчивое западение грудной клетки, крепитацию (хруст, выявляемый при пальпации) и хрип при аускультации грудной клетки, также наблюдается сильное перераздутие легких и увеличение передне-заднего диаметра грудной клетки. У большинства этих младенцев также имеет место открытый артериальный проток, и через некоторое время может развиться право-сердечная недостаточность (corpulmonale).
РАДИОЛОГИЯ
Оригинальное описание БЛД Northway et al . установило радиологическую картину четырех степеней (Таблица 10.5).
Таблица 10.5, Рентгенологическая классификация бронхолегочной дисплазии.
| Стадия | Дни жизни | Описание | Вид на ренгеновском исследовании |
| 1 | 2-3 | Острый РДС | Генерализованная гранулоретикулярная структура, бронхограммы воздуха или «white out» |
| 2 | 4-10 | Период регенерации | Почти полное или полное затемнение |
| 3 | 10-20 | Переходный период | Небольшие кистозные инфильтраты, хроническое заболевание |
| 4 | > 4 недель | Период хронического заболевания | Гиперяркость, длинные инфильтраты наподобие нитки бус, увеличение кист. |
Первые две неотличимы от РДС и не могут служить целям описания. При большинстве тяжелых форм имеется сотовидный (пористый) вид легкого с перераздутыми легочными областями, выраженный фиброз и множественные кисты нерегулярного размера (рис. 10.11). У большинства младенцев с БЛД эти макропризнаки не развиваются, но имеют место более благоприятные, более гомогенные модели нарушений с полосками уплотнений на рентгене грудной клетки.
Рис. 10.11. Ренген грудной клетки показывает
тяжелую бронхо-легочную дисплазию. 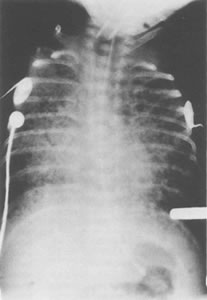
ЛЕЧЕНИЕ
Предотвращение БЛД требует внимательного ведения младенцев, находящихся на искусственной вентиляции. Легочная интерстициальная эмфизема, отек легких и открытый артериальный проток, а также избыток жидкости увеличивают риск развития БЛД. Описано быстрое закрытие препаратом индометацина, или хирургическим путем открытого артериального протока, что обуславливает застойную сердечную недостаточность. Установленная БЛД часто связана с застойной сердечной недостаточность или cor pulmonale и при этих условиях вводится ограничение жидкости, диуретиков и дигиталиса (или наперстянки). Предполагаются полезными следующие методы лечения:
- дексаметазон.
Исследования показали, что дексаметазон снижает потребность в кислороде у младенцев с БЛД. Курс этого препарата варьирует между 5 и 42 днями, но оптимальная продолжительность и время начала курса не выяснены; - диуретики.
Терапия диуретиками уменьшает интерстициальную жидкость легких, и было показано, что снижает потребность в кислороде; - терапия, направленная на снижение кислородной токсичности.
Антиоксиданты, такие как витамин Е оказываются бесполезными, но другие вещества, такие как витамин А и супероксид дисмутаза, в настоящее время оцениваются (исследуются). - вентиляция отрицательным давлением.
Помещение младенца в резервуар, который обеспечивает прерывистое отрицательное грудное давление, позволяет снизить потребность в кислороде, но этот метод пока не оценен всесторонне, как надежный метод терапии;
Адекватная оксигенация на протяжении всей дневной активности (насыщение О2 92-96%) минимизирует прогрессирование заболевания легочных сосудов. Для обеспечения оптимального роста при наличии высокого энергетического потребления, обусловленного работой дыхания, необходимо удовлетворение дополнительных нутриционных потребностей.
ПРОГНОЗ
Цифры смертности варьируют от 0 до 75 % в зависимости от того, когда был поставлен диагноз. Если диагностирована 4 стадия БЛД в то время, как младенцу по-прежнему требуется вентиляция, шанс отлучить его или ее от вентилятора маловероятен. Большинство младенцев с вылеченной БЛД имеют эпизоды одышки, часто связанные с вирусной инфекцией. Стадия выздоровления связана с продолжительным ростом легких и может занять 2-3 года. Большинство выживших младенцев не проявляют симптомов в течении 2 лет и их рентген грудной кленки остается в норме в течении 2-3 лет. Исследования функции дыхания остаются нарушенными в течение многих лет, хотя у ребенка нет никаких симптомов. Многие младенцы с тяжелой БЛД выписываются домой на непрерывной интраназальной подаче кислорода с небольшой (низкой) скоростью и с периодическим мониторингом потребности кислорода путем пульсоксиметрии.
Было показано, что дети с БЛД имеют повышенное сопротивление дыхательных путей и более подвержены тяжелому дыханию и одышке. Они также имеют повышенную реактивность дыхательных путей. Эпизоды одышки обычно наблюдаются у младенцев и детей, которые имели БЛД в период новорождения. Одышка может быть устойчива к симптомомиметику и ксантину, но стероиды могут быть эффективны.
Инфекция нижних дыхательных путей в первый год жизни имеет особенный риск для детей, которые имели БЛД в неонатальной периоде. У них наиболее вероятно развитие RSV -положительного бронхиолита, который обуславливает наиболее тяжелую дыхательную недостаточность. Антивирусный агент рибавирон (Респигам) и анти- RSV g-глобулин являются эффективными профилактическими агентами. Родителям можно посоветовать стараться не подвергать ребенка риску вирусной инфекции в первый год-два жизни.
Синдром Вильсона-Микити (нарушение созревания легких) (Northway et al. 1967)
Это состояние возникает у недоношенных детей, рожденных при менее чем 32 неделях беременности и не имеющих РДС. Патология развивается незаметно, в большинстве случаев в течении 2-3 недель и прогрессирует с увеличивающимся диспноэ, ретракцией грудной клетки и увеличением потребности в кислороде.
Первоначально рентген грудной клетки в норме, но билатеральные крупные полосатые инфильтраты с небольшими кистами начинают появляться на второй и третьей неделе. Кисты увеличиваются, и легкие становятся перераздутыми. Остеопения костей и иногда переломы ребер видны на рентгене.
ЭТИОЛОГИЯ
Этиология этого состояния у недоношенных детей неизвестна и может быть обусловлена различными инсультами, включая вирусы, хроническую аспирация молока и задержку бронхиальной секреции. Имеет место увеличивающееся нарушение распределения воздуха с дисбалансом V / Q . Частота заболевания снижается в течение последних десяти лет в то время, как частота БЛД увеличивается. Возможно, что снижение частоты синдрома Вильсона-Микити связано с увеличением использования производных ксантина для предотвращения рецидивирующего апноэ недоношенных.
РАДИОЛОГИЯ
Видны диффузные билатеральные тени, формирующие однообразную похожую на кружева картину с множественными небольшими кистами через оба легочных поля (рис. 10.12).
Рис. 10.12. На рентгене грудной клетки при
синдроме Вильсона-Микити видно тонкая сеточка. 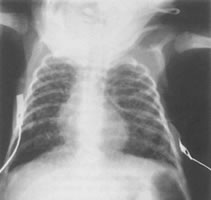
ПРОГНОЗ
Большинства младенцев выживают и обычно достигают полного клинического и радиологического выздоровления. Пострадавшим детям может потребоваться дополнительный кислород в течение месяцев прежде, чем заболевание полностью пройдет. Выжившие дети склонны к рецидивирующим эпизодам одышки, связанным с вирусной инфекцией в первые два года жизни.
Хроническая легочная недостаточность недоношенных
Это клиническое состояние обусловлено рядом патологических процессов. Под хронической легочной недостаточностью новорожденных (ХЛНН) понимают ситуацию, когда недоношенному младенцу постоянно требуется кислород или у него развивается потребность в дополнительном кислороде, кроме того, на рентгене грудной клетки у таких младенцев имеется типичная затемненная (подернутая дымкой) картина. Обычно это состояние обусловлено микроателектазами, связанными с жесткими легкими (медленно проходящий РДС), диафрагмальной слабостью или гибкой стенкой грудной клетки. Наиболее частой причиной является поздний неонатальный рахит (см. след. публикации). Недостаточное окостенение ребер совместно с определенной степенью мышечной слабости позволяет легким прогрессивно спадаться. Вирусная инфекция может обусловить такую же картину.
ЛЕЧЕНИЕ
Лечение включает распознавание и лечение рахита, если он имеет место. Для улучшения тонуса мышц могут быть эффективны ксантины, а короткий курс НПДДП применяется для раздувания спавшихся альвеол. Младенцу может потребоваться дополнительный кислород на протяжении несколько недель, но в конечном счете, он полностью выздоравливает.
Носовые кровотечения у детей. Носовое кровотечение может быть симптомом заболеваний носа и других органов. Изредка оно наблюдается и у здоровых детей. Носовые кровотечения занимают первое мксто по количеству случаев среди самопроизвольных кровотечений, они чаще возникают внезапно и могут сопровождаться значительной кровопотерей, пугающей как самого ребенка, так и окружающих взрослых. Это обусловлено обильным кровоснабжением полости носа и особенностью анатомии и физиологии в детском возрасте. Нос ребенка относительно мал, носовые ходы узкие, слизистая оболочка полости носа и носоглотки нежная, рыхлая, легко травмируется. Полость носа кровоснабжается из ветвей внутренней и наружной сонных артерий в большом количестве переплетающихся между собой в слизистой оболочке. Они образуют особое сосудистое сплетение, получившее название кровоточивая зона, или зона Киссельбаха, которое находится в передних отделах перегородки носа. Это сосудистое сплетение расположено поверхностно и в 90% случаев является источником носовых кровотечений. Местные причины носовых кровотечений. В основе носового кровотечения лежит нарушение целостности сосудистой стенки или нарушение свертывания крови. Причины носовых кровотечений разделяются на общие и местные. К местным причинам относят:
- повреждение сосудистого сплетения в перегородке носа (наиболее частая причина);
- травмы носа (от небольших механических раздражений слизистой оболочки носа пальцами до значительных, сопровождающихся переломами костей лицевого скелета);
- попадание инородных тел в полость носа. Особенно это актуально для детей младшего возраста, которые зачастую засовывают в нос различные предметы, после чего забывают об этом или скрывают от взрослых. В этом случае кровянистые выделения сопровождаются гноем и неприятным запахом;
- доброкачественные и злокачественные опухоли полости носа ( у детей наиболее часто встречаются доброкачественные);
- искривление перегородки носа, где наряду с периодическими кровотечениями в большинстве случаев будет наблюдаться затруднение носового дыхания;
- аномалии развития сосудистой системы полости носа – расширение артерий и вен различной локализации;
- изменение структуры слизистой оболочки при различных инфекциях (туберкулез, дифтерия) и хроническом насморке;
- сухой воздух в помещении. Пересохшая слизистая оболочка носовой перегородки ссыхается со стенкой кровеносного сосуда и они теряют свою эластичность и прочность. В результате чихания, сморкания пересохшая слизистая оболочка трескается и разрывает ссохшийся с ней кровеносный сосуд.
Общие причины носовых кровотечений. К причинам носовых кровотечений общего характера относятся заболевания, сопровождающиеся нарушениями свертывающих свойст крови и их сочетание с нарушением проницаемости сосудистой стенки:
- заболевания крови (например, гемофилия – врожденная патология, характеризующаяся отсутствием или дефицитом одного из факторов чвертывания крови);
- повышение проницаемости сосудов при их воспалении (васкулит), возникающие при тяжелых инфекциях, таких как корь, грипп и др.; при недостатке витамина С (гиповитаминоз С); принаследственных заболевания, характеризующихся нарушениями в строении сосудистой стенки;
- хронические заболевания печени (гепатиты, цирроз);
- хронические воспалительные заболевания полости носа и околоносовых пазух;
- состояния, сопровождающиеся подъемом артериального давления (почечная гипертензия – повышение артериального давления при заболеваниях почек, физической нагрузке, солнечном ударе, перегреве).
Как остановить кровотечение из носа.
Носовые кровотечения, как и любые кровотечения, необходимо быстро останавливать. Если кровотечение вызвано инородным телом – следует обратиться в травматологический пункт или вызвать скорую помощь. При попытках самостоятельно достать инородное тело оно может сместиться и попасть в дыхательные пути, спровоцировать удушье.
Первая помощь при носовом кровотечении:
1. Успокойте ребенка. Испуг, возникший у ребенкапри виде крови, приводит к учащению сердцебиения и подъему артериального давления, что увеличивает потерю крови. Убедите ребенка и окружающих людей, что ничего страшного не происходит, опасности для жизни нет, и кровотечение скоро прекратится.
2. Придайте ребенку вертикальное положение (посадите, максимально приподнимите спинку кровати) и слегка наклоните его голову вперед, чтобы кровь вытекала из ноздрей (лучше поставить емкость, в которую будет литься кровь). Наклон головы вперед позволит определить, из какой половины носа идет кровотечение. Это правило относится и к самым маленьким детям – их нужно взять на руки, поддерживая голову.
3. Расстегните одежду на ребенке, обеспечьте приток свежего воздуха. На область носа наложите холод (носовой платок, смоченный в холодной воде, или кусочек льда в целлофановом пакете), а ногам обеспечьте тепло. Эти действия уменьшат циркуляцию крови в области носа и ослабят, а возможно и прекратят кровотечение.
4. Прижмите рукой крыло носа к5 перегородке на стороне кровотечения и удерживайте в течение 5 – 10 минут, чтобы образовался кровяной сгусток. Если эта мера не помогает – установите в носовой ход тампон из ваты длиной 2-3 см и толщиной 0,5 см, смоченный 3% раствором перекиси водорода, или любыми сосудосуживающими каплями в нос (Санорин, Галазолин, Отривин, Тизин) или 0,1% раствором адреналина с повторнымприжатием крыла носа.
5. Во время оказания помощи контролируйте общее состояние ребенка, степень сознания, пульс, артериальное давление. После остановки кровотечения отсмаркивание и физическая нагрузка недопустимы в течение суток!
6. После прекращения кровотечения аккуратно смажьте обе половины носа вазелиновым маслом с помощью ватного тампона – это предохранит слизистую оболочку носа от пересыхания.
7. Если после предпринятых попыток самостоятельной остановки кровотечения в течение 20 минут оно не прекращается или общее состояние ребенка ухудшается необходимо срочно доставить ребенка в ближайшее медицинское учреждение или вызвать бригаду скорой помощи.
Дети с носовым кровотечением в обморочном или предобморочном состоянии, с частыми повторными носовыми кровотечениями, с кровотечением, явившимся результатом травмы, сопровождающимся головокружением, тошнотой, рвотой или с подозрением на перелом носа подлежат экстренной госпитализации в ЛОР-отделение.
Вовремя поставленный диагноз и начатое лечение позволят предотвратить неблагоприятные последствия носовых кровотечений и сохранить здоровье ребенку.




