Кровоизлияние в голове
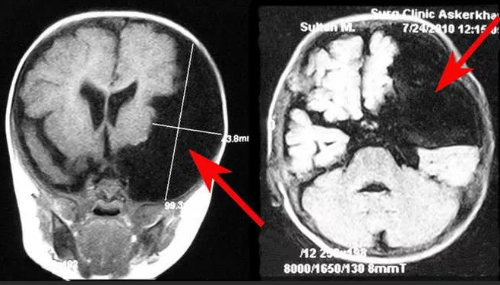
 Послеоперационное обследование глиальной опухоли головного мозга
Послеоперационное обследование глиальной опухоли головного мозга
Кровоизлияние в мозг
Кровоизлияние в мозг выражается кровотечением с попаданием крови в мозговую ткань (внутрицеребральное кровоизлияние) или же в пространство между наружной мозговой оболочкой и черепной коробкой (субарахноидальные, субдуральные, эпидуральные кровоизлияния). Все эти кровотечения могут возникать как в результате черепно-мозговых травм, так и из-за каких-либо других причин, связанных с такими заболеваниями, как системная гипертензия и других системных заболеваний организма.
Внутримозговое кровоизлияние
Внутримозговое кровоизлиянеие возникает в результате разрыва стенок мелких, снабжающих мозг, кровеносных сосудов, особенно в определенных областях головного мозга, в связи с чем, кровь из лопнутых сосудов поступает внутрь мозга и разрушает ткань головного мозга. Ежегодно, внутримозговое кровоизлияние наблюдается примерно у 12-15 пациентов из 100 000 человек. Причем этот показатель значительно выше у пациентов в возрасте старше 40 лет. Соотношение мужчин и женщин, у которых наблюдается внутримозговое кровоизлияние составляет как 1:1,67.
К факторам риска относятся артериальная гипертензия, амилоидная ангиопатия, травмы, употребление алкогольных напитков и табакокурение. Кроме того, внутримозговое излияние также могут вызывать и употребление таких лекарственных препаратов, как аспирин, нестероидные противовоспалительные средства и тромболитические препараты. С возрастом сосуды головного мозга подвержены износу и теряют свои упругие свойства. В связи с чем, стенки таких сосудов теряют свою эластичность. Утрата эластичности и износ стенок сосудов, вызванные такими заболеваниями, как амилоидная ангиопатия и гипертония способствуют разрыву сосудов и утечки крови в ткани головного мозга. Это создает накопление и образования сгустков крови, которые разрушительно воздействуют на мозговую ткань. В то же время, такое проявление, обусловленное образованием и скоплением подобных сгустков крови, нарушая систему кровообращения, способствует развитие ишемии в мозге.
Клинические симптомы чаще всего проявляются как одностороннее ослабление мышечного тонуса, головная боль и изменения в сознании. К тому же, может наблюдаться невнятность речи, судороги, тошнота и рвота.
Для установления предварительного диагноза необходимо получить подробую информацию в отношении истории болезни пациента. При постановке диагноза необходимо анализировать радиологические результаты и визуализационные изображения, полученные в ходе проведения компьютерной томографии и магнитно-резонансной томографии. При выборе метода диагностики предпочтение отдается компьютерной томографии из-за возможности точной постановки диагноза в течение короткого времени.
Для того, чтобы защитить жизненно важные функции пациента при лечении внутримозгового кровоизлияния, прежде всего необходимо обеспечить поддержку дыхательной и сердечно-сосудистой систем. После проведения анализа и определения объема кровотечения и его локализации в головном мозге, выполняется общая оценка неврологической картины пациента. Затем принимается решение, определяющее какое лечение должно быть назначено пациенту: хирургическое или медикаментазное. При хирургическом вмешательстве происходит удаление кровяной массы, скопившейся в мозговой ткани, а также остановление кровотечения. При медикаментозном лечении пациенту назначаются лекарственные препараты для снижения внутричерепного давления и уменьшения отека в области локализации кровотечения. Кроме того, чтобы предотвратить возможное появление судорог пациенту могут быть назначены противоэпилептические препараты.
Субарахноидальное кровоизлияние
Субарахноидальное кровоизлияние представляет собой кровоизлияние в субарахноидальное пространство или полость, которая расположена между паутинной и мягкой мозговыми оболочками. Оно наблюдается у 10-16 человек на 100 000 человек. К факторам риска можно отнести наследственные заболевания, табакокурение, употребление алкоголя, гипертонию, а также употребление таких лекарственных препаратов, как оральные контрацептивы, кокаин и амфетамины. Субарахноидальное кровоизлияние может произойти спонтанно, обычно вследствие разрыва артериальной аневризмы, или в результате черепно-мозговой травмы, гипертонии, атеросклероза, артериовенозных мальформаций, опухоли головного мозга, нарушения свертываемости крови, энцефалита, менингита, менингоэнцефалита, а также из-за осложнений, связанных с антикоагулянтной терапией или же в результате каких-либо других неизвестных причин.
Наиболее распространенные симптомы чаще всего проявляются в виде очень интенсивной головной боли и ригидности затылочных мышц являются. Кроме того, у пациентов может наблюдаться тошнота, рвота, головокружение, раздвоенное видение, судороги, помутнение сознания, которые сопутствуют симптомам, встречающимся и при внутримозговом кровоизлиянии. Постановка диагноза осуществляется после обследования при помощи компьютерной томографии, благодаря которой самым быстрым образом выявляется наличие кровоизлияния в мозговой ткани. После определения кровотечения требуется проведение ангиографии для визуализации сосудов головного мозга.
Если в ходе ангиографии будет выявлена аневризма, то в зависимости от области ее локализации и ее характерных свойств при помощи хирургических или эндоваскулярных методов она должна быть удалена, при этом, стенки сосуда укрепляются при помощи специального материала. Несмотря на все развития в
современной медицине, 25-30% пациентов с субарахноидальным кровоизлиянием умирает, до того, как они поступят в больницу, при этом, 30-50% оставшихся пациентов полностью излечивается.
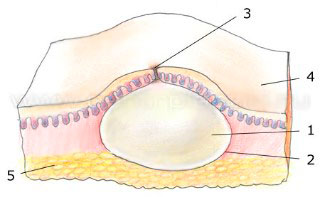
Эпидуральная гематома
Эпидуральная гематома — это скопление крови, которое возникает между внутренней поверхностью черепа и твёрдой мозговой оболочкой в результате травматического повреждения костей черепа. Причиной возникновения такой гематомы является разрыв и повреждение кровеносных сосудов твердой мозговой оболочки, которые, как правило, являются следствием травмы или перелома костей черепа. Эпидуральная гематома составляет 0,2-0,6% от всех случаев травм головного мозга. Клинически эпидуральная гематома проявляется тримя способами: в первую очередь, это светлый промежуток (lucid interval) — временное улучшение состояния пациента после черепно-мозговой травмы, за которым следует резкое ухудшение. Во втором случае, сознание полностью закрыто и не наступает какого-либо улучшения состояния, в третьем случае происходит помутнение сознания. Точный диагноз подтверждается с помощью компьютерной томографии, при этом, для диагностики также возможно использование магнитно-резонансной томографии. Но в связи с тем, что компьютерная томография дает возможность более быстрым способом получить результаты, которые имеют жизненно важное значение, а она является более предпочтительной при диагностике данного вида гематомы.
Лечение эпидуральной гематомы предусматривает отслеживание, скопившейся в области между внутренней поверхностью черепа и твёрдой мозговой оболочкой, крови и степень давления, которое она оказывает на мозговую ткань, с последующим хирургическим вмешательством. Если имеется небольшое количество скопившейся крови, за пациентом устанавливается очень тщательное наблюдение и состояние его здоровья постоянно контролируется. Если же, принимается решение о необходимости проведения хирургического вмешательства, оно должно быть реализовано в самый кратчайший срок. При хирургическом вмешательстве, скопившуюся в мозговой ткани, кровь сливают и определяя источник возникновения, останавливают кровотечение. Исход хирургического вмешательства приносит довольно блестящие результаты. Хорошие результаты достигаются в 55-89% после хирургического лечения, при этом, уровень смертности колеблется в пределах 5-29%.
Субдуральная гематома
У пациентов, перенесших травму головы, в 8-57% случаев наблюдается субдуральная гематома.Она представляет собой скопление крови, которое возникает между внутренней поверхностью черепа и твёрдой мозговой оболочкой в результате травматического повреждения костей черепа. В 50% случаев субдуральная гематома сопровождается другими различными патологиями головного мозга. В целом, пациенты поступают с серьезными неврологическими расстройствами и в 50% случаев у таких пациентов отсутствует сознание. Самые лучшие способы диагностики эпидуральной гематомы, это компьютерная томография и магнитно-резонансная томография.
Для лечения гематом, вызывающих неврологические расстройства и оказывающие давление на окружающие ткани, используется хирургическое вмешательство. При хирургическом вмешательстве, скопившуюся в мозговой ткани, кровь удаляют и определяя источник возникновения, останавливают кровотечение. Уровень смертности колеблется в пределах 42-90%, при этом, данный показатель в значительной степени выше, чем при эпидуральной гематоме.
Кровоизлияние в мозг представляет собой не что иное, как геморрагический инсульт. В последнее время распространенность этого заболевания демонстрирует тенденцию к росту. Последствия перенесенного такого инсульта, особенно обширного, бывают очень серьезными и могут приводить к смертельному исходу.
Геморрагический инсульт чаще всего развивается при разрыве артерий. Излившаяся кровь пропитывает часть мозга, поэтому такой тип инсульта называют еще кровоизлиянием в мозг. Наиболее часто геморрагический инсульт происходит у лиц, страдающих артериальной гипертонией, и развивается на фоне повышения артериального давления. В какой-то момент сосудистая стенка не выдерживает резкого подъема крови и разрывается. Более редкая причина геморрагического инсульта — разрыв аневризмы. Артериальная аневризма представляет собой, как правило, врожденное мешотчатое выпячивание на стенке сосуда. Стенка такого выпячивания тоньше стенки самого сосуда и для ее разрыва часто достаточно небольшого подъема артериального давления в стрессовых ситуациях или при физическом напряжении.
Разрыв сосуда на поверхности мозга ведет к попаданию крови в пространство, окружающее мозг (субарахноидальное пространство). Такой тип инсульта называют субарахноидальным кровоизлиянием. Самая частая его причина — разрыв аневризмы.
Симптомы инсульта:
— внезапная слабость;
— паралич или онемение мышц лица, конечностей (часто с одной стороны);
— нарушение речи;
— ухудшение зрения;
— сильная резкая головная боль;
— головокружение;
— потеря равновесия и координации, нарушение походки.
Причинные факторы кровоизлияния
Знание причинных факторов , которые могут привести к кровоизлиянию в мозг, позволит предупредить их воздействие на организм. Основными факторами являются:
- артериальная гипертензия (хроническое повышение уровня артериального давления, особенно когда лечение этой патологии отсутствует);
- сахарный диабет (состояние, которое развивается при постоянном повышении уровня глюкозы в крови, на фоне чего развиваются различные осложнения);
- сосудистые аневризмы (расширение артерии на каком-либо протяжении), которые могут быть как врожденными, так и приобретенными в течение жизни;
- травматическое повреждение сосудов головного мозга, особенно после травмы от острого предмета;
- геморрагические диатезы (состояния, которые сопровождаются повышенной ломкостью сосудистой стенки);
- бесконтрольное применение антикоагулянтов (препараты, которые предупреждают свертываемость крови). Обычно они назначаются после тромбоэмболических состояний;
- поражение сосудов амилоидом (вещество, которое откладывается в сосудистой стенке и приводит к изменению прочности сосуда);
- опухолевое поражение;
- инфекционно-воспалительный процесс в мозговой ткани (энцефалит) и другие.
Независимо от первичной причины, оказывающей воздействие на нервную ткань, происходит изменение сосудистой проницаемости в сторону ее повышения. В итоге это приводит к разрыву сосудистой стенки. Это сопровождается появлением кровоизлияния в мозг. Однако очень редко могут появляться и диапедезное внутримозговое кровоизлияние, которое характеризуются выходом форменных элементов крови и плазмы через неповрежденную сосудистую стенку. Это становится возможно в результате расширения пространств между эндотелиоцитами (клетками сосудистой оболочки). Так происходит поражение головного или спинного мозга.
Чаще всего кровоизлияния в мозг поражают большие полушария. Реже могут развиваться кровоизлияния в стволовую часть мозга или мозжечок. Геморрагический инсульт, поражающий ствол мозга, приводит к нарушению витальных функций, так как в продолговатом мозге находятся центр дыхания, центр работы сердечно-сосудистой системы и т.д. Последствия в этом случае очень серьезные. Симптомы в этом случае яркие и быстро прогрессируют. Поэтому признаки такого кровоизлияния легко диагностируются. Операция в данном случае является единственным методом спасения, но она не всегда эффективна.
Лечение геморрагического инсульта
Лечение геморрагического инсульта направлено на быстрейшую остановку кровоизлияния, образованного в мозговой артерии, а также удаление из нее тромба, который давит на мозг. В таких случаях показана нейрохирургическая операция.
Кроме того, при лечении геморрагического инсульта назначаются таблетки от повышенного давления, которые необходимо принимать строго по назначению врача.
![]() : 28.06.2016
: 28.06.2016
Каждый шестой человек с геморрагическим инсультом – кровоизлиянием в мозг, вызванным разрывом сосудов, умирает в машине скорой помощи. Риск кровоизлияния, приводящего к летальному исходу или тяжелым неврологическим последствиям, остается высоким даже после успешной операции на сосудах. Приблизиться к пониманию законов движения крови в сосудах головного мозга и методов управления кровотоком, чтобы полностью контролировать ход операций на сосудах головного мозга и свести к минимуму послеоперационные риски, позволили результаты работы большого коллектива, объединившего нейрохирургов с «фундаментальными» механиками и математиками в рамках междисциплинарного проекта «Мозг и нейронауки»
Сосудистые заболевания центральной нервной системы являются одной из основных причин смертности во всем мире, в том числе и в России. Лечение таких патологий как аневризмы и врожденная артериовенозная мальформация заключается в их полном «выключении» из кровотока, которое производится путем эндоваскулярной (внутрисосудистой) или открытой операции на сосудах мозга.
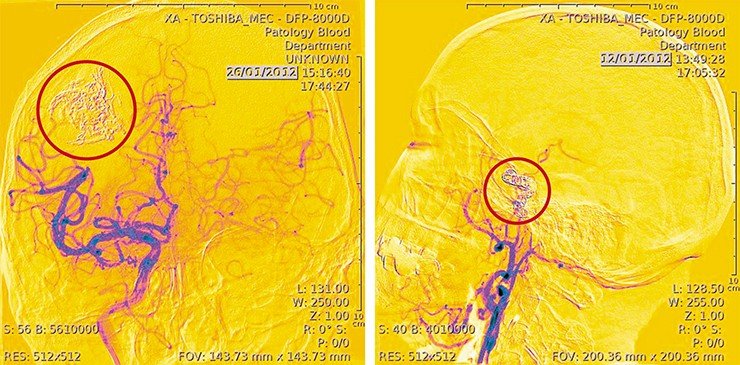
Ежегодно в России примерно у 15 человек из каждых 100 тысяч происходит разрыв аневризмы (выпячивания стенки сосудов мозга), и около 15% таких больных погибает, не успевая доехать до больницы. У половины пациентов кровоизлияние повторяется в течение последующих шести месяцев – в этом случае смертность достигает 70%
Нейрохирурги во всем мире давно оперируют подобные патологии, но проблема в том, что даже после успешной операции у пациента может произойти кровоизлияние, что значительно увеличивает риски, в том числе – летального исхода. Почему две совершенно одинаковые операции заканчиваются для пациентов по-разному? Как спрогнозировать эффективность предстоящей операции?
Именно эти вопросы привели нейрохирургов ННИИПК им. акад. Е.Н. Мешалкина к осознанию необходимости изучения механизмов образования аномалий и гемодинамики головного мозга. За помощью обратились к ученым из Института гидродинамики им. акад. М.А. Лаврентьева СО РАН. Так начались мультидисциплинарные исследования, результаты которых легли в основу новых методов лечения сосудистых аномалий.
Участники проекта РНФ «Мозг и нейронауки»: Институт гидродинамики им. М. А. Лаврентьева СО РАН, Институт теоретической и прикладной механики им. С. А. Христиановича СО РАН, ФИЦ Институт цитологии и генетики СО РАН, Международный томографический центр СО РАН, Новосибирский государственный университет, Владимирский государственный университет, Новосибирский научно-исследовательский институт патологии кровообращения им. академика Е. Н. Мешалкина, НИИ нейрохирургии им. Н. Н. Бурденко
В своих интервью корреспонденту журнала «НАУКА из первых рук» ключевые участники проекта – Кирилл Юрьевич Орлов, нейрохирург, руководитель Центра ангионеврологии и нейрохирургии ННИИПК им. акад. Е.Н. Мешалкина, и д. ф.-м. н. Александр Павлович Чупахин, заведующий лабораторией дифференциальных уравнений ИГиЛ СО РАН и заведующий кафедрой высшей математики ММФ НГУ, – рассказали о том, как дифференциальное уравнение, описывающее поведение нелинейной пружинки, погруженной в вязкую среду, и усовершенствованный русскими программистами американский прибор радикально изменили принципы нейрохирургических операций и значительно снизили риск послеоперационных осложнений.
«Кровь существует только в движении»

К. Ю. Орлов: Нейрохирурги давно имеют дело с артериальной аневризмой – выпячиванием стенки артериальных сосудов и артериовенозной мальформацией – спутанным сосудистым клубком, образующимся во время эмбрионального развития из-за ошибки в формировании сосуда. Первую операцию по «выключению» аневризмы с помощью специальной клипсы сделал американский нейрохирург Уолтер Э. Денди в начале прошлого века – так началась эра сосудистой нейрохирургии. В 1980-х гг. на смену открытым операциям на мозге пришла эндоваскулярная нейрохирургия. Начало ей положил советский профессор Ф. А. Сербиненко, придумавший специальные баллоны-катетеры – «воздушные шарики», которые через прокол в шее «добирались» до аневризмы. В 1970 г. Сербиненко при помощи баллонов-катетеров успешно провел операцию на внутренней сонной артерии. Позже баллоны Сербиненко стали применяться и для лечения аневризм и артериовенозных мальформаций.
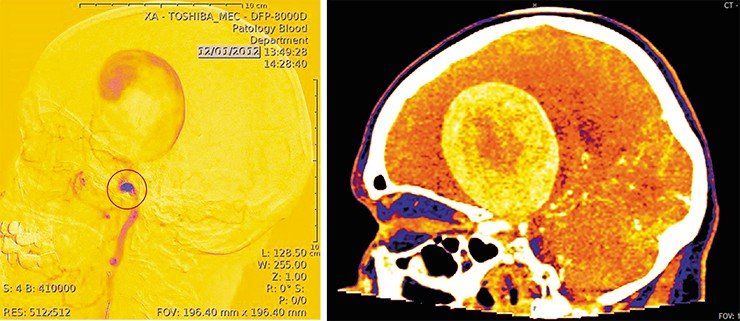
Сегодня для лечения аневризм используются совершенно другие методы: в аневризматическую полость внедряют конструкции из различных металлов (спирали, стенты), позволяющие достигать результата с минимальным числом осложнений. И хотя частота таких аномалий высока – из 100 человек примерно у 10 есть артериальная аневризма, – их можно диагностировать с помощью МРТ, а благодаря современным технологиям пациент возвращается домой уже через пару дней после операции.
Сложнее обстоит дело с артериовенозной мальформацией (АВМ), которая образуется во время эмбрионального развития из-за ошибки в формировании сосудов – выглядит она как спутанный клубок. Диагностировать ее на раннем этапе сложно, так как до определенного возраста (обычно до 30 лет) эта аномалия никак себя не проявляет. Суть лечения АВМ заключается в ее полном выключении из кровотока – эмболизации, для чего в патологические сосуды вводят специальные вещества, «заклеивающие» аномалию. Раньше части АВМ «отключали» по очереди, но недавно появился препарат Onyx, который позволяет полностью выключать аномалию введением эмболизата в один из сосудов. Прекрасный препарат, если бы частота кровоизлияний во время и после такой операции не оказалась такой высокой – от 2 до 16,7%.
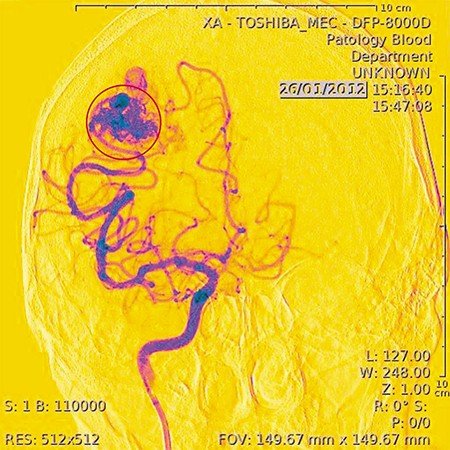 Наше сотрудничество с Институтом гидродинамики СО РАН началось с поиска ответов на вопросы, которые встали перед нами при лечении именно этой патологии. Дело в том, что по АВМ идет очень большой поток крови, но до мозга он не доходит и сбрасывается в вены – так аномалия «обкрадывает» головной мозг. Чтобы восполнить потери, рядом с аномалией формируются новые сосуды, которые питают мозг. И когда врач полностью выключает АВМ, весь кровеносный поток устремляется по этим сосудам, которые рвутся, потому что они не готовы к такому напору. Так возникают послеоперационные кровоизлияния. Поэтому первый вопрос касался объема аномалии, который допустимо «выключить» за одну операцию – 10, 15, 30%?
Наше сотрудничество с Институтом гидродинамики СО РАН началось с поиска ответов на вопросы, которые встали перед нами при лечении именно этой патологии. Дело в том, что по АВМ идет очень большой поток крови, но до мозга он не доходит и сбрасывается в вены – так аномалия «обкрадывает» головной мозг. Чтобы восполнить потери, рядом с аномалией формируются новые сосуды, которые питают мозг. И когда врач полностью выключает АВМ, весь кровеносный поток устремляется по этим сосудам, которые рвутся, потому что они не готовы к такому напору. Так возникают послеоперационные кровоизлияния. Поэтому первый вопрос касался объема аномалии, который допустимо «выключить» за одну операцию – 10, 15, 30%?
Следующий вопрос – с каких сосудов начинать эмболизацию? Клубок АВМ состоит из сосудов разного диаметра: здесь и большие фистулы – трубки диаметром несколько миллиметров, и среднесосудистая часть – диаметром меньше миллиметра, и «ниточки». В сосудах разного диаметра кровь течет с разной скоростью. Нейрохирурги чаще начинают с мелких сосудов – правильно ли это?

После процедуры эмболизации пациента отпускают на полгода. Практика показывает, что за этот период кровоснабжение полностью перестраивается. Но за эти же полгода у 2% пациентов происходит кровоизлияние – как избежать этого? Как определить, когда закончился процесс перестройки гемодинамики?
Медицина не такая точная наука, как математика, часто врачам во время операций приходится импровизировать, изменять намеченный сценарий. Чтобы ответить на эти вопросы, нам нужны были точные данные, понимание механики гемодинамики при аномалиях в цифрах – совместно с коллегами-математиками их удалось получить.

А. П. Чупахин: Рассматривать работу головного мозга как механическую – очень непривычно. Только задумайтесь: весь сложный каскад молекулярных, биологических и физиологических действий, которые позволяют нам поднять руку при встрече, отвечают за наше понимание точных наук и любовь к музыке, – все это запускается кровотоком в головном мозге.
Кровь – очень загадочная субстанция, существующая только в движении. Когда кровь останавливается, она перестает быть кровью. А останавливается она тогда, когда нарушается целостность сосудов: малейший перебой в кровоснабжении одной из зон головного мозга приводит к отключению жизненно важных функций, потере речи, частичному параличу. К счастью, мозг очень пластичен и способен включать резервные сосудистые системы, но и врачам нужно действовать быстро, а для этого они должны понимать, как идут процессы гемодинамики в норме и при патологии.
В общем виде задача, которую перед нами поставили, звучала так: есть две операции, похожие по своим внешним результатам (рентгенологическим снимкам с контрастным веществом), но с различными клиническими исходами. Требуется определить причины возникших осложнений и найти параметры, которые определяют безопасность хирургического лечения у пациентов со случайно выявленными аномалиями сосудов головного мозга.
Важно, что в наших дискуссиях сразу было достигнуто понимание, что если не будет экспериментальных клинических данных о том, как происходит течение крови, если мы не будем проводить мониторинг во время операций, то прийти к конечной точке – созданию единой модели, описывающей течение крови в сосудах мозга, – не получится. Да, можно будет написать интересные академические статьи о компьютерном моделировании движения крови в сосудах головного мозга, но все это вряд ли окажет влияние на хирургическую практику.
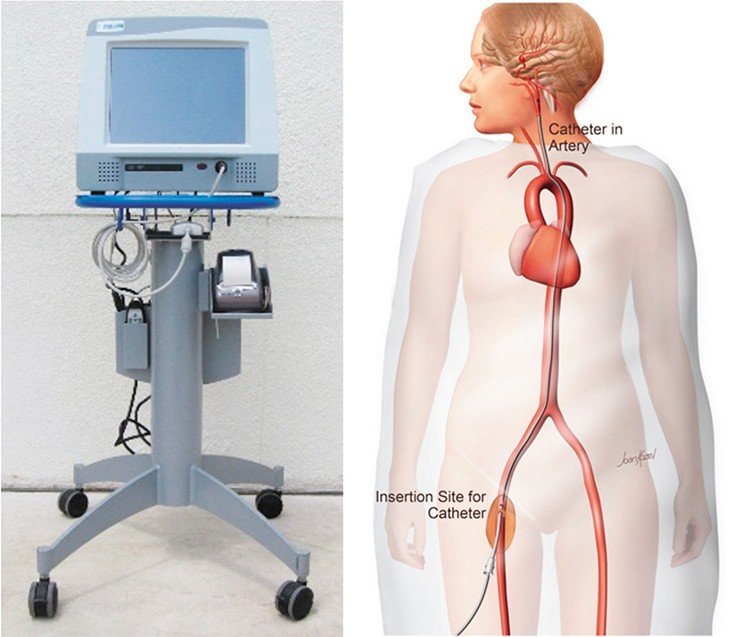
Для мониторинга гемодинамики в сосудах головного мозга был приобретен прибор ComboMap американского производителя Volcano. Вообще-то этот прибор предназначен для измерений давления и скорости кровотока в коронарных сосудах, и инженеры компании, приехавшие устанавливать прибор, сильно удивились, узнав, что мы собираемся его использовать для измерения скорости и давления кровотока в сосудах головного мозга – «ох уж эти беспокойные русские ученые!».
Однако вопреки их скепсису нам удалось усовершенствовать первоначальное программное обеспечение и, в конечном счете, создать новый приборно-измерительный комплекс для эндоваскулярного интраоперационного мониторинга.
Датчик прибора – очень тонкий, волосовидный, позволяет с высокой точностью измерять давление и скорость потока крови в сосудах диаметром более 1,5 мм. Измерения давления и скорости движения крови проводились до и после операции в одних и тех же точках, расположенных на различных расстояниях от аномалии. Это позволило получить точные качественные свойства и количественные параметры кровотока, сопутствующие аномалии. На основе этих данных, была создана математическая модель кровотока головного мозга, которая позволяет предсказывать, что будет с сосудами при тех или иных показателях.
Нами был разработан и внедрен аппарат диаграмм «давление – скорость» и «расход – поток энергии», позволяющий характеризовать тип сосудистой аномалии по гемодинамическим параметрам и отслеживать эффективность операции. На данный момент такой мониторинг является уникальным не только в России, но и в мире.
Параметры, которые мы получаем на нейрохирургических операциях, – это параметры кровотока очень сложной системы: пульсирующий нестационарный поток крови в сосуде, упругие стенки которого помогают течению, и погружены они в гелеобразное вещество мозга, помещенного в твердую мозговую оболочку и черепную коробку. Такие параметры с потолка не возьмешь. Мы видим на графиках, что пульсация скорости и давления являются практически периодическими функциями. Почти, потому что на самом деле имеется несколько периодических процессов: это и пульсации сердца, которые обусловливают движение крови, это и колебательный характер дыхательных процессов и др. Говоря упрощенным языком, человек – это система связанных осцилляторов, колебательных контуров.
Уравнение гармонического осциллятора – широко употребительная модель, которая используется во многих разделах физики. А вот как связаны осцилляторы сердца, дыхательного цикла, пищеварения? Эту связь обнаружить трудно. Мы исходили из того, что начинать нужно с простой модели единого осциллятора. Так должно быть и с точки зрения здорового организма: раз все работает «как часы», система не должна быть сложной.
Появилась идея использовать для моделирования кровотока в сосудах головного мозга дифференциальное уравнение, описывающее нелинейный осциллятор Ван дер Поля-Дуффинга. Фактически, это описание нелинейной пружинки, которая по-разному работает на растяжение и сжатие, и погружена в вязкую среду. Казалось бы, как такая простая математическая модель объяснит то, что происходит в голове, в этой сложной субстанции? Но, несмотря на свою внешнюю простоту, это уравнение имеет широкое многообразие решений и позволяет измерять и оценивать важные свойства всех компонентов сложной среды: пульсирующий поток крови, упругие стенки сосуда и окружающую среду мозга. Уравнение позволяет учитывать то, какими свойствами обладает упругая среда, как устроена пружина, которая колеблет эту среду, и какими вязкими свойствами обладает эта среда.
Модель нелинейного осциллятора хорошо моделирует поведение кровотока в окрестностях сосудистой аномалии и может показать, к чему это приводит. Когда мы увеличиваем параметры кровотока на модели, то в результате расчетов видим, что произойдет с организмом в реальности. Оказалось, что отклонения в организме человека не могут быть произвольными, есть определенная цепочка образцов «поведения», которая при развитии аномалии приводит к потере периодических решений, к потере колебаний, к сбою кровотока. Это одна из моделей, есть и другие – наша работа продолжается.
«Риск сведен до минимума»
К. Ю. Орлов: Результатом работы врачей и ученых-гидродинамиков стала разработка нового алгоритма эндоваскулярного лечения АВМ. Его суть в том, что при аномалии средних и крупных размеров лечение должно быть поэтапным, причем за одно вмешательство не следует выключать более 60% объема АВМ.
На примере локальной модели гипотетической АВМ были рассмотрены различные сценарии ее эмболизации, чтобы понять, какие сосуды нужно закрывать в первую очередь. Оказалось, что если хирург сначала выключает мелкие «составляющие» аномалии, то увеличивается поток по фистуле и по «здоровым» сосудам рядом с аномалией на весь объем, который шел по мелкой сети. Последующее выключение самого большого сосуда делает нагрузку на «резервную» систему непосильной. Работа с гемодинамической моделью помогла понять, что начинать эмболизацию нужно с самого крупного сосуда, и лишь когда кровяной поток перераспределится, идти дальше. Этот принцип упрощает работу нейрохирурга: теперь он знает, какой сосуд из спутанного клубка выключать первым.
Не менее важным результатом стало понимание того, сколько времени требуется на перестройку кровообращения после операции – то есть, когда можно приглашать пациента для следующего этапа эмболизации. Оказалось, что не нужно ждать «классических» шести месяцев, кровообращение перестраивается уже через неделю. Это очень важно, потому что в течение года после операции у 4% пациентов случается кровоизлияние, значит, отпуская пациентов на полгода, мы рискуем 2% жизней. Если же промежуток между операциями составляет неделю, риск сводится до минимума.
С появлением гемодинамической модели удалось решить и некоторые проблемы, связанные с лечением артериальных аневризм. Зачастую к нам поступают пациенты с несколькими аневризмами, и встает вопрос – у какой из них вероятность разрыва больше? Оценив поведение параметра «скорость-давление» для каждой из них, легко понять, от какой нужно избавиться в первую очередь. А благодаря мониторингу во время операций мы может сразу оценивать результаты наших действий и менять тактику по ходу операции. Если, к примеру, установки одного стента окажется недостаточно, можно поставить спираль или дополнительный стент. Так мы не подвергаем пациента дополнительному риску повторной операции.
Математики помогли нам решить и проблему, связанную с так называемыми бифуркационными аневризмами – сосудистыми «тройниками», как называет их Александр Павлович Чупахин, которые образуются на месте расхождения сонных артерий. После видимого успешного лечения такая аномалия очень часто возвращается в свое первоначальное состояние.
Оказалось, что все дело в величине угла между сосудами. Когда мы закрываем аневризму спиралями, в этих углах могут образовываться дочерние вихревые потоки, которые вызывают сужение артерий, не заметное на ангиограмме. Поток крови по сосудам затрудняется, а у шейки аневризмы – увеличивается, аномалия снова начинает расти. Чтобы избежать этого осложнения, мы теперь ставим стенты таким образом, чтобы паразитарные потоки не образовывались.
Ежегодно в Новосибирском научно-исследовательском институте патологии кровообращения им. академика Е. Н. Мешалкина оперируют 350 человек с артериовенозными мальформациями. Благодаря применению новых операционных протоколов удалось значительно снизить риск послеоперационных кровоизлияний: в 2015 г. с 10% до 3%
Своими результатами мы делимся с коллегами по всему миру, но нужно понимать, что в медицине не всегда есть место золотым стандартам – у разных клиник свой формат работы, у разных хирургов свои предпочтения. Хорошего результата можно добиться разными способами. Есть приверженцы открытых операций на головном мозге, кто-то просто удаляет аномалию. Как оценивает результат хирург? Ушел пациент на своих ногах – значит, все хорошо, но есть еще качество жизни, на котором может отразиться даже шрам на голове. Например, в США после успешно проведенной открытой операции по удалению АВМ около 14% американцев теряют работу, а после эндоваскулярных – всего 2-3%.
А. П. Чупахин: Мы начали эту большую работу для того, чтобы понять законы движения крови в сосудах головного мозга и для того, чтобы научиться управлять кровотоком. Задача довольно амбициозная, и решить ее силами специалистов одного профиля невозможно. Нам удалось создать коллектив из хирургов, биологов, физиологов, механиков и математиков и достигнуть результатов удалось во многом благодаря включению наших исследований в проект РНФ «Мозг и нейронауки». Результаты работ по мониторингу нейрохирургических операций, поддержанные грантом РФФИ, стали основой для развития и других направлений.
При содействии Международного томографического центра СО РАН мы создали физическую модель сосудов, выполненную из упругих материалов, имитирующих реальные ткани, по которым с помощью специального насоса движется жидкость (вода+глицерин), имитирующая кровь. Для визуализации этого движения используется магнитно-резонансный томограф. Эксперименты на моделях кровеносных сосудов позволяют получить ответ, а значит и предсказать последствия различных воздействий на сосуды, что нельзя сделать при реальных операциях. Например, проверить, как увеличится скорость кровотока, если повысить давление на 10 мм ртутного столба или больше. Такие исследования интересны и с точки зрения фундаментальной и прикладной гидродинамики, так как позволяют многое узнать о течении жидкости в упругих средах. Математическое моделирование таких сложных систем – дело будущего, в России же подобные эксперименты больше нигде не проводятся.
Еще одна грань наших работ – изучение влияния гемодинамики на физиологические и интеллектуальные возможности человека. Вместе с коллегами из Института цитологии и генетики СО РАН мы строим компьютерный образ сети кровеносных сосудов головного мозга лабораторных животных-моделей, чтобы при помощи выработанного нами алгоритма отслеживать различия гемодинамики головного мозга у разных особей одного и того же вида, различающихся физиологическими и поведенческими характеристиками. Все расчеты проводятся на базе Информационно-вычислительного центра НГУ в программном комплексе ANASYS
В конечном счете все, что мы делаем сегодня, должно привести к построению исчерпывающей математической модели гемодинамики головного мозга. Описывать кровоток головного мозга с помощью уравнений – фантастически сложная задача, выходящая за рамки возможностей современной математики, гидродинамики и механики. Конечно, никто не ждал и не ждет от нас создания супермодели, которая объяснит все. Мы работаем в рамках нескольких моделей: наше преимущество в том, что они создаются на основании клинических экспериментальных данных, а не абстрактных рассуждений.
Сегодняшний день замечателен тем, что у нас есть возможность решать такие мультидисциплинарные задачи. Какое-то время назад наука была разделена «перегородками»: каждый занимался своим делом, иногда встречаясь с коллегами и обсуждая результаты. Сегодня эти перегородки стираются, и мы, математики по образованию и механики по роду деятельности, работаем в коллективе, который проводит полный цикл исследований – от получения клинических данных и их обработки до создания математических моделей и «возвращения» результатов в виде рекомендательных протоколов в клинику.
Сегодня такие точные науки, как математика, физика, механика выходят из-за письменного стола и начинают работать в «живых» системах. И это очень хорошо, ведь разные парадигмы исследований могут привести к самым неожиданным результатам. Не менее важно и то, что огромный интерес эта тематика вызывает у молодежи – например, к нам в институт на специализацию приходит много толковых студентов из НГУ. Их привлекает комплексный характер нашей работы, связанный с решением «живых задач», которые имеют реальный выход на практику.
Подготовила Татьяна Морозова


.png)