Капли от цистита канефрон
В настоящее время отмечен явный рост интереса к проблемам фитотерапии, т. е. лечению лекарственными средствами растительного происхождения. Фитотерапия имеет давнюю историю, первые упоминания относятся к XXVII веку до н. э. и пришли к нам из древнего Китая. На сегодняшний день эффективность применения лекарственных растений доказана не только опытным путем, но и с помощью научно обоснованных методов — биохимических, биологических (на молекулярном и клеточном уровне), а также структурно-аналитических.
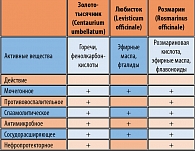 Таблица 1. Лекарственные растения, входящие в состав Канефрона Н, и спектр их действия
Таблица 1. Лекарственные растения, входящие в состав Канефрона Н, и спектр их действия  Таблица 2. Результаты цистоскопии у больных хроническим циститом (n=48)
Таблица 2. Результаты цистоскопии у больных хроническим циститом (n=48)  Таблица 3. Динамика жалоб у больных из группы А (n=20) через 10 дней лечения
Таблица 3. Динамика жалоб у больных из группы А (n=20) через 10 дней лечения  Таблица 4. Динамика жалоб у больных из группы Б (n=28) через 30 дней после окончания курса инициальной терапии
Таблица 4. Динамика жалоб у больных из группы Б (n=28) через 30 дней после окончания курса инициальной терапии
Современная медицина научилась работать с растениями и использовать их потенциал. Так, появилась возможность получения экстрактов, в состав которых входят определенные действующие вещества в точно подобранных пропорциях. Это обеспечивается благодаря тщательному возделыванию культур и применению специальных методов изготовления лекарственных средств. Изучение мира растений позволяет создавать фитопрепараты, наиболее полно отвечающие потребностям современной медицины. Сегодня фитотерапия особенно привлекательна, так как на многих примерах показано, что экстракты лекарственных растений ни в чем не уступают по эффективности химическим веществам, а часто даже превосходят их. К фитопрепаратам больше не относятся, как к препаратам второго сорта. Каждый из них имеет собственный профиль. Об их клинической значимости говорит тот факт, что крупнейшие фармакологические предприятия, десятилетиями производившие только синтетические препараты, буквально прочесывают леса в поисках целебных растений.
Современные растительные препараты производятся с применением высоких технологий и проходят многоступенчатый контроль качества. Одним из фитопрепаратов нового поколения, широко применяемым в урологии, является КанефронâН (Bionorica, Германия).
КанефронâН – комбинированный препарат, в состав которого входят золототысячник (Centaurium umbellatum), любисток (Levisticum officinale) и розмарин (Rosmarinus officinale). Входящие в состав препарата вещества оказывают антисептическое, спазмолитическое, противовоспалительное действие на органы мочевой системы, уменьшают проницаемость капилляров почек, обладают диуретическим эффектом, улучшают функцию почек, потенциируют эффект антибактериальной терапии (см. таблицу 1).
Различные виды действия КанефронаâН обусловлены входящими в его состав эфирными маслами, фенолкарболовыми кислотами, фталидами, горечами. Например, диуретическое действие препарата обусловлено сочетанием различных точек приложения его компонентов. Эфирные масла расширяют сосуды почек, что способствует улучшению кровоснабжения почечного эпителия, а также оказывают влияние на процессы обратного всасывания клетками почечных канальцев. Это проявляется главным образом в уменьшении реабсорбции ионов натрия и соответствующего количества воды. Диуретическое действие фенилкарбоновых кислот объясняется осмотическим эффектом: при попадании в просвет почечных канальцев они создают высокое осмотическое давление (обратному всасыванию эти вещества не подвергаются); при этом значительно снижается реабсорбция воды и ионов натрия. Таким образом, увеличение выведения воды происходит без нарушения ионного баланса (калий-сберегающий эффект).
Спазмолитический эффект обусловлен флавоноидной составляющей препарата. Аналогичное действие проявляют фталиды (любисток) и розмариновое масло. Слабыми спазмолитическими свойствами обладают фенолкарбоновые кислоты (1-4).
Противовоспалительный эффект в основном обусловлен наличием розмариновой кислоты, которая блокирует неспецифическую активацию комплемента и липооксигеназы с последующим угнетением синтеза лейкотриенов. Как и другие фенольные соединения, розмариновая кислота проявляет антиоксидантное действие и прерывает свободнорадикальные цепные реакции.
Все лекарственные растения, входящие в состав КанефронаâН, содержат вещества, обладающие широким антимикробным спектром действия: фенолкарболовые кислоты влияют на бактериальный белок; эфирные масла разрушают цитоплазматическую мембрану бактерий и уменьшают активность аэробного дыхания, что приводит к уменьшению выделения энергии, необходимой для синтеза различных органических соединений; флавоны, флавоноиды и флавонолы способны связываться с белками клеточной стенки и разрушать клеточные мембраны бактерий. Это обеспечивает активность препарата даже при устойчивой к синтетическим средствам микрофлоре.
Достоинством КанефронаâН является также сочетание противомикробного и противовоспалительного эффектов, что особенно ценно при хронических процессах в мочевыводящих путях. Кроме того, выделение органических фенолкарбоновых кислот и их глюкуронидированных и сульфатированных метаболитов с мочой приводит к изменению ее кислотности, что противодействует росту бактерий. Помимо перечисленных свойств элиминации бактерий из мочевых путей способствуют следующие факторы:
- биофлавоноиды тормозят бактериальную гиалуронидазу и таким образом ограничивают распространение бактерий в тканях;
- диуретический эффект препятствует адгезии микроорганизмов.
Установлено, что КанефронâН усиливает выведение солей мочевой кислоты. Эта сторона действия лишь отчасти связана с мочегонным эффектом и довольно специфична. Усиление выделения мочевой кислоты препятствует выпадению в мочевыводящих путях кристаллов, росту имеющихся камней и формированию новых. Также было отмечено, что данный препарат подщелачивает мочу, если она резко кислая, и поддерживает значение рН в пределах 6,2-6,8, что также препятствует образованию уратных камней.
Фармакологически доказанное действие КанефронаâН на тубулярный аппарат почки четко показывает, что выделение белка с мочой из-за ранее перенесенных патологических процессов, повреждающих тубулярный аппарат, значительно снижается.
Материал и методы
В урологической клинике ММА им. И.М. Сеченова было обследовано 55 женщин, страдающих хроническим циститом, в возрасте от 18 до 45 лет. Длительность заболевания на момент обращения составляла от 3 месяцев до 15 лет (у большинства больных – от 1 года до 3 лет).
При обследовании больных применялись следующие методы:
- сбор анамнеза, физикальное обследование;
- микроскопическое исследование мочи и мочевого осадка;
- бактериологическое исследование мочи;
- анализ мазков из влагалища и цервикального канала на наличие специфических возбудителей (методами ПЦР и ПИФ) и общую чистоту;
- ультразвуковое исследование органов мочевой системы;
- экскреторная урография с нисходящей цистографией;
- цистоскопия.
Сопутствующих заболеваний (камней, кист, опухолей, пороков развития) органов мочевой системы не было выявлено ни в одном из случаев.
С помощью ПЦР и ПИФ у 7 больных были обнаружены специфические возбудители: у 2 больных была выявлена Clamydia trachomatis, у 2 больных – Mycoplasma hominis, у 3 больных – Ureaplasma urealiticum. Эти больные были исключены из последующего анализа.
Дальнейшее обследование проводилось у 48 больных.
При бактериологическом исследовании мочи в большинстве (52%) случаев (у 25 больных) выявлялась Escherichia coli. У 18 (37,5%) больных результаты посева мочи были отрицательными; у 5 (10,5%) больных были обнаружены другие возбудители – Proteus spp., Enterococcus spp., Staphylococcus spp.
Результаты цистоскопии представлены в таблице 2. Учитывая, что у многих больных выявлено сочетание различных изменений слизистой оболочки мочевого пузыря, итоговый показатель превышает 100%.
Таким образом, у большинства (79,1%) обследованных нами больных имелся шеечный цистит; другие отделы мочевого пузыря были вовлечены в патологический процесс значительно реже (в 20,9% случаев).
Во время цистоскопии патологических новообразований мочевого пузыря не было выявлено ни у одной из больных.
Оставшиеся 48 больных были подразделены на 2 группы с учетом наличия пиурии.
В группу А вошли 20 больных, количество лейкоцитов в анализе мочи у которых превышало 10 (от 10 до 20) в поле зрения. В группу Б вошли 28 больных, пиурия у которых отсутствовала.
Каждая из групп была дополнительно разделена на 2 равные подгруппы в зависимости от применения препарата КанефронâН. В подгруппы были включены больные, сравнимые по своим характеристикам (возрасту, анамнезу, клиническим проявлениям и т. д.).
Больные из подгруппы А1 (n=10) получали фосфомицин (монурал) по 3 г с интервалом 24 часа – всего 2 приема.
Больные из подгруппы А2 (n=10) получали фосфомицин (монурал) по описанной выше схеме в сочетании с приемом КанефронаâН по 2 драже 3 раза в сутки в течение 30 дней.
Больным из подгруппы Б1 (n=14) был проведен инициальный курс лечения, включавший противовоспалительные средства, препараты, улучшающие кровоток, местную терапию и физиотерапевтические процедуры, в течение 10 дней. Затем проводилось динамическое наблюдение в течение 1 месяца, в течение которого никакие дополнительные препараты не назначались.
Больным из подгруппы Б2 (n=14) был проведен аналогичный инициальный курс лечения. Однако в течение последующих 30 дней они получали КанефронâН по 2 драже 3 раза в сутки.
Контрольное обследование больных из группы А проводилось двукратно – через 10 и 30 дней после начала лечения. Критерии оценки: клинические проявления, наличие пиурии, наличие бактериурии.
Контрольное обследование больных из группы Б проводилось через 30 дней после окончания курса комплексной инициальной терапии. Критерии оценки – клинические проявления. Учитывая, что все 18 больных с отрицательными результатами бактериологического исследования мочи вошли в группу Б, а у оставшихся 10 больных возбудитель высевался в низких титрах (103-104 КОЕ/мл), наличие бактериурии не рассматривалось в качестве критерия оценки эффективности лечения.
Результаты и обсуждение
Результаты лечения больных из группы А После проведенного лечения у большинства больных из группы А наступило клиническое (см. таблицу 3) и лабораторное улучшение различной степени выраженности.
В подгруппе А1 пиурия через 10 дней лечения отсутствовала у 9 (90%) больных, в то время как в подгруппе А2 – у 100% больных.
При бактериологическом исследовании мочи, проведенном через 10 дней, исходно выделенный возбудитель был обнаружен только у 1 больного из подгруппы А1; в подгруппе А2 результаты посева мочи были отрицательными в 100% случаев.
Сходные результаты были получены через 30 дней. У всех больных, принимавших КанефронâН, клинические проявления заболевания отсутствовали, в то время как у 3 (30%) больных, получавших монотерапию фосфомицином (монуралом), они были выражены в той или иной степени. Пиурия по-прежнему не выявлялась у 100% больных из подгруппы А2. В подгруппе А1 повторное повышение количества лейкоцитов в моче было отмечено у 3 (30%) больных.
Таким образом, становится очевидным, что, несмотря на достаточно высокую лабораторную эффективность фосфомицина (монурала), достигающую 90%, добавление к терапии КанефронаâН, повышает клиническую эффективность лечения с 70 до 100% (при длительном приеме препарата). Вероятно, это связано с комплексным антимикробным, противовоспалительным, спазмолитическим и диуретическим эффектом последнего. Потенцируя действие фосфомицина (монурала), КанефронâН обеспечивает дополнительный противовоспалительный и симптоматический эффект, который сохраняется и после прекращения активной антибактериальной терапии. Кроме того, оказалось, что длительный прием КанефронаâН обеспечивает устойчивый противорецидивный эффект, о чем свидетельствует отсутствие клинических и лабораторных проявлений цистита через 30 дней лечения.
Результаты лечения больных из группы Б
После проведенного курса инициальной терапии клиническое улучшение наступило у 25 (89%) больных – 13 (92,8%) больных из подгруппы Б1 и 12 (85,8%) больных из подгруппы Б2.
Через 30 дней наблюдения жалобы по-прежнему отсутствовали или были выражены незначительно у 10 из 14 (71%) больных, не получавших поддерживающей терапии КанефрономâН. У 3 (21%) больных, несмотря на достигнутый ранее положительный эффект, было отмечено повторное развитие клинической картины цистита (см. таблицу 4).
Что касается больных из подгруппы Б2, получавших поддерживающую терапию КанефрономâН, то через 30 дней жалобы отсутствовали у 13 из 14 (92,8%) больных (см. таблицу 4).
Таким образом, прием КанефронаâН не только способствовал поддержанию достигнутого ранее эффекта, но и дополнительно повышал эффективность инициальной терапии на 7%. В общем, через 30 дней наблюдения эффективность лечения с применением КанефронаâН была выше эффективности терапии без приема данного препарата на 21,8%.
По-видимому, в отсутствие выявляемого возбудителя (или при выявлении его в низких титрах) и пиурии эффективность применения КанефронаâН обусловлена его противовоспалительным, спазмолитическим и диуретическим эффектом, что делает целесообразным применение данного препарата с целью профилактики рецидивов хронического цистита после достигнутого клинического улучшения, а также для повышения эффективности курса инициальной комплексной терапии.
Следует отметить, что в процессе применения КанефронаâН в группах А и Б не было зарегистрировано ни одного случая развития побочных эффектов или непереносимости препарата.
Результаты нашего исследования свидетельствуют о том, что:
- применение фитопрепарата КанефронâН в комплексной терапии хронического цистита не только повышает эффективность инициальной терапии (антибактериальной или комплексной, проводимой в отсутствие пиурии), но и способствует достижению более длительной ремиссии заболевания;
- длительный прием КанефронаâН не сопровождается развитием побочных эффектов.
Таким образом, КанефронâН следует рекомендовать к широкому применению у женщин, страдающих хроническим циститом.
Канефрон – препарат, который обладает противовоспалительным, спазмолитическим, антисептическим и диуретическим действиями, направленный на лечение мочекаменных болезней.
Содержание
Состав
Препарат «Канефрон» содержит активные биологически вещества, обладающие антибактериальным действием (фенол карбоновые кислоты, эфирные масла и другие биологически активные компоненты растений) действующие вещества: 1 таблетка содержит высушенные лекарственные растения в виде порошка:
-
травы золототысячника – 18 мг,
-
корня любыстка – 18 мг,
-
листья розмарина – 18 мг
Дополнительные вещества: крахмал кукурузный, кремния диоксид коллоидный безводный; повидон, магния стеарат железа оксид красный рибофлавин, кальция карбонат; декстрин; глюкозы сироп; воск горный гликолевый; масло касторовое; сахароза; шеллак; тальк титана диоксид.
Лекарственная форма
Круглые выпуклые таблетки, покрытые оболочкой оранжевого цвета с гладкой поверхностью. Капли Канефрон содержат те же растительные экстракты, по 0,6 грамм каждого в 100 г продукта. Капли содержат этанол (19% от общего объема). Они отличаются темным цветом, резковатым, но приятным ароматом и горьковатым привкусом.
Показания
Применяется при комплексной терапии острых и хронических инфекций мочевого пузыря (цистита) и почек (пиелонефрита), а также в качестве средства, препятствующего образованию камней в почках. Такой список показаний обусловлено составом препарата, в который входят лекарственные растительные вещества с антисептическим, диуретическим, спазмолитическим и противовоспалительным действиями. Профилактика образования мочевых камней, также и после их удаления.
Препарат выписывается для:
-
борьбы с воспалением и спазмами;
-
для содействия удалению микроорганизмов из мочевых путей и уменьшению боли при цистите;
-
для уменьшения риска повторных обострений.
Противопоказания
«Канефрон» не следует употреблять, если у вас повышенная чувствительность к компонентам. Также, если есть язва в стадии обострения. Его не следует применять в качестве монотерапии для лечения нарушений функций почек. Не следует применять для диуретической терапии отеков, вызванных сердечной или почечной недостаточностью.
Особенности применения
При применении «Канефрона» необходимо употреблять достаточное количество жидкости. Если имеются воспалительные процессы в почках следует обязательно проконсультироваться с врачом. При появлении крови в моче, расстройств мочеиспускания и острой задержки мочи необходимо немедленно обратиться к врачу. Препарат содержит глюкозу и сахарозу, поэтому пациентам с непереносимостью некоторых сахаров перед началом приема таблеток «Канефрон» следует проконсультироваться с врачом.
Взаимодействие с другими лекарственными средствами
Неизвестно.
Взаимодействие с алкоголем
Взаимодействие препарата в таблетках с алкоголем в инструкции не описывается. Но врачи не рекомендуют на время лечения заболеваний почек и мочевого пузыря употреблять любые спиртные напитки. Алкоголь повышает нагрузку на почки и раздражает слизистую мочевого пузыря, прием спиртного во время терапии может привести к ухудшению.
Применение при беременности и лактации
«Канефрон» при беременности нельзя использовать как диуретик через потенциальный риск для ребенка. Так как усвоение лекарств подробно еще не изучено, есть вероятность проникновения компонентов состава в грудное молоко, поэтому на время лактации от приема препарата следует отказаться.
Способность влиять на скорость реакции
Препарат не влияет на способность управлять автотранспортом или работать с механизмами.
Способ применения и дозы
Срок лечения назначается индивидуально. При хорошем усвоении компонентов, таблетки можно пить в длительный срок до 6 месяцев. Взрослым выписывают по 2 таблетки 3 раза в сутки. Детям старше 12 лет по 1 таблетке 3 раза в сутки. Прием пищи не влияет на усвоение препарата, поэтому принимать таблетки можно как до еды, так и после. Режим дозирования раствора — 150 капель в сутки. Делят на три раза, принимая утром, в обед и вечером. Взрослым можно пить капли в неразбавленном виде. Детям старше 12 лет лучше растворить 50 капель на 50 мл воды, чтобы уменьшить неприятные ощущения. Дозировка, приведенные в инструкции, рассчитанные для детей от 12 лет и взрослых. Детям младшего возраста препарат не назначается.
Передозировка
Лекарство нетоксично за счет естественного состава, передозировка маловероятна. Однако если же у пациента плохое самочувствие после приема большого препарата, следует промыть желудок и провести лечение. Случаи отравления препаратом вследствие передозировки неизвестны.
Побочные эффекты
-
диспепсические нарушения;
-
эпигастральные боли;
-
диарея;
-
крапивница;
-
эритема;
-
гиперемия эпидермиса.
При гипер чувствительности следует прекратить прием препарата и обратиться к врачу для подбора аналога с другими составом. Снять симптоматику аллергии поможет любой антигистаминный препарат.
Срок годности
Срок годности препарата – 4 года.
Не следует применять после окончания срока годности.
Условия хранения
Хранить в оригинальной упаковке, в сухом месте недоступном детям.
Категория отпуска
Выпускается без рецепта.
Цена
Цена колеблется от 219 до 262 за таблетки и от 192 до 230 гривен за капли.
Опубликовано в журнале:
Урология, 2005, №4:29-33
Введение. Лечение заболеваний почек и моче-выводяших путей с помощью лекарственных растений имеет многовековую историю. Несмотря на то что в XX веке, ознаменованном бурным развитием фармакоиндустрии и появлением многочисленных синтетических средств, фитопрепараты стали применяться значительно реже, но многих случаях их преимущества являются очевидными: во-первых, низкий риск развития осложнений и нежелательных побочных эффектов, во-вторых, широкий простор для маневрирования, который обеспечивается богатым выбором растений, оказывающих различные виды действия. Поэтому в последние годы «хорошо забытое старое” постепенно восстанавливает свои позиции |1, 2|.
Современные растительные препараты производятся с применением высоких технологий и проходят многоступенчатый контроль качества. Одним из фитопрепаратов нового поколения, широко применяемым в урологии, является Канефрон®Н («Bionorica”, Германия).
Канефрон®Н — комбинированный препарат, в состав которого входят золототысячник (Centaurium umbellatum), любисток (Levisiicum officinale) и розмарин (Rosmarinus officinale). Входящие в состав препарата вещества оказывают антисептическое, спазмолитическое, противовоспалительное действие на органы мочевой системы, уменьшают проницаемость капилляров почек, дают диуретический эффект, улучшают функцию почек, потенциируют эффект антибактериальной терапии (табл. 1) |1, 2|.
Таблица 1. Лекарственные растения входящие в состав Канефрона®Н, и спектр их действия.
| Активные вещества | Золототысячник (Centaurium umbellatum) |
Любисток (Levisticum officinale) |
Розмарин (Rosmarinus officinale) |
| Горечи, фенолкарбоновые кислоты |
Эфирные масла, фталеины | Розмариновая кислота, флавоноиды |
|
| Действие: | |||
| мочегонное | + | + | + |
| противовоспалительное | + | + | |
| спазмолитическое | + | + | + |
| антимикробное | + | + | + |
| сосудорасширяющее | + | + | + |
| нефропротективное | + | + | |
Различные виды действия Канефрона®Н обусловлены входящими в его состав эфирными масслами, фенол карболовым и кислотами, фталидами, горечами. Например, диуретическое действие препарата обусловлено сочетанием различных точек приложения его компонентов. Эфирные масла расширяют сосуды почек, что способствует улучшению кровоснабжения почечного эпителия, а также оказывают влияние на процессы обратного всасывания клетками почечных канальцев. Это проявляется главным образом в уменьшении реабсорбции ионов натрия и соответствующего количества воды. Диуретическое действие фенилкарбоновых кислот объясняется осмотическим эффектом: при попадании в просвет почечных канальцев они создают высокое осмотическое давление (обратному всасыванию эти вещества не подвергаются), при этом значительно снижается реабсорбция воды и ионов натрия. Таким образом, увеличение выведения воды происходит без нарушения ионного баланса (калийсберегаюший эффект).
Спазмолитический эффект обусловлен флавоноидной составляющей препарата. Аналогичное действие проявляют фталиды (любисток) и розмариновое масло. Слабыми спазмолитическими свойствами обладают фенолкарбоновые кислоты |1-4|.
Противовоспалительный эффект в основном обусловлен наличием розмариновой кислоты, которая блокирует неспецифическую активацию комплемента и липооксигеназы с последующим угнетением синтеза лейкотриенов. Как и другие фенольные соединения, розмариновая кислота проявляет анти-оксидантное действие и прерывает свободнорадикальные цепные реакции.
Все лекарственные растения, входящие в состав Канефрона®Н, содержат вещества, обладающие широким антимикробным спектром действия: фенолкарболовые кислоты влияют на бактериальный белок: эфирные масла разрушают цитоплазматическую мембрану бактерий и уменьшают активность аэробного дыхания, что приводит к уменьшению выделения энергии, необходимой дня синтеза различных органических соединений: флавоны, флавоноиды и флавонолы способны связываться с белками клеточной стенки и разрушать клеточные мембраны бактерий. Это обеспечивает активность препарата даже при устойчивой к синтетическим средствам микрофлоре.
Достоинством Канефрона®Н является также сочетание противомикробного и противовоспалительного эффектов, что особенно ценно при хронических процессах в мочевыводяших путях. Кроме того, выделение органических фенолкарбоновых кислот и их глюкуронидированных и сульфатированных метаболитов с мочой приводит к изменению ее кислотности, что противодействует росту бактерий. Помимо перечисленных свойств, элиминации бактерий из мочевых путей способствуют следующие факторы:
- биофлавоноиды тормозят бактериальную гиалуронидазу и таким образом ограничивают распространение бактерий в тканях;
- диуретический эффект препятствует адгезии микроорганизмов.
Установлено, что Канефрон®Н усиливает выведение солей мочевой кислоты. Эта сторона действия лишь отчасти связана с мочегонным эффектом и довольно специфична. Усиление выделения мочевой кислоты препятствует выпадению в мочевыводяших путях кристаллов, росту имеющихся камней и формированию новых. Также было отмечено, что данный препарат подщелачивает мочу, если она резко кислая, и поддерживает значение рН в пределах 6,2 — 6,8, что также препятствует образованию уратных камней.
Фармакологически доказанное действие Канефрона®Н на тубулярный аппарат почки четко показывает, что выделение белка с мочой из-за ранее перенесенных патологических процессов, повреждающих тубулярный аппарат, значительно снижается.
В нашей клинике мы применяли препарат Канефрон®Н для лечения двух групп больных — с хроническим циститом и мочекаменной болезнью.
Материалы и методы. Было обследовано 55 женщин, страдающих хроническим циститом и 79 пациентов с мочекаменной болезнью в возрасте от 18 до 45 лет. Длительность заболевания циститом на момент обращения составляла от 3 мес до 15 лет (у большинства больных от 1 года до 3 лет), а мочекаменной болезнью — от 3 до 5 лет с камнями почек и мочеточников.
При обследовании больных циститом применялись следующие методы:
- сбор анамнеза, физикальное обследование;
- микроскопическое исследование мочи и мочевого осадка;
- бактериологическое исследование мочи;
- анализ мазков из влагалища и цервикалыюго канала на наличие специфических возбудителей и общую чистоту;
- ультразвуковое исследование органов мочевой системы;
- экскреторная урография с нисходящей цистог-рафией;
- цистоскопия.
Сопутствующих заболеваний (камней, кист, опухолей, пороков развития) органов мочевой системы не было выявлено ни в одном случае.
С помощью ПЦР и ПИФ у 7 больных циститом были обнаружены специфические возбудители: у 2 больных — Chlamydia trachomatis, у 2 — Mycoplasma hominis, у 3 — Ureaplasma urealiticum. Эти больные были исключены из последующего анализа.
Дальнейшее обследование проводилось у 48 больных. При бактериологическом исследовании мочи у большинства больных (25 человек — 52%) выявлялась Escherichia coli. У 18 (37,5%) больных результаты посева мочи были отрицательными, у 5 (10,5%) больных были обнаружены другие возбудители — Proteus spp., Enterococcus spp., Staphylococcus spp.
Результаты цистоскопии представлены в табл. 2. Учитывая, что у многих больных выявлено сочетание различных изменений слизистой оболочки мочевого пузыря, итоговый показатель превышает 100%.
Таблица 2. Результаты цистоскопии у больных хроническим циститом (n = 48)
| Результаты цистоскопии | Количество больных | |
| абс. | % | |
| Гиперемия шейки мочевого пузыря | 38 | 79,1 |
| Инъекция сосудов слизистой оболочки и/или петехиальные кровоизлияния | 30 | 62,5 |
| Отечность слизистой оболочки шейки мочевого пузыря | 27 | 56,2 |
| Наличие фибринозных наложений | 10 | 20,9 |
| Поражение других отделов мочевого пузыря (помимо шейки) | 10 | 20,9 |
Таким образом, у большинства (79,1%) обследованных нами больных имелся шеечный цистит, другие отделы мочевого пузыря были вовлечены в патологический процесс значительно реже (в 20,9% случаев).
Во время цистоскопии патологических новообразований мочевого пузыря не было выявлено ни у одной больной. Оставшиеся 48 больных были подразделены на 2 группы с учетом наличия пиурии.
В группу А вошло 20 больных, у которых количество лейкоцитов в анализе мочи превышало 10 (от 10 до 20) в поле зрения, в группу Б — 28 больных, у которых пиурия отсутствовала.
Каждая группа была дополнительно подразделена на 2 равные подгруппы в зависимости от применения препарата Канефрона®Н. В подгруппы были включены больные, сравнимые по своим характеристикам (возрасту, анамнезу, клиническим проявлениям и т. д.).
Больные подгруппы А1 (n = 10) получали фосфомицин (монурал) по 3 г с интервалом 24 ч — всего 2 приема. Больные подгруппы А2 (n = 10) получали фосфомицин (монурал) по описанной выше схеме в сочетании с приемом Канефрона®Н по 2 драже 3 раза в сутки в течение 30 дней.
Больным подгруппы Б1 (n = 14) был проведен инициальный курс лечения, включавший противовоспалительные средства, препараты, улучшающие кровоток, местную терапию и физиотерапевтические процедуры, в течение 10 дней. Затем проводилось динамическое наблюдение 1 мес, в течение которого никакие дополнительные препараты не назначались. Больным подгруппы Б2 (n = 14) был проведен аналогичный инициальный курс лечения. Однако в течение последующих 30 дней они получали Канефрон®Н по 2 драже 3 раза в сутки.
Контрольное обследование больных группы А проводилось двукратно — через 10 и 30 дней после начала лечения. Критерии оценки: клинические проявления, наличие пиурии, наличие бактериурии.
Контрольное обследование больных группы Б проводилось через 30 дней после окончания курса комплексной инициальной терапии. Критерии оценки: клинические проявления. Учитывая, что все 18 больных с отрицательными результатами бактериологического исследования мочи вошли в группу Б, а у оставшихся 10 больных возбудитель высевался в низких титрах (103— 104 КОЕ/мл), наличие бактериурии не рассматривали в качестве критерия оценки эффективности лечения.
Результаты, полученные у больных с циститом. После проведенного лечения у большинства больных группы А наступило клиническое (табл. 3) и лабораторное улучшение различной степени выраженности.
Таблица 3. Динамика жалоб у больных группы А (n = 20) через 10 дней лечения
| Жалобы | До лечения (n = 10) | После лечения (n= 20) | ||||
| подгруппа А1 (монурал + канефрон, n = 10) | подгруппа А2 (монурал + канефрон, n = 10) | |||||
| абс | % | абс | % | абс | % | |
| Отсутствуют | 0 | 0 | 7 | 70 | 9 | 90 |
| Учащенное мочеиспускание | 19 | 95 | 3 | 30 | 1 | 10 |
| Резь при мочеиспускании | 20 | 100 | 2 | 20 | 1 | 10 |
| Зуд, жжение в промежности во время мочеиспускания и после него | 10 | 50 | 1 | 10 | 0 | 0 |
| Терминальная макрогематурия | 8 | 8 | 0 | 0 | 0 | 0 |
В подгруппе А1 пиурия через 10 дней лечения отсутствовала у 9 (90%) больных, в то время как в подгруппе А2 — у 100% больных.
При бактериологическом исследовании мочи, проведенном через 10 дней, исходно выделенный возбудитель был обнаружен только у 1 больного подгруппы А1; в подгруппе А2 результаты посева мочи были отрицательными в 100% случаев.
Сходные результаты были получены через 30 дней. У всех больных, принимавших Канефрон®Н, клинические проявления заболевания отсутствовали, в то время как у 3 (30%) больных, получавших монотерапию фосфомицином (монуралом), они были выражены в той или иной степени. Пиурия по-прежнему не выявлялась у 100% больных подгруппы А2. В подгруппе А1 повторное повышение количества лейкоцитов в моче было отмечено у 3 (30%) больных.
Таким образом, становится очевидным, что, несмотря на достаточно высокую лабораторную эффективность фосфомицина (монурала), достигающую 90%, добавление к терапии Канефрона®Н повышает клиническую эффективность лечения с 70 до 100% (при длительном приеме препарата). Вероятно, это связано с комплексным антимикробным, противовоспалительным, спазмолитическим и диуретическим эффектом последнего. Потенцируя действие фосфомицина (монурала), канефрон®Н обеспечивает дополнительный противовоспалительный и симптоматический эффект, который сохраняется и после прекращения активной антибактериальной терппии. Кроме того, оказалось, что длительный прием Канефрона®Н обеспечивает устойчивый противорецидивный эффект, о чем свидетельствует отсутствие клинических и лабораторных проявлений цистита через 30 дней лечения.
Через 30 дней наблюдения жалобы по-прежнему отсутствовали или были выражены незначительно у 10 (71%) из 14 больных, не получавших поддерживающей терапии Канефроном®Н. У 3 (21%) больных, несмотря на достигнутый ранее положительный эффект, было отмечено повторное развитие клинической картины цистита (табл. 4). Что касается больных подгруппы Б2, получавших поддерживающую терапию Канефроном®Н, то через 30 дней жалобы отсутствовали у 13 (92,8%) из 14 больных (см. табл. 4).
Таблица 4. Динамика жалоб у бальных группы Б (n = 28) через 30 дней после окончания курса инициальной терапии
| Жалобы | До лечения (n = 28) | После инициальной терапии и 10 дней наблюдения (n = 28) |
||||
| подгруппа Б1 (без поддерживающей терапии n = 14) | подгруппа Б2 (поддерживающая терапия n = 14) | |||||
| абс | % | абс | % | абс | % | |
| Отсутствуют | 0 | 0 | 10 | 71 | 13 | 92,8 |
| Учащенное мочеиспускание | 27 | 96,4 | 3 | 21,4 | 1 | 7,1 |
| Резь при мочеиспускании | 28 | 100 | 4 | 29 | 1 | 7,1 |
| Зуд, жжение в промежности во время мочеиспускания и после него | 10 | 35,7 | 2 | 14,3 | 1 | 7,1 |
| Терминальная макрогематурия | 5 | 17,8 | 0 | 0 | 0 | 0 |
Таким образом, прием Канефрона®Н не только способствовал поддержанию достигнутого ранее эффекта, но и дополнительно повышал эффективность инициальной терапии на 7%. В общем через 30 дней наблюдения эффективность лечения с применением Канефрона®Н была выше эффективности терапии без приема данного препарата на 21,8%.
По-видимому, в отсутствие выявляемого возбудителя (или при выявлении его в низких титрах) и пиурии эффективность применения Канефрона®Н обусловлена его противовоспалительным, спазмолитическим и диуретическим эффектом, что делает целесообразным применение данного препарата с целью профилактики рецидивов хронического цистита после достигнутого клинического улучшения, а также для повышения эффективности курса инициальной комплексной терапии.
Следует отметить, что в процессе применения Канефрона®Н в группах А и Б не было зарегистрировано ни одного случая развития побочных эффектов или непереносимости препарата.
Применение Канефрона®Н у больных мочекаменной болезнью, перенесших ударноволновую литотрипсию
Группу канефрона составили 45 пациентов (27 мужчин и 18 женщин) в возрасте от 29 до 55 лет.
Контрольную группу составили 34 пациента (19 мужчин и 15 женщин) В возрасте от 34 до 62 лет. Длительность заболевания у большинства больных составляла от 2 до 4 лет. При обследовании у всех пациентов были выявлены камни почек или мочеточников (табл. 5, 6).
Таблица 5. Локализация камней у больных группы канефрона (n = 34)
| Локализация камней | Число больных | Средний размер камней. мм |
| Группа А1 — камни почек | 12 | 8,1 |
| Группа B1 — камни верхней трети мочеточника | 8 | 2,8 |
| Группа С1 — камни средней трети мочеточника | 5 | 3,1 |
| Группа D1 — камни нижней трети мочеточника | 9 | 3,6 |
Таблица 6. Локализация камней у больных группы канефрона (n = 45)
| Локализация камней | Число больных | Средний размер камней. мм |
| Группа А1 — камни почек | 22 | 7,4 |
| Группа B1 — камни верхней трети мочеточника | 7 | 3,2 |
| Группа С1 — камни средней трети мочеточника | 6 | 2,6 |
| Группа D1 — камни нижней трети мочеточника | 10 | 2,1 |
При обследовании пациентов как основной, так и контрольной групп обращалось внимание на лейкоцитурию, значение рН мочи, суточный диурез.
В основной группе лейкоцитурия была выявлена у 29 (64,4%) больных, в контрольной группе — у 15 (44,1%) больных. Значение рН мочи в основной и контрольной группах в среднем составляло 5,7, суточный диурез — 1300 мл.
Всем пациентам была выполнена дистанционная ударно-волновая литотрипсия. Пациентам основной группы в состав медикаментозной терапии назначался Канефрон®Н по 2 драже 3 раза и день. Пациентам контрольной группы проводилась спазмолитическая и противовоспалительная терапия без назначения Канефрона®Н.
Критериями оценки эффективности препарата Канефрона®Н служили сроки отхождения дезинтегрированных конкрементов после дистанционной ударно-волновой литотрипсии, снижение лейкоцитурии, увеличение суточного диуреза, нормализация рН мочи.
Результаты и обсуждение. Отхождение дезинтегрированных конкрементов в течение первых 5 сут после дистанционной ударно-волновой литотрипсии в группе А (n = 22) произошло у 16 (72.7%) больных, тогда как в группе A1 (n = 12) — у 4 (33.3%) пациентов. 2 пациентам группы А и 3 пациентам группы A1 потребовался повторный сеанс дистанционной ударно-волновой литотрипсии.
Отхождение дезинтегрированных конкрементов в течение первых 5 сут после дистанционной ударно-волновой литотрипсии в группе В (n = 7) произошло у 5 (71,4%) больных, тогда как в группе B1 (n = 8) — у 3 (37,5%) пациентов. 1 пациенту группы B1 потребовался повторный сеанс дистанционной ударно-волновой литотрипсии.
Отхождение дезинтегрированных конкрементов в течение первых 5 сут после дистанционной ударно-волновой литотрипсии в группе С (n = 6) произошло у 4 (66,6%) больных, тогда как в группе C1 (n = 5) — у 2 (40%) пациентов.
Отхождение дезинтегрированных конкрементов в течение первых 5 суток после дистанционной ударно-волновой литотрипсии в группе D (n = 10) произошло у 9 (90%) больных, тогда как в группе D1 (n = 9) — у 5 (55,5%) пациентов.
Таким образом, очевидно, что применение Канефрона®Н в составе комплексной терапии после дистанционной ударно-волновой литотрипсии ускоряет отхождение осколков конкрементов из мочевых путей независимо от уровня их исходной локализации. По-видимому, это обусловлено комплексным спазмолитическим и диуретическим эффектом препарата, а также его антимикробным и противовоспалительным действием, вследствие которого уменьшались воспалительные изменения слизистой оболочки мочевых путей. Данную гипотезу подтверждает тот факт, что исчезновение лейкоцитурии на 7-е сутки в основной группе отмечено у 27 (93,1%) пациентов, тогда как в контрольной группе — всего у 7 (46,6%) пациентов.
В группе Канефрона®Н повышения количества лейкоцитов в контрольных анализах мочи не наблюдалось, рН мочи поддерживался в диапазоне 6,2– 6,8, суточный диурез увеличился до 2–2,5 л.
Ни у одного пациента признаков непереносимости, побочных эффектов и осложнений при приеме препарата Канефрона®Н не отмечено.
Заключение. Анализ проведенного исследования позволяет нам рассматривать препарат Канефрон®Н как эффективное и безопасное лекарственное средство для лечения больных циститом и мочекаменной болезнью, перенесших дистанционную ударно-волновую литотрипсию.
Опубликовано в журнале:
«Вестник педиатрической фармакологии и нутрициологии», 2008, том 5, №4, с. 66-69
В.В. Длин, О.В. Шатохина, И.М. Османов, Э.А. Юрьева
Московский НИИ педиатрии и детской хирургии Росмедтехнологий
Canephron® N effectiveness in children with dysmetabolic nephropathy with oxalate-calcium cristalluria
В статье приведены современные представления о спорадических дизметаболических нефропатиях: методах диагностики, лечения и профилактики. Указаны современные препараты растительного происхождения для лечения детей с дизметаболической нефропатией с оксалатно-кальциевой кристаллурией. Представлены собственные данные по эффективности Канефрона Н для лечения детей с дизметаболической нефропатией. Ключевые слова: дети, спорадическая дизметаболическая нефропатия, оксалатно-кальциевая кристаллурия, Канефрон Н
Vestn Pediatr Farmacol Nutnts 2008; 4: 66-69
Проблема спорадических дизметаболических нефропатий является весьма актуальной в педиатрии и детской нефрологии. Это обусловлено высокой частотой патологии в популяции, а так же возможностью ее прогрессирования вплоть до развития мочекаменной болезни и/или интерстициального нефрита. Ее эффективное решение возможно при объединении достижений нормальной и патологической физиологии, клинической медицины, патологической анатомии, биохимии, фармакологии, иммунологии и нефрологии. Использование такого комплекса знаний современной медицины определяется необходимостью изучения сложных процессов, обусловливающих роль почек в поддержании вместе с энтероцитами кишечника и другими системами постоянства внутренней среды организма, а также их значения в регуляции кровообращения и кроветворения, углеводного и липидного обменов. При этом обеспечивается как ауторегуляция режима работы самих почек, так и организма в целом.
Под дизметаболическими нефропатиями понимают большую группу нефропатий с различной этиологией и патогенезом, объединенных тем, что их развитие связано с нарушениями обмена веществ. Патология обмена веществ приводит к изменениям функционального состояния почек или к структурным сдвигам на уровне различных элементов нефрона.
Дизметаболические нефропатий в широком смысле слова объединяют заболевания, связанные с тяжелыми нарушениями водно-солевого обмена, которые развиваются при желудочно-кишечных заболеваниях с токсическим синдромом и нарушениями гемодинамики. К ним могут быть отнесены поражения почек, протекающие на фоне нарушений фосфорно-кальциевого обмена при гиперпаратиреозе, гипервитаминозе D и других заболеваниях.
Термин дизметаболическая нефропатия может быть употреблен и в более узком смысле слова для обозначения полигеннонаследуемой (мультифакториально развивающейся) нефропатий, которая связана с патологией обмена щавелевой кислоты и проявляется в условиях семейной нестабильности цитомембран .
Клинически — это дизметаболическая нефропатия с оксалатно-кальциевой кристаллурией, которая охватывает различные варианты заболевания: вторичную тубулопатию с минимальными клинико-морфологическими проявлениями патологии, интерстициальный нефрит, развивающийся вследствие нарушения метаболизма оксалатов, и мочекаменная болезнь. По своей патогенетической сущности дизметаболическая нефропатия с оксалатно-кальциевой кристаллурией является вариантом почечной мембранопатии. В последние годы установлено, что так называемая вторичная оксалатная нефропатия в отличие от первичной гипероксалурии, обусловленной нарушением метаболизма глиоксиловой кислоты, включает гетерогенную группу полигеннонаследуемых заболеваний почек, связанных с патологией обмена щавелевой кислоты и развивающихся в условиях нестабильности клеточных мембран .
При этом в генезе мембранодестабилизирующих процессов в тканях важная роль принадлежит процессам интенсификации перекисного окисления липидов, активации эндогенных фосфолипаз, и окислительного метаболизма гранулоцитов .
При лечении дизметаболической нефропатии с оксалатно-кальциевой кристаллурией показано применение средств, стабилизирующих клеточные мембраны: антиоксидидантов, димефосфона, ксидифона, солей калия и магния, повторных курсов витаминов В6, А, Е.
У детей с дизметаболической нефропатией с оксалатно-кальциевой кристаллурией широко используются фитопрепараты и лекарственные растения, обладающие литолитическим действием, улучшающие обменные процессы, способствующие выведению продуктов обмена не только через мочевыделительную систему, но и через желудочно-кишечный тракт, а также антиоксиданты, особенно содержащие флавоноиды.
Из комбинированных фитопрепаратов рекомендуется использовать Канефрон Н, цистон или фитолизин.
В клинической практике очень удобно использовать Канефрон Н, который существует в 2-х лекарственных формах — капли для приема внутрь и драже и, поэтому его можно использовать для лечения спорадической дизметаболической нефропатии даже у детей раннего возраста. Канефрон Н — лекарственное средство, содержащее экстракты золототысячника, любистка, розмарина и 19 об.% спирта. Канефрон Н оказывает комплексное действие: диуретическое, противовоспалительное, спазмолитическое, антиоксидантное и нефропротективное, уменьшает проницаемость капилляров, потенцирует эффекты антибиотиков. Терапевтические свойства Канефрона Н обусловлены входящими в его состав эфирными маслами (любисток, розмарин), фенолкарбоновыми кислотами (розмарин, любисток, золототысячник), фталидами (любисток), горечами (золототысячник). Как известно, основные признаки воспаления связывают с так называемыми медиаторами воспаления (брадикинин, простагландины, гистамин, серотонин и др.). Противовоспалительные свойства Канефрона Н обусловлены в основном антагонизмом розмариновой кислоты в отношении медиаторов воспаления. Механизм действия связан с блокированием неспецифической активации комплемента и липооксигеназы с последующим угнетением синтеза лейкотриенов. Широкий спектр антимикробного действия препарата обусловлен фенолкарбоновыми кислотами, эфирными маслами и т.д. Противомикробный эффект фенолкарбоновых кислот опосредован воздействием на бактериальный белок. Липофильные флавоноиды и эфирные масла способны разрушать клеточные мембраны бактерий. Диуретическое действие препарата определяется в основном сочетанным действием эфирных масел и фенолкарбоновых кислот. Эфирные масла расширяют сосуды почек, что увеличивает их кровоснабжение. Фенолкарбоновые кислоты при попадании в просвет почечных канальцев создают высокое осмотическое давление, что также снижает реабсорбцию воды и ионов натрия. Таким образом, увеличение выведения воды происходит без нарушения ионного баланса (калий-сберегающий эффект). Спазмолитический эффект обусловлен флавоноидной составляющей препарата. Аналогичное действие проявляют фталиды (любисток), розмариновое масло. Слабыми спазмолитическими свойствами обладают фенолкарбоновые кислоты. Обнаружена высокая эффективность флавоноидной составляющей в уменьшении протеинурии (влияние на проницаемость мембраны). Благодаря антиоксидантным свойствам флавоноиды способствуют защите почек от повреждения свободными радикалами. По клиническим данным, Канефрон Н увеличивает выделение мочевой кислоты и способствует поддержанию рН мочи в диапазоне 6,2-6,8, что является важным в лечении и профилактике уратного и кальций-оксалатного уролитиаза. Флавоноиды и розмариновая кислота могут связывать кальций и магний в хелатные комплексы, а наличие мочегонной составляющей позволяет быстро выводить их из организма. Также ряд авторов рекомендуют применять Канефрон Н для улучшения отхождения фрагментов конкрементов после литотрипсии . Применяют препарат по 2 драже или по 50 капель 3 раза в сутки. Для детей доза препарата уменьшается в 2-3 раза в зависимости от возраста: по 10-25 капель или по 1 драже 3 раза в день в течение 6-8 недель. Препарат особенно показан при наличии вторичного пиелонефрита метаболического генеза, эффективен при оксалатной и/или уратной кристаллурии, изменяет рН мочи. Может использоваться как в активной стадии в комбинации с антибактериальными средствами, так и в виде монотерапии в качестве поддерживающей противорепидивной терапии. Сукало А.В. и соавт. (2004) .
Целью работы явилось определение клинической эффективности препарата Канефрон Н у детей со спорадической дизметаболической нефропатией с оксалатно-кальциевой кристаллурией.
Пациенты и методы исследования
Общий дизайн исследования: открытое, сравнительное исследование эффективности и безопасности лечения дизметаболической нефропатии у детей препаратом Канефрон Н.Основная группа (группа 1) — 25 детей (10 девочек и 15 мальчиков) в возрасте от 3 лет до 17 лет (средний возраст 10 лет 4 мес.) — получали Канефрон Н в течение 3 месяцев в возрастных дозах:
- Дети школьного возраста — по 1 драже или 25 капель 3 раза в сутки;
- Дети дошкольного возраста — по 15 капель 3 раза в сутки.
Все дети обследовались до начала лечения, через 1 месяц и 3 месяца после начала лечения. Объем обследования: анализы мочи (общий и Нечипоренко), биохимия мочи с определением суточной экскреции оксалатов, кальция и липидов в моче. Уровень экскреции кальция пересчитывался на креатинин (кальций/креатининовый индекс).
Результаты и обсуждение
До начала терапии микрогематурия (более 2 эритроцитов в поле зрения) отмечалась несколько чаще у детей 1-ой группы (0,88) по сравнению со 2-й (0,8), а средний уровень оксалатов в основной (1 группа) и контрольной (2 группа) группах достоверно не отличался (198,9±31,4 и 187,2±17,5 мкмоль/24ч, соответственно). Частота гипероксалурии в обеих группах была примерно равна: 0,8 и 0,84, соответственно. До начала терапии частота кальциурии составляла 0,36 в 1 и 2 группах, а средний уровень достоверно не отличался (2,6±0,45 и 3,11±0,47 ммоль/24 ч, соответственно). Однако у детей 1-ой группы по сравнению с группой сравнения несколько чаще выявлялся повышенный кальций/креатининовый индекс (норма — менее 0,5) — 0,64 и 0,48, соответственно. Частота липидурии у детей обеих групп достоверно не отличалась (0,83 и 0,82, соответственно) (таблица).
Клиническая характеристика детей с дизметаболической нефропатией до начала терапии
| Группы обследованных детей | Эритроциты в моче | Оксалурия | Кальциурия | Кальций/ креатини- новый индекс |
Липидурия |
| 1 группа | 0,88 | 0,8 | 0,36 | 0,64 | 0,83 |
| 2 группа | 0,8 | 0,84 | 0,36 | 0,48 | 0,82 |
Примечание. Достоверных различий клинической характеристики детей 1 и 2 групп не выявлено.
В динамике лечения отмечено более значимое снижение частоты гематурии, гиперксалурии и гиперкальциурииу детей основной группы, по сравнению с группой сравнения (рис. 1-4). Через 3 месяца терапии гиперкальциурия сохранялась у 1 ребенка основной группы и у 4-х детей (17%) — группы сравнения.
Рис. 1. Динамика гематурии у детей с дизметаболической нефропатией при лечении Канефроном Н
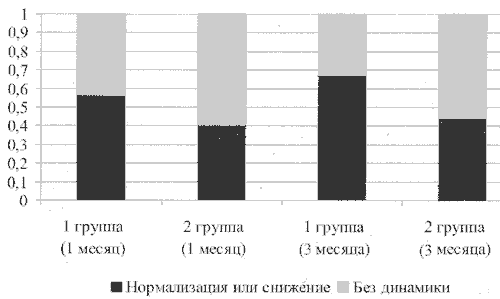
Рис. 2. Частота гиперксалурии у детей с дизметаболической нефропатией в динамике лечения Канефроном Н
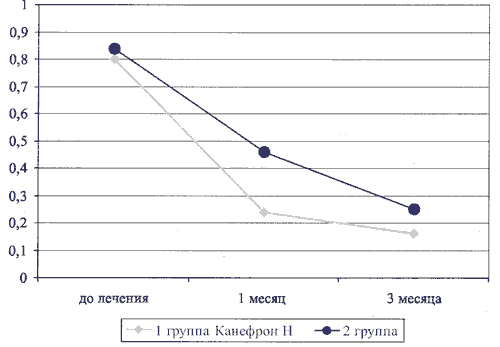
Рис. 3. Динамика гипероксалурии у детей с дизметаболической нефропатией при лечении Канефроном Н
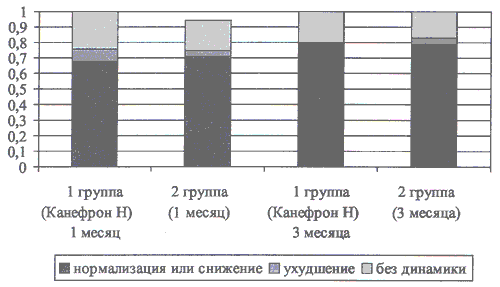
Рис. 4. Частота гиперкальциурии у детей с дизметаболической нефропатией в динамике лечения Канефроном Н
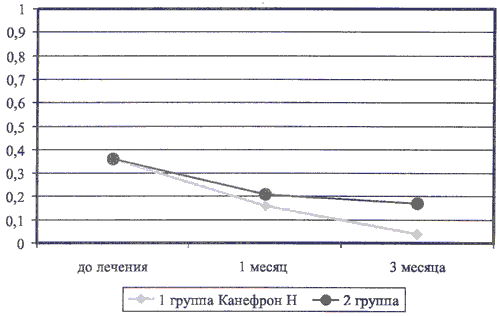
При анализе динамики изменения уровня кальция в моче достоверных различий в обеих группах не получено (рис. 5). Это связано с тем, что при анализе учитывалась не только нормализация уровня кальция в моче (этот показатель в 4 раза лучше в основной группе, см. рис. 4), но и улучшение — снижение уровня кальция более чем на 15% от начального уровня.
Рис. 5. Динамика кальциурии у детей с дизметаболической нефропатией при лечении Канефроном Н
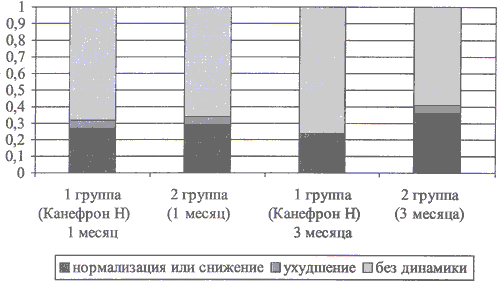
У четверти детей 1-ой группы нормализация кальций/креатининового индекса отмечалась уже через 1 месяц лечения Канефроном Н, а через 3 месяца еще у четверти детей наблюдалась нормализация кальций/креатининового индекса. Иная ситуация выявлена во 2-ой группе. Здесь через 1 месяц лечения ни у одного ребенка не отмечено нормализации кальций/креатининового индекса, а через 3 месяца только у 2-х детей (0,1) отмечена нормализация кальций/креатининового индекса.
Уже через 1 месяц лечения Канефроном Н у большинства детей нормализовался уровень липидурии (рис. 6). Сходные, но несколько менее выраженные данные отмечены и в группе сравнения. Через 3 месяца от начала терапии только у 3-х детей основной группы сохранилась повышенная экскреция липидов с мочой, а в группе сравнения частота детей с высокой экскрецией липидов была вдвое выше (0,14 и 0,28, соответственно).
Рис. 6. Частота липидурии у детей с дизметаболической нефропатией в динамике лечения Канефроном Н
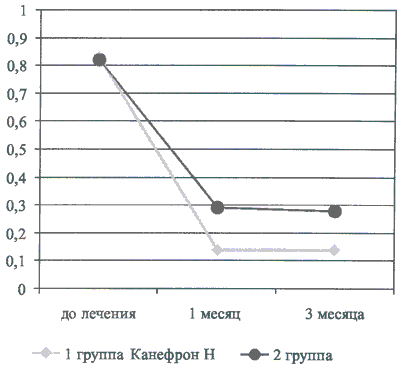
При анализе динамики липидурии на фоне терапии установлено, что через 1 месяц лечения несколько лучше динамика отмечена в группе сравнения, тогда как через 3 месяца терапии лучше динамика наблюдалась в основной группе (рис. 7).
Рис. 7. Динамика липидурии у детей с дизметаболической нефропатией при лечении Канефроном Н
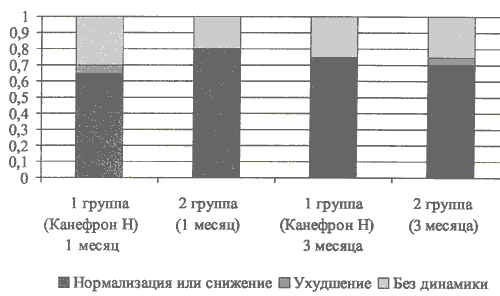
Заключение
Таким образом, установлено, что лечение детей с дизметаболической нефропатией Канефроном Н по сравнению с терапией комплексом витаминов (А, Е, В6) более эффективно и приводит к более быстрому и значимому снижению частоты и выраженности гематурии, гипероксалурии, кальцийурии и липидурии. Полученные результаты показывают, что наибольшая эффективность терапии дизметаболической нефропатии достигается только к 3-м месяцам лечения препаратом Канефрон Н, что указывает на необходимость применения этого препарата не менее 3-х месяцев непрерывно.




