Гбн новорожденного
- Ключевые слова
- Список сокращений
- Термины и определения
- 1. Краткая информация
- 2. Диагностика
- 3. Лечение
- 4. Реабилитация
- 5. Профилактика и диспансерное наблюдение
- 6. Дополнительная информация, влияющая на течение и исход заболевания
- Критерии оценки качества медицинской помощи
- Список литературы
- Приложение А1. Состав рабочей группы
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение А3. Связанные документы
- Приложение Б. Алгоритмы ведения пациента
- Приложение Г.
Содержание
- Ключевые слова
- Список сокращений
- Термины и определения
- 1.2 Этиология и патогенез
- 1.3 Эпидемиология
- 1.4 Коды по МКБ 10
- 1.5 Классификация
- 2.1 Жалобы и анамнез
- 2.2 Физикальное обследование
- 2.3 Лабораторная диагностика
- 2.4 Инструментальная диагностика
- 2.5 Иная диагностика
- 3.1 Консервативное лечение
- 3.2 Хирургическое лечение
- Реабилитация
- Профилактика и диспансерное наблюдение
- Дополнительная информация, влияющая на течение и исход заболевания
- Критерии оценки качества медицинской помощи
- Список литературы
- Приложение А1. Состав рабочей группы
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение А3. Связанные документы
- Приложение Б. Алгоритмы ведения пациента
- Список литературы диссертационного исследования кандидат медицинских наук Чистозвонова, Елена Александровна, 2004 год
Ключевые слова
-
гемолитическая болезнь
-
новорожденный
-
фототерапия
-
операция заменное переливание крови
-
ядерная желтуха
-
водянка плода
-
резус – изоиммунизация плода и новорожденного
-
АВО — изоиммунизация плода и новорожденного
Список сокращений
АГ ? антиген
АД ? артериальное давление
АЛТ ? аланинаминотрансфераза
АСТ ? аспартатаминотрансфераза
АТ ? антитело
БЭ ? билирубиновая энцефалопатия
ГБН ? гемолитическая болезнь новорожденных
ГГТ ? гамма-глютамилтранспептидаза
ДВС ? диссеминированное внутрисосудистое свертывание крови
КОС ? кислотно-щелочное состояние
МКБ ? международная классификация болезней -10
ОБ ? общий билирубин
ОЗПК ? операция заменного переливания крови
ОРИТН ? отделение реанимации и интенсивной терапии новорожденных
ОЦК ? объем циркулирующей крови
ПИТН — палата реанимации и интенсивной терапии новорожденных
СЗП- свежезамороженная плазма
ФТ ? фототерапия
ЧД ? частота дыхания
ЧСС ? частота сердечных сокращений
ЩФ ? щелочная фосфатаза
Hb ? гемоглобин
IgG ? иммуноглобулин G
IgM ? иммуноглобулин M
Термины и определения
Гемолитическая болезнь плода и новорожденного (ГБН) – изоиммунная гемолитическая анемия, возникающая в случаях несовместимости крови матери и плода по эритроцитарным антигенам, при этом антигены локализуются на эритроцитах плода, а антитела к ним вырабатываются в организме матери.
1.2 Этиология и патогенез
Возникновение иммунологического конфликта возможно, если на эритроцитах плода присутствуют антигены, отсутствующие на мембранах клеток у матери. Так, иммунологической предпосылкой для развития ГБН является наличие резус-положительного плода у резус-отрицательной беременной. При иммунологическом конфликте вследствие групповой несовместимости у матери в большинстве случаев определяется O (I) группа крови, а у плода A (II) или (реже) B (III). Более редко ГБН развивается из-за несовпадения плода и беременной по другим групповым (Дафф, Келл, Кидд, Льюис, MNSs и т.д.) системам крови.
К попаданию эритроцитов плода в кровоток матери и возникновению иммунологического конфликта в случаях антигенной несовместимости по факторам крови предрасполагает предшествовавшая изосенсибилизация, вследствие абортов, выкидышей, внематочной беременности, родов, при которых иммунная система матери вырабатывает антитела к эритроцитарным антигенам. Если АТ относятся к иммуноглобулинам класса G (к подклассам IgG1, IgG3, IgG4) ? они беспрепятственно проникают через плаценту. С увеличением их концентрации в крови повышается вероятность развития гемолитической болезни плода и новорожденного. Антитела подкласса IgG2 обладают ограниченной способностью трансплацентарного транспорта, антитела класса IgM, к которым относятся в том числе ?- и ?-агглютинины, не проникают через плаценту.
Реализация ГБН по резус-фактору, как правило, происходит обычно при повторных беременностях, а развитие ГБН в результате конфликта по групповым факторам крови возможно уже при первой беременности. При наличии иммунологических предпосылок для реализации обоих вариантов ГБН чаще развивается по системе АВО. При этом возникновение гемолиза вследствие попадания в кровь ребенка II группы материнских анти-А- антител встречается чаще, чем при попадании в кровь ребенка III группы анти-В-антител. Однако в последнем случае проникновение анти-В-антител приводит к более тяжелому гемолизу, нередко требующему заменного переливания крови . Тяжесть состояния ребенка и риск развития ядерной желтухи при ГБН по АВО-системе менее выражены по сравнению с ГБН по резус-фактору. Это объясняется тем, что групповые антигены А и В экспрессируются многими клетками организма, а не только эритроцитами, что приводит к связыванию значительного количества антител в некроветворных тканях и препятствует их гемолитическому воздействию .
1.3 Эпидемиология
ГБН в России диагностируется приблизительно у 0,6% всех новорожденных.
1.4 Коды по МКБ 10
Гемолитическая болезнь плода и новорожденного (P55):
P55.0 — Резус – изоиммунизация плода и новорожденного
P55.1 — АВО — изоиммунизация плода и новорожденного
P55.8 — Другие формы гемолитической болезни плода и новорожденного
P55.9 — Гемолитическая болезнь плода и новорожденного неуточненная
1.5 Классификация
1.5.1 По конфликту между матерью и плодом по системе АВО и другим эритроцитарным факторам крови:
- несовместимость по системе АВО;
- несовместимость эритроцитов матери и плода по резус- фактору;
- несовместимость по редким факторам крови.
1.5.2 По клиническим проявлениям выделяют формы заболевания:
отечная (гемолитическая анемия с водянкой);
желтушная (гемолитическая анемия с желтухой);
анемическая (гемолитическая анемия без желтухи и водянки).
1.5.3 По степени тяжести желтухи в желтушной форме:
легкая;
средняя тяжесть;
тяжелую степень.
1.5.4 По наличию осложнений:
билирубиновая энцефалопатия: острое поражение центральной нервной системы;
ядерная желтуха: необратимое хроническое поражение центральной нервной системы;
синдром сгущения желчи;
геморрагический синдром.
2.1 Жалобы и анамнез
- При сборе анамнеза рекомендуется обратить внимание на:
резус- принадлежность и группа крови матери;
инфекции во время беременности и родов;
наследственные заболевания (дефицит Г6ФДГ, гипотиреоз, другие редкие заболевания);
наличие желтухи у родителей;
наличие желтухи у предыдущего ребенка;
вес и гестационный возраст ребенка при рождении;
вскармливание ребенка (недостаточное вскармливание и/или рвота).
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
2.2 Физикальное обследование
Отечная форма ГБН
Общий отечный синдром (анасарка, асцит, гидроперикард), выраженная бледность кожи и слизистых, гепатомегалия и спленомегалия, желтуха отсутствует или слабо выражена. Возможен геморрагический синдром, развитие ДВС синдрома.
Желтушная форма ГБН
При рождении могут быть желтушно прокрашены околоплодные воды, оболочки пуповины, первородная смазка. Характерно раннее развитие желтухи, бледность кожных покровов и видимых слизистых оболочек, увеличение печени и селезенки.
Анемическая форма ГБН
На фоне бледности кожных покровов отмечают вялость, плохое сосание, тахикардию, увеличение размеров печени и селезенки, возможны приглушенность тонов сердца, систолический шум.
Осложнения ГБН
Ядерная желтуха – билирубиновая интоксикация- вялость, снижение аппетита, срыгивания, патологическое зевание, мышечная гипотония, исчезновение 2 фазы рефлекса Моро, далее возникает клиника энцефалопатии – опистотонус, «мозговой» крик, выбухание большого родничка, судороги, патологическая глазодвигательная симптоматика – симптом «заходящего солнца», нистагм. Синдром сгущения желчи – желтуха приобретает зеленоватый оттенок, печень увеличена, насыщенный цвет мочи.
2.3 Лабораторная диагностика
- Рекомендуется по Rh-фактору установление уже в первые часы жизни ребенка на основании анамнеза (прирост титра анти-D антител у Rh(–)
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1в).
-
Всем женщинам с отрицательным резус-фактором во время беременности рекомендуется определение уровня иммунных АТ в крови в динамике .
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Коментарии: ГБН по АВ0-системе, как правило, не имеет специфических признаков в первые часы после рождения.
-
Если кровь матери характеризуется отрицательным резус-фактором или принадлежностью к О (I) группе, новорожденному рекомендуется обязательно проводить исследование концентрации общего билирубина в пуповинной крови и определение группы и резус-фактора крови
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
-
При подозрении на ГБН рекомендуется провести следующие лабораторные тесты :
- Групповая и резус принадлежность крови матери и ребенка.
- Общий анализ крови.
- Биохимический анализ крови (общий билирубин и фракции, альбумин, уровень глюкозы; другие параметры (фракции билирубина, кислотно-щелочное состояние (КОС), электролиты и др.) — по показаниям);
- Серологические тесты: Реакция Кумбса.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3 ).
Комментарии: Прямая проба Кумбса становится положительной при наличии фиксированных антител на поверхности эритроцитов, что, как правило, наблюдается при ГБН по резус-фактору. Из-за небольшого количества фиксированных на эритроцитах антител, при ГБН по АВО чаще наблюдается слабо положительная прямая проба Кумбса в первые сутки жизни, которая уже может стать негативной через 2-3 дня после рождения.
Непрямая проба Кумбса предназначена для выявления неполных антител, присутствующих в исследуемой сыворотке. Это более чувствительный тест для выявления материнских изоантител, чем прямая проба Кумбса. Непрямая проба Кумбса может применяться в индивидуальных случаях, когда причина гемолиза неясна.
Следует помнить, что выраженность реакции Кумбса не коррелирует с тяжестью желтухи! (Уровень доказательности D)
2.4 Инструментальная диагностика
- Рекомендуется провдение УЗИ брюшной полости;
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
- Рекомендуется нейросонография.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
2.5 Иная диагностика
- Рекомендуется провести лабораторное ииследование крови:
-
кровь на ИФА (на наличие инфекции);
-
кровь на ПЦР (на наличие инфекции);
-
коагулограмма;
-
бактериологическое исследование крови.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 4).2%
3.1 Консервативное лечение
-
Рекомендуется фототерапия (ФТ), как наиболее эффективный метод консервативной терапии ГБН.
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: Особенности проведения ФТ при ГБН:
-
Возможно применение как стандартных ламп, так и фиброоптической и светодиодной ФТ, целесообразно комбинировать несколько методов ФТ;
-
Источник света располагается на расстоянии 50 см над ребенком. Для усиления эффекта фототерапии лампа может быть приближена на расстояние 10-20 см от ребенка при постоянном наблюдении медицинского персонала и контроле температуры тела ;
-
Проведение фототерапии при ГБН (особенно у детей с риском ОЗПК) должно выполняться в непрерывном режиме;
-
Поверхность тела ребенка на фоне ФТ должна быть максимально открыта. Подгузник может быть оставлен на месте;
-
Глаза и половые органы должны быть защищены светонепроницаемым материалом;
-
Суточный объем жидкости, который ребенок получает энтерально или парентерально, необходимо увеличить на 10-20% по сравнению с физиологической потребностью ребенка;
-
Спустя 12 часов после окончания фототерапии необходимо выполнить контрольное исследование билирубина;
-
Фототерапия проводится до, во время (при помощи фиброоптической системы) и после операции заменного переливания крови.
-
Рекомендуется внутривенное введение иммуноглобулина человека нормального . Высокие дозы стандартных иммуноглобулинов блокируют Fc-рецепторы клеток ретикуло-эндотелиальной системы и тем самым позволяют снизить гемолиз и, следовательно, уровень билирубина, что в свою очередь уменьшает число ОЗПК .
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b.).
Комментарии: Препараты иммуноглобулина человеческого новорожденным с ГБН вводятся по следующей схеме:
-
в первые часы жизни новорожденного внутривенно медленно (по возможности, в течение 2 часов), но с обязательным соблюдением требований инструкции к лекарственному препарату;
-
доза ? 0,5-1,0 г/кг (в среднем 0,8 г/кг)*
*В случае назначения дозы иммуноглобулина, превышающей указанную в инструкции к препарату, необходимо как можно подробнее обосновать данное действие в истории болезни и оформить коллегиальное разрешение на проведение ребенку терапии «Off-label». Применение терапии «вне инструкции» («off-label») также требует обязательного оформления добровольного информированного согласия законного представителя пациента, в котором подробно разъясняются особенность применения такой терапии, возможные риски и побочные явления, а также разъясняется право отказаться от проведения терапии «off-label»;
-
повторное введение иммуноглобулина при необходимости осуществляется через 12 часов от предыдущего;
-
введение иммуноглобулина при ГБН возможно в течение первых 3 суток жизни.
-
Не рекомендуется допаивание детей на грудном вскармливании .
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b).
Комментарии: Исключение составляют случаи, когда грудного молока недостаточно, чтобы увеличить суточный объем на 10-20%. Если состояние ребенка не позволяет увеличить объем жидкости энтерально, только тогда проводится инфузионная терапия.
-
Желчегонная терапия рекомендована в случае развития синдрома холестаза на фоне ГБН. Проводится только препаратом урсодезоксихолевой кислоты в виде суспензии из расчета 20-30 мг/кг/сут .
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3).
-
Введение альбумина человека . Доказательств того, что инфузия альбумин человека увеличивает долгосрочные исходы у детей с тяжелой гипербилирубинемией нет, поэтому его рутинное применение не рекомендуется .
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3).
-
Фенобарбитал** – эффект при ГБН не доказан, применение не допустимо .
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3).
-
Другие медикаментозные средства ( препараты группы гепатопротекторов ) – применение при ГБН не доказано и не допустимо.
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 3).
3.2 Хирургическое лечение
-
Рекомендована операция заменного переливания крови.
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: Показания для ОЗПК:
-
в случае неэффективности фототерапии рекомендуется заменное переливание крови;
-
в случае появления клинических симптомов острой билирубиновой энцефалопатии (мышечный гипертонус, опистотонус, лихорадка, «мозговой» крик) заменое переливание крови проводится независимо от уровня билирубина;
-
при ГБН, вызванной изолированным резус-конфликтом используется Rh- отрицательная одногруппная с кровью ребенка ЭМ и СЗП по возможности АВ (IV) группы крови в соотношении ЭМ к СЗП — 2:1;
-
при ГБН, вызванной изолированным групповым конфликтом, используется ЭМ первой (I) группы, совпадающая с резус-принадлежностью эритроцитов ребенка и одногруппная или АВ (IV) группы СЗП в соотношении 2:1;
-
при несовместимости крови матери и крови ребенка по редким факторам необходимо использовать кровь от индивидуально подобранных доноров.
При ГБН используют только свежеприготовленную ЭМ (срок хранения не более 72 часов);
ОЗПК проводится в асептических условиях в отделении интенсивной терапии или операционной;
Во время операции должен быть обеспечен мониторный контроль за частотой сердцебиений, дыхания, артериальным давлением, насыщением гемоглобина кислородом, температурой тела. Перед началом операции пациенту вводится назогастральный зонд;
Переливание производят через пупочную вену с помощью поливинилового катетера (№ 6, 8, 10). Глубина введения катетера зависит от массы тела пациента (не более 7 см.).
Расчет объема для ОЗПК
V общий = m?ОЦК?2, где V- объем, m- масса тела в кг,
ОЦК – для недоношенных – 100-110 мл/кг, для доношенных – 80-90 мл/кг.
Пример: ребенок массой тела 3 кг.
(V эр.массы) = Vабс : 0,7 (примерный Ht эритроцитов) = 255: 0,7 = 364 мл
-
Фактический объем СЗП = V общ. — V эр. Массы = 510 – 364 = 146 мл
Вначале через катетер выпускают 10 мл крови, которую используют для определения концентрации билирубина. Затем вводят такой же объем донорской крови со скоростью 3-4 мл/мин.
Введение и выведение крови чередуются объемом 20 мл у доношенных и 10 мл у недоношенных детей.
Объем одной эксфузии-инфузии не должен превышать 5-10% ОЦК. Общая продолжительность операции составляет около 2-х часов.
После операции провести ОАМ и через два часа по окончании трансфузии рекомендуется определить концентрацию глюкозы в крови.
Об эффективности проведенной ОЗПК свидетельствует более, чем двукратное снижение концентрации билирубина в конце операции.
Реабилитация
- Рекомендуется проведение реабилитационных мероприятий:
неонатальный уход;
исключительно грудное вскармливание;
медицинский отвод от профилактических прививок на 1 месяц.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Профилактика и диспансерное наблюдение
-
Рекомендована профилактика Rh-иммунизации после родов Rh-отрицательным родильницам, не имеющим анти-резусных антител, родивших резус-положительного ребенка. Выполняется в первые 72 часа после родов путем введения 300 мкг анти-Д(Rh)-иммуноглобулина .
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
- Рекомендовано:
- наблюдение врача-педиатра участкового, врача общей практики;
- каждый месяц контроль ОАК;
- в 6 месяцев детям после ОЗПК – кровь на ВИЧ;
- вопрос о профилактических прививках решают после 6 месяцев жизни.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Дополнительная информация, влияющая на течение и исход заболевания
Дополнительные факторы, повышающие риск развития билирубиновой энцефалопатии:
- Факторы, повышающие проницаемость ГЭБ для билирубина: гиперосмолярность крови, ацидоз, кровоизлияния в мозг, нейроинфекции, артериальная гипотензия.
- Факторы, повышающие чувствительность нейронов головного мозга к токсическому действию неконъюгированного билирубина: недоношенность, тяжелая асфиксия, голодание, гипогликемия, анемия.
- Факторы, снижающие способность альбумина крови прочно связывать неконъюгированный билирубин: недоношенность, гипоальбуминемия, инфекция, ацидоз, гипоксия, повышение уровня неэстерифицированных жирных кислот в крови, использование сульфаниламидов, фуросемида, фенитоина , диазепама, индометацина, салицилатов, полусинтетических пеницилинов, цефалоспоринов.
Критерии оценки качества медицинской помощи
|
№ |
Критерии качества |
Уровень достоверности доказательств |
Уровень убедительности рекомендаций |
|
Выполнено исследование уровня общего билирубина и уровня общего гемоглобина в пуповинной крови у новорожденного при рождении (при отрицательном резус факторе и/или группы крови 0(I) у матери) |
В |
||
|
Выполнено определение основных групп крови (A, B, 0) и определение резус-принадлежности у новорожденного в пуповинной крови при рождении |
А |
||
|
Выполнен прямой антиглобулиновый тест (прямая проба Кумбса) и/или непрямой антиглобулиновый тест (тест Кумбса) |
В |
||
|
Выполнено повторное исследование уровня общего билирубина и определен почасовой прирост общего билирубина не позднее 6 часов и 12 часов от момента рождения |
В |
||
|
Выполнен общий (клинический) анализ крови с определением количества ретикулоцитов7% |
В |
||
|
Выполнена фототерапия кожи и/или операция заменного переливания крови после оценки уровня общего билирубина в зависимости от массы тела при рождении (при наличии показаний) |
1 | А | |
|
Выполнена операция частичного заменного перелевания крови не позднее 3 часов от момента рождения (при отечной форме гемолитической болезни) |
А |
Список литературы
Приложение А1. Состав рабочей группы
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций – специалисты, имеющие высшее медицинское образование по специальностям:
-
Врач -Неонатология;
-
Врач-Анестезиология-реаниматология;
-
Врач-Педиатрия.
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрановскую библиотеку, базы данных MEDLINE и EMBASE. Глубина поиска составляла 25 лет.
Методы, использованные для оценки качества и силы доказательств:
-
консенсус экспертов;
-
оценка значимости в соответствии с рейтинговой схемой для оценки степени обоснованности («силы») рекомендаций (табл. П1, П2).
Таблица П1 – Уровни достоверности доказательств в соответствии с международными критериями
|
Уровень достоверности |
Тип данных |
|
Мета-анализ рандомизированных контролируемых исследований |
|
|
По крайней мере, 1 рандомизированное контролируемое исследование |
|
|
По меньшей мере, 1 контролируемое исследование без рандомизации |
|
|
По крайней мере, 1 квази-экспериментальное исследование |
|
|
Описательные исследования, такие как сравнительные исследования, корреляционные исследования или «случай-контроль» исследования |
|
|
Отчет экспертного комитета или мнение и/или клинический опыт призванного авторитета |
-
Таблица П2 – Уровни убедительности рекомендаций
|
Уровень убедительности |
Основание рекомендации |
|
Уровень доказательства 1 |
|
|
Уровень доказательства 2 или экстраполированные рекомендации уровня доказательства 1 |
|
|
Уровень доказательства 3 или экстраполированные рекомендации уровней доказательства 1 или 2 |
|
|
Уровень доказательства 4 или экстраполированные рекомендации уровней доказательства 2 или 3 |
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Методы валидизации рекомендаций:
-
Внешняя экспертная оценка;
-
Внутренняя экспертная оценка.
Порядок обновления клинических рекомендаций – пересмотр 1 раз в 3 года.
Приложение А3. Связанные документы
-
Международная классификация болезней, травм и состояний, влияющих на здоровье, 10-го пересмотра (МКБ-10) (Всемирная организация здравоохранения) 1994.
-
Номенклатура медицинских услуг (Министерство здравоохранения и социального развития Российской Федерации) 2011.
-
Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 № 323 Ф3.
-
Перечень жизненно необходимых и важнейших лекарственных препаратов на 2016 г. (Распоряжение Правительства РФ от 26.12.2015 № 2724-р.)
-
Порядок оказания медицинской помощи по профилю «неонатология» (Приказ Минздрава России от 15 ноября 2012 г. N 921н).
Приложение Б. Алгоритмы ведения пациента
Тактика ведения детей с ГБН в возрасте более 24 часов жизни:
зависит от абсолютных значений билирубина (табл. 1) или динамики этих показателей.
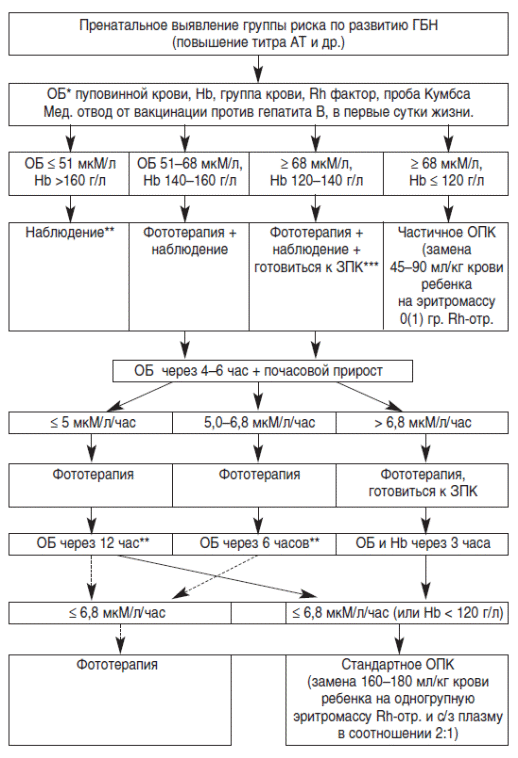
-
при появлении желтухи в течение первых 24 часов жизни – неотложное исследование ОБ, дальнейшая тактика ведения зависит от величины почасового прироста билирубина;
-
заказать необходимые препараты крови (плазма + эрмасса), стабилизировать жизненно важные функции организма.
Список литературы диссертационного исследования кандидат медицинских наук Чистозвонова, Елена Александровна, 2004 год
2. Азбукина Л.Н. Современные принципы лечения гемолитической болезни плода и новорожденного.
4. Бобев Др.,Иванова Ив. Гемолитическая болезнь новорожденного.// Болезни новорожденных. София, 1963. — С. 169-182.
6. Васильева З.Ф. Антигенно-несовместимая беременность и методы защиты плода и новорожденного при иммунологическом конфликте. Автореф. Дисс.докт. Л. — 1972.
8. Горюшина Н.Б. Биофизический профиль плода у беременных с резус-изосенсибилизацией: Автореф.дисс. канд.мед.наук. -М. 1996.
9. Гуревич П.С. Об особенностях изменений сосудов при ГБН// Архив патол. 1966. — № 8. — С.60-65.
11. П.Калманова В.П. Показатели эритропоэтической активности и обмена железа при гемолитической болезни плода и внутриутробных трансфузиях эритроцитов: Дисс. канд.мед.наук . -М., 2000. 142 с.
13. Кошель И.В. Гемолитическая болезнь новорожденных (ГБН)// Кроветворение плода и новорожденного. М.: Медицина, 1993. С. 127138.
14. Кристесашвили Д.И. Генетические аспекты перинатальной патологии. — Тбилиси.- 1995.-50 с.
15. Михайлов А.В. Клиническое руководство по ультразвуковой диагностике. М.: Медицина, 1996. 265 с.
17. Персианинов Л.С., Сидельникова В.М., Елизарова И.П. Гемолитическая болезнь плода и новорожденного. Л. Медицина- 1981.- 208 с.
18. Полякова Г.П. Профилактика и лечение гемолитической болезни новорожденных. //Акуш. и гинекол.- 1959. № 1. — С. 6-10.
19. Поттер Э. Патологическая анатомия плодов и новорожденных и детей раннего возраста: Пер. с англ. -М.: Медицина, 1971. 359 с.
20. Румянцев А.Г., Аграненко В.А. Гемотрансфузионная терапия в педиатрии и неонатологии. //Макс-пресс. 2002. — С. 411-486.
22. Савельева Г.М., Сичинава Л.Г. Акушерство и гинекология. М. — 1997. -С. 161-162.
27. Таболин В.А., Никончик О. Этиология, патогенез и комплексная терапия гемолитической болезни новорожденных (Методические указания) // Изд. Минздрава СССР. 1965.
28. Таболин В.А. Роль факторов несовместимости крови матери и плода // Вестн.АМН СССР. 1966. — № 6. — С.84-91.
29. Таболин В.А. Справочник неонатолога. Д.: Медицина, 1984. 280 с.
30. Таболин В.А. и др. Динамика реанимационной помощи недоношенных детей.// 1У Конгресс педиатров России, М. — 2000. — С. 278.
31. Тимошенко Л.В. Гемолитические заболевания новорожденных. — Киев, 1956.- 120 с.
32. Тимошенко Л.В., Бондарь М.В., Дашкевич В.Е. Гемолитическая болезнь плода и новорожденного. М. 1968.
33. Тур А.Ф. Клиника, профилактика и лечение гемолитической болезни новорожденных // Сов.Мед. 1957. — № 11.- С.25-30.
34. Тур А.Ф. Гемолитическая болезнь новорожденных. //Медгиз. 1958.
36. Шабалов Н.П. Патология гемостаза новорожденных. //Вопросы охраны материнства и детства. 1983. — № 1. — С. 3-9.
39. Ahlfors CE.Bilirubin-albumin binding and free bilirubin.// J Perinatol. 2001. — Vol.21. — Suppl. 1.- P.S40-S42. — Discussion S59-S62.
42. Avent N.D. Hemolytic anemia// Brit.J.Biomed.Sci. 1997. — Vol.54. — N 1. -P. 16-37.
46. Bournazeau J.A. et.al. Complications of cordocentesis associated with therapy// J.Gynecol.Obstet. 1999. — Vol.28. — N1.-P.24-30.
47. Bowman J.M. Suppression of Rh isoimmunization //Obstet. Gunecol. 1978. -Vol.52.-P. 385-389.
51. Bowman J.M., Herman F.A., Manning C.R. Erythroblastosis fetalis produced by anti-k// Vox Sang. 1989. — Vol.56. — P. 187-191.
54. Bowman J.M. The management of hemolytic disease in the fetus and newborn.//Semin. Perinatol. 1997. — Vol. 21. — P. 39-45.
63. Dugoff L, Hobbins JC. Invasive procedures to evaluate the fetus. //Clin Obstet Gynecol. 2002. — Vol.45. — N 4. — P. 1039-1053.
69. Fisk N.M., Bower S. Fetal blood sampling in retreat.// Brit.Med.J. 1993. -Vol.307. — P.143-144.
72. Gartner L.M. Neonatal jaundice.//Pediatrie. 1994. — Vol.15. — P.422-432.
73. Gest A.L., Moise K.J. Hydrops fetalis//Neonatology for the Clinician. East Norwalk: Appleton and Lange, 1993. — Vol.8. — P.395-410.
75. Giacoia GP. Severe fetomaternal hemorrhage: a review.//Obstet .Gynecol. Surv. 1997.- Vol.52.-N 6.-P.372-38.0
82. Hansen TW.Mechanisms of bilirubin toxicity: clinical implications.//Clin Perinatol. 2002.- Vol.29.-N 4.-P.765-778.
83. Harrington K., Fayyad A. Prediction of fetal anaemia. //Curr Opin Obstet Gynecol. 2002.- Vol.14.-N 2.-P.177-185.
84. Hershko C., Gale R.P., Ho W. ABH antigens and bone marrow transplantation// Drit.J.Haematol. 1980. — Vol.44. — P.65-70.
91. Koenig J.M. Evaluation and treatment of Erythroblastosis Fetalis in the Neonate.???
99. Liley A.W. Intrauterine transfusion of foetus in haemolytic disease.// Brit.Med.J. 1963. — Vol.2. — P. 1107-1109.
105. Maede R.et.al.Haemolytic disease of the newborn due to anti-Ce //Transfus.Med. -2000. Vol.10. -N 4. -P.305-306.
106. Maiseis M.J. Neonatal Jaundice// Clin.Perinatol. 1990. — Vol.17.- P.245249.
108. Mari G, Deter RL, Carpenter RL, Rahman F, Zimmerman R, Moise KJ Jr,
110. Maroni E.S., Angst F. Der Stand der Rhesusprophylaxein der Schweiz in
111. Jahre 1985 //Arch.Gynecol. 1986. — Bd.239. -N 3-4.- P.235-250.
113. Moise K.J. Non-anti-D antibodies in red-cell alloimmunization // Eur.J.Obstet.Gynecol.Reprod.Biol. 2000. — Vol.92. — N 1. — P.75-81.
114. Moise KJ Jr. Management of rhesus alloimmunization in pregnancy. Obstet Gynecol. 2002.- Vol.100.-N 3. — P.600-611.
117. Nevanlinna H.R. Factors affecting maternal Rh immunization // Ann.Med.Exp.Biol. 1953. — Vol.31. — P. 1-10.
118. Nikolaides K.H., Rodeck C.H. ,Millar S.S. Fetal haematology in rhesus isoimmunization// Brit.Med.J. 1985. — Vol.290. — P. 661-663.
123. Parilla B.V., Socol M.L. Hydrops fetalis with Kell isoimmunization // Obstet.Gynecol. 1996. — Vol.88. — P.730-735.
124. Peddle L.J. Increase of antibody titer following amniocentesis // Amer.J.Obstet.Gynecol. 1986.-Vol. 100.-P. 567-571.
125. Peterec S,.M. Management of neonatal Rh disease. //Clin Perinatol. -1995. -Vol.22.-P.561-592.
131. Queenan J.T. Amniotic fluid analysis.//Clin Obstet Gynecol. 1971. — Vol.14. -N 2. — P.505-536.
133. Queenan JT. Fetal transfusion //Fetal Ther. 1986. — Vol. 1. — P.59-64.
134. Race R.R. The Rh genotype and Fisher’s theory //Blood. 1948. — Vol.3. -P.27-35.
139. Rex K.B. Relationship between blood groups and ratio of the newborn // Acta Bio.Hung. 1991. — Vol.42. -N4. -P.357-364.
140. Ryan G., Morrow R.J. Fetal blood transfusion // Clin. Perinatol. 1994. -Vol.21. -P.573-589.
147. Smoleniec J, James D. Predictive value of pleural effusions in fetal hydrops. Fetal Diagn Ther. 1995.- Vol.10.-N 2.-P.95-100.
149. Sosa ME. Nonimmune hydrops fetalis. //J Perinat Neonatal Nurs. -1999. -Vol.13.-N3.-P.33-44.
152. Thompson J.Haemolytic disease of the newborn: the new NICE guidelines.//.! Fam Health Care. 2002.- Vol.12.-N 5.- P.133-136.
155. Tolpe J.J. Bilirubin and brain injury // Neurology of the newborn. -Philadelphia: WB Saunders, 1987.-P.386-408.
160. SM. Mirror syndrome. A case report.// J. Reprod. Med. 2002 . — Vol. 47. -N 9. — P.770-774.
163. Wegmann A., Gluck R. The history of rhesus prophylaxis with anti-D // Eur.J.Pediatr. 1996. — Vol.155. -P.835-840.
167. Prediction of fetal anemia //Am.J. Obstet.Gynecol. 1991. — Vol. 165. -P.546-553.
169. Woodrow J.XC. Rh immunization and its prevention: the immune response in the mothers. Copenhagen: Munksgaard, 1970. — P.3-10.
Гемолитическая болезнь плода и новорожденного развивается вследствие несовместимости организмов матери и плода по различным эритроцитарным антигенам.
В большинстве случаев гемолитическая болезнь плода и новорожденного вызывается сенсибилизацией матери антигенами системы резус и АВО. Значительно реже она возникает при несовместимости по другим антигенам эритроцитов. Наиболее часто и наиболее тяжело протекает гемолитическая болезнь при резус-несовместимости.
Существует 3 основные разновидности резус-фактора, качественно различающиеся: АГ Д, С, Е. При наличии хотя бы одного из этих антигенов на эритроцитах, человек является резус-положительным.
Кровь резус-отрицательных людей также не лишена антигенных свойств. Имеется 3 разновидности антигена Hr: АГ d, c, e. Фактор d не обладает способностью вызывать образование антител. АГ c обладает выраженными антигенными свойствами. АГ е обладает слабыми антигенными свойствами.
В крови человека естественные антитела по отношению к резус-фактору отсутствуют. Иммунные анти-резус антитела появляются в ответ на попадание резус-антигена либо после переливания резус-несовместимой крови либо после родоразрешения резус-положительным плодом.
Наличие в крови резус-отрицательных лиц антирезус-антител является показателем сенсибилизации организма к резус-фактору. Выработка антител наблюдается через 4 – 5 месяцев и позднее с момента попадания антигена в кровоток. Сенсибилизация организма усиливается по мере продолжающегося действия антигена.
Наиболее распространенными способами выявления анти-резус антител является прямая и непрямая проба Кумбса с применением антиглобулиновой сыворотки. Выявлению антител, особенно при слабой реакции, способствует применение эритроцитов, предварительно обработанных ферментами (трипсином, химотрипсином, папаином и др.). Об активности антител судят по их титру.
Иммунизация женщин с резус-отрицательной кровью чаще всего наступает в результате беременности и родов плодом с резус-положительной кровью. Наиболее вероятное время получения первичного стимула – послеродовый период. Различные оперативные вмешательства в родах, особенно ручное отделение последа, кесарево сечение, намного увеличивают трансплацентарный переход эритроцитов плода в кровь матери. В связи с выраженной антигенностью резус-фактора у большого числа резус-отрицательных женщин в результате трансплацентарого перехода эритроцитов плода развивается иммунизация.
К сенсибилизации организма к резус-фактору могут принести не только роды. Причиной ее нередко является самопроизвольное либо искусственное прерывание беременности. На развитие сенсибилизации кроме трансплаентарного перехода эритроцитов, влияют группа эритроцитов и генотип по резус-фактору у плода. Кроме того, имеют значение пол плода, иммунологическая толерантность организма матери, снижение иммунологической реактивности организма во время беременности, генетические факторы. Какими бы ни были пути развития сенсибилизации, иммунное состояние, возникнув, остается на всю жизнь. У женщины, сенсибилизированной к резус-фактору, уже при первой ее беременности может развиться гемолитическая болезнь.
Иммунизация оказывает неблагоприятное влияние на развивающийся плод, но и на течение беременности. Одним из частых осложнений при изоиммунизации материнского организма является угроза прерывания беременности, анемия, отмечается значительное нарушение функционального состояния печени, зависящее от степени сенсибилизации.
Гемолитическая болезнь развивается в результате проникновения материнских антител к плоду через плаценту. Резус-антитела вступают в реакцию с резус-положительными эритроцитами плода, что ведет к их гемолизу. Развивающаяся анемия вызывает компенсаторную реакцию организма, возникновение экстрамедуллярных очагов кроветворения с последующей гепатоспленомегалией. Продукты распада эритроцитов стимулируют костный мозг к образованию молодых незрелых форм красной крови. В результате преобладания процессов разрушения у плода развивается анемия.
Появление и усиление желтухи при гемолтической болезни связано с увелечением содержания в крови непрямого билирубина. При ограниченной возможности печени в отношении перевода непрямого билирубина в прямой ,переработка продуктов обмена веществ оказывается для нее большой натрузкой в связи с чем наблюдается быстрое накопление непрямого билирубина. Последний обладает токсическими свойствами и не выводится почками. Токсичность сегопроявляется в нарушении тканевого метаболизма за счет выключения дыхательных ферментов и процессов фосфорилирования. В результате происходит перегрузка печени железом, билирубиновыми пиг ментами и нарушается ее функция, особенно синтез белков, что ведет к гипопротеинемии и к усилению проницаемости сосудов. Возникает сердечная недостаточность и увеличенная печень приводят к выведению жидкости в ткани и развивается анасарка.
Выделяют 3 основные формы гемолитической болезни:
1. Гемоли тическая анемия — наиболее легкая форма заболевания . Основным ее симптомом является бледность кожных покровов в сочетании с низким количеством гемоглобина и эритроцитов . Отмечается небольшое увеличенне селезенки и петехиальные высыпания.
2. Гемолитическая анемия с желтухой. Важнейшими симптомами ее являичся анемия,в тяжелых случаях наблюдаются симптомымы поражения ЦНС . При рождении ребенка обрашает на себя внимание желтая окраска околоплодных вод, первородной смазки, кожных покровов. Анемия чаше бывает нормохромной и обычно не достигает выраженной степени. Эритробластоз служит показателем тяжести заболевания. Появление и усиление желтухи обусловлены повышением в крови непрямого билирубина.
3. Гемолитическая анемия с желтухой и водянкой (отечная форма) наиболее тяжелая форма. Дети с отечной формой обычно рождаются мертвыми или погибают вскоре после рождения. Резко выраженными симптомами заболевания являются общий отек, значительно выраженные симптомы — желтуха, гепатоспленомегалия, гемодинамические нарушения. Часто при этой форме заболевания отмечается геморрагический синдром.
Степени тяжести гемолиги ческой болезни :
-легкая — гемоглобин в крови более 150г/л, билирубин в крови пуповины менее 5.5 мкмоль /л.
-средняя — гемоглобин от 100- 150 г/ л. билирубин 5.0 мкмоль/л. Отмечается бледность кожи и слизистых покровов. . -тяжелая — гемоглобин менее 100 г/л, отмечается анасарка. . Диагностика. 1)иммунолог ический анализ у женщин с резус-отрицательной кровью — обнаружение в крови беременной антител позволяют сделать вывод о вероятности развития заболевания плода и о необходимости применения лечебно-профилактических мероприятий
2)определение генотипа крови. Позволяет определить вероятность возникновения гемолитической болезни;
3)анализ сердечной деятельности плода показатели, характерные для гипоксии.
4)УЗИ — увеличение толщины плаценты, шаровидные зоны,двойной контур головки, асцит.
5)амниоцентез с последующим исследованием на наличие сенсебилизации при беременности, мертворождении,повышение общег о белка в околоплодных водах.
Однократное исследование околоплодных вод, особенно в поздние сроки беременности не всегда позволяет поставить правильный диагноз,поэтому исследование целесообразно начинать со 2 недели беременности и переодически повторять. Лечение гемолитической болезни плода и новорожденных: . -динамическое наблюдение поликлинике за состоянием здоровья беременной и плода: систематическое профилактическое обследование женщины,
-госпитализация на 12 ,24 и 32 неделях беременности для проведения более длительного и тщательного обследования беременной и плода.
а) внутривенное введение 2.0 мл раствора глюкозы с аскорбиновой кислотой ежедневно:
б) 2 мл сиТсТина:
в) 100 мл кокарбоксилазы:
I ) р\ 1 ни;
.1)1 .покоил I на.к.кии.
с) оксшснчкрапия:
ж) ;)п Iпансмнческое лечение:
ч) дначолнн:
ксантинола никотинат (теоннкол) для ул\чтения микропиркуля?1ин:
трансплантация беременным лоскуIа кожи, в’.яюн у мужа (для дссснсибили :апии.) при наличии симпюмов пораженной и’.оссненбнлнзацнн. обношенном акушерском анамнезе, осложненном течении беременности:
при особо тяжелых проявлениях сенсибилизации предннчолон по 0.005 I ежедневно с 28 педели беременности. Препарат блаютворно влияет на обмен веществ, снижает проницаемость сосудов, подавляет сите*’, ашиге.т и аллерт ические реакции:
некоюрые авюры рекомендуют вызывать преждевременные ролы с целью предупреждения длительно! о воздействия резуе-сштнтел матери на плод. 11ос»1а1алы1ЫЙ период: 1) каменное переливание крови:
раннее (в I 2-е сутки жижи) с целью повышения \ровня |емо!лобина и проведения ленппоксикаиионной терапии. Показания наличие или появление желтухи в первые часы жизни, содержание непрямо! о билирубнна в пмтовинной крови более 68.4 мкмольлл почасовой прирост билпрубнна в первые часы жизни более (>.8 мкмоль л’ ч. уровень 1емо1лобина менее 150 I л. I емаюкри I менее 40°о:
позднее (в конце 2-х суток и позже) с иедыо борьбы с билирубиновой интоксикацией. Показания непрямой билирубнн 300.7 мкмоль л (у зрелою ребенка) и 273. 6 мкмоль л (у незрелою).
Появление первых признаков билирубиновой интоксикации (нарастающая вялосп». снижение сосательною и коленною рефлексов. Пристли ;авнсимо от уровня бнлнрубнна является показанием к чамснному переливанию крови. Донорсклто кровь ребенку вводят череч пупочную
I ) фототерапия направлена на разрушение непрямот о билирубина до ею водорасмворнмых дериватов в повер.чнос1ных с.юя\ кожи тата новорожденного под действием дневного света: _
2) инфучнопная гсраиия с целью дечннюксикапин. повьпттення свя’-ыпающей способности альбуминов крови, коррекции метаболических нарушении : I емодеч:
5 10°о раствор тлн^ко’.ы: 10 20°.»раствор альбумина: плачма:
3) ашиоксндантная крайня:
20 Ы)»о распи>р юкоф^рола апета та: рибофлавин: кальция нантамат: •4) повышение бнлирубиневячывающей функции печени фенобарбитал нлдуцнруе» активность и \величпвает синтез
микросомальных ((крмепюв печени, ответственнт.тх ча утилизацию непрямою билир^бина. 17.Методы лечения недостаточности фетоплацентарното кровообращения. Лечение фетоплацентарной недостаточности должно быть направлено на улучшение маточноплацентарного и фетоплацентарного кровообращения. Новыми направлениями в лечении недостаточности плаценты являются: устранение или уменьшение недостаточности, Улучшение метаболической функцин плаценты.
Воздействуя на организм плода, минуя плаценту и используя трансптлацентарный путь обмена.
Применяемые методы и отдельные средства воздействуют одновременно на несколько функций плаценты. Однако основным звеном в улучшении функции плаценты является улучшение маточно-плацентарной перфузии, что достигается применением комплекса различных средств и методов либо препаратов, расслабляющих матку в сочетании с мероприятиями, направленными на нормализацию реологических свойств крови (управляемая гемоделюция).
Методы и средства, применяемые при лечении недостаточности фетоплацентарного кровообращения:
-тепловые процедуры на околопочечную область , приводящие к расслаблению миометрия и к расширению сосудов,
Абдоминальная декомпрессия — снижает излишнюю работу мускулатуры матки по преодолению тонуса мышц брюшною пресса, что приводит к усилению кровотока в матке и к улучшению плацентарной перфузии, а также достигается усиление и повышение функции плаценты.
ЪО — применяется для улучшения функции плаценты и состояния плода, особенно у беременных с пороками сердца. Она обеспечивает активность дыхательных ферментов, способствует нормализации углеводного обмена. . Сосудорасширяющие препараты (эуфиллин. теофиллин. ксантинола никотинат).
Трентал — вазоактивный препарат, обладающий сосудорасширяющим действием, снижающий периферическое сопротивление сосудов, улучшающий реологические свойства крови и микроциркуляцию.
Преператы токолитического действия (бета-адреномиметики) — их малые дозы снижают сопротивленне сосудов на уровне маточно-плацентарного кровообращения.
. коррекция реологических расстройств — инфузия низкомолекулярных декстранов (реополиглюкин) под его влиянием кровоток значительно увеличивается в плаценте.
гепарин — способен расширять кровеносные сосуды, особенно при гипертензнонном синдроме , улучшает микроциркулянию, предотвращает избыточное отложение фибрина.
Средства, улутшающие газообмен и метаболизм в плаценте:
ОКСИГЕНОтерапия,
Витаминотерапия,
Препараты железа,
нестероидные анаболические средства.
Карбоксилаза осушествляет защиту углеводного обмена в системе мать-дитя, расширяет сосуды маточно-плапентарното комплекса; рибоксин оказывают хороший эффект на метаболическую функцию плаценты, участвуют в синтезе белковых молекул.
Длительность терапии плацентарной недостаточности должна составлять не менее 6 недель (в стационаре, с продолжением терапии в условиях женской консультации). В случае выявления этой патологии и проведения соответствующей терапии во 2 триместре для закрепления эффекта от первого курса следует проводить повторное лечение в сроки 32 — 34 недели беременности.