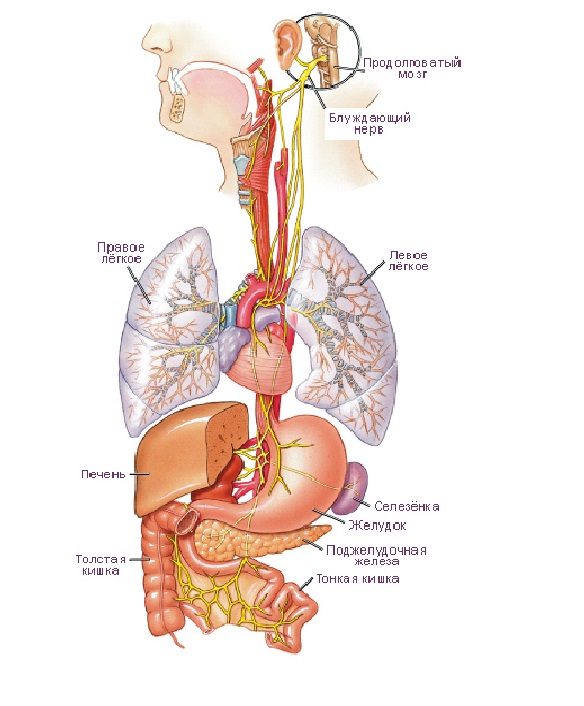
Ботулотоксин при инсульте
В нашей стране ежегодно регистрируется около 400 тыс. инсультов, при этом примерно у одной трети больных, выживших после инсульта, развивается спастичность . По данным ВОЗ, распространенность постинсультной спастичности в мире составляет 200 человек на 100 тыс. жителей, спастичностью страдает более 12 млн больных .
Спастический мышечный гипертонус характеризуется возникновением увеличивающегося сопротивления при первых быстрых пассивных движениях и затем внезапном уменьшении его — феномен «складного ножа» по Шеррингтону. В настоящее время под спастичностью понимают двигательное нарушение, являющееся частью синдрома поражения верхнего мотонейрона, характеризующееся скорость-зависимым повышением мышечного тонуса и сопровождающееся повышением сухожильных рефлексов в результате гипервозбудимости рецепторов растяжения .
Однажды развившись, спастический парез, как правило, сохраняется в течение всей жизни больного. При этом если спастичность сохраняется в течение длительного времени, развиваются вторичные изменения в мышцах, сухожилиях и суставах (фиброз, атрофия, контрактура). Лечение спастического пареза — пока практически неразрешимая задача. В связи с этим столь актуальной является разработка подходов к лечебному воздействию на мышечную спастичность, основанных на изучении механизмов ее развития .
Для коррекции мышечного гипертонуса нередко используют различные методы физиотерапии, лечебной физкультуры, рефлексотерапии, а также фармакологическое лечение в виде назначения миорелаксантов .
В последние годы при лечении постинсультной спастичности стали применяться препараты ботулинического нейротоксина типа А. Данный метод лечения предложен для освоения практикующим врачам сравнительно недавно, несмотря на то, что первое научное сообщение о применении блокад ботулотоксина появилось в печати более 20 лет назад .
В сравнении с имеющимися методами лечения мышечного гипертонуса, локальное введение ботулотоксина имеет ряд несомненных преимуществ . Во-первых, лечение хорошо переносится и не связано с риском серьезных осложнений. Во-вторых, возможен выбор одной или нескольких мышц для инъекции и подбор дозы препарата, обеспечивающей желаемую степень расслабления.
Как известно, ботулизм — тяжелое инфекционное заболевание, проявляющееся периферическими параличами мышц и вегетативными расстройствами вследствие нарушения периферической холинергической медиации, вызываемого ботулиническим нейротоксином. В настоящее время известны 8 серологических подтипов ботулотоксина: А, В, С1, С2, D, E, F, G. Ботулизм у человека могут вызвать серотипы А, В, Е, F, G, но самым сильнодействующим является тип А .
Как в своей природной форме, так и в виде лекарства ботулотоксин представляет смесь различных белков. Основные составные их части — нейротоксин и нетоксичные протеины. Нейротоксин состоит из двух полипептидных цепей (легкой — массой 50 кДа и тяжелой — массой 100 кДа), соединенных одной дисульфидной группой и одним атомом цинка. Такая структура молекулы нейротоксина обуславливает лабильность ее конформации и неустойчивость к действию механических, физических и химических факторов, приводящих к потере биологической активности. В своей лекарственной форме нейротоксиновые цепи окружены и стабилизированы крупными пептидными молекулами гемагглютининов и нетоксичных негемагглютининовых протеинов. Большая молекулярная масса нетоксичной части комплекса (730 кДа) препятствует как расщеплению нейротоксина, так и быстрой диффузии его в окружающие ткани, обеспечивая тем самым локальность воздействия. Однако присутствие белковых молекул является фактором, способствующим образованию нейтрализующих антител ко всему нейротоксин-гемагглютининовому комплексу, что может явиться причиной вторичной нечувствительности пациентов к повторным инъекциям препарата .
Аминокислотный состав нейротоксина типа А расшифрован, в легкой цепи содержится 448 аминокислот, в тяжелой — 848. Другие серотипы ботулотоксина отличаются количеством и последовательностью аминокислот, главным образом, в легкой цепи .
Принципиальный механизм действия всех типов ботулинических токсинов заключается в пресинаптической блокаде выброса ацетилхолина из нервной терминали периферического холинергического синапса. Ацетилхолин является медиатором в синапсах парасимпатической нервной системы, некоторых синапсах ЦНС, в соматических двигательных и преганглионарных симпатических нервных окончаниях. Холинорецепторы находятся в скелетных и гладких мышцах, внутренних органах, симпатических и парасимпатических ганглиях. Выделяют М- и Н-холинорецепторы. Особым видом холинорецепторов является Н-холинорецепторы афферентных окончаний, расположенных в вегетативных ганглиях, где они по существу являются рецепторами сенсорного волокна .
Передача нервного импульса в холинергическом синапсе происходит в несколько этапов. В пресинаптической нервной терминали постоянно синтезируется и накапливается ацетилхолин в виде везикул, которые транспортируются к пресинаптической мембране, с тем, чтобы молекула медиатора могла выйти в синаптическую щель и связаться со специфическими холинергическими рецепторами постсинаптической мембраны. На этом участке постсинаптической мембраны возникает мембранный потенциал и происходит сокращение мышечного волокна. Однако процесс транспорта везикул ацетилхолина к пресинаптической мембране происходит не спонтанно, а активно с помощью комплекса особых транспортных белков, главными из которых являются SNAP-25, синтаксин и синаптобревин. Именно транспортные белки являются мишенью действия ботулинических нейротоксинов. При попадании ботулотоксина в мышцу или другой орган-мишень (с током крови при ботулизме или с лечебной целью при инъекции) молекулы токсинового комплекса достигают нервных терминалей аксонов, прикрепляются к ним, и далее нейротоксиновая часть внедряется в цитозоль нервной терминали, где распадается на короткую и длинную цепи. Короткая цепь (являющаяся цинк-зависимой протеазой) необратимо и специфично расщепляет транспортный белок, тем самым делая невозможным выход ацетилхолина в синаптическую щель и мышечное сокращение .
При внутримышечном введении ботулотоксина развиваются два эффекта: прямое ингибирование альфа-мотонейронов на уровне нервно-мышечного синапса и ингибирование гамма-мотонейронного холинергического синапса на интрафузальном волокне. Снижение гамма-активности ведет к расслаблению интрафузальных волокон мышечного веретена и уменьшает активность 1а-афферентов. Это приводит к снижению активности как мышечных рецепторов растяжения, так и эфферентной активности альфа- и гамма-мотонейронов. Клинически это проявляется в выраженном расслаблении инъецированных мышц и значительном уменьшении боли в них .
При локальном введении в терапевтических дозах, ботулотоксин не проникает через гематоэнцефалический барьер и не вызывает существенных системных эффектов .
Серотипы ботулотоксина различаются по своему сродству к транспортным белкам. Подтипы А и Е блокируют SNAP-25, подтипы В, D, F, G — синаптобревин, а подтип С блокирует синтаксин и SNAP-25. Процесс пресинаптического расщепления транспортных белков ботулотоксином является необратимым и занимает в среднем 30–60 минут, поэтому специфический ботулинический антитоксин эффективен лишь в течение получаса после поступления токсина к органам-мишеням. Несмотря на то, что клеточные эффекты развиваются очень быстро и необратимо, клиническое миорелаксирующее действие препарата после проведенной инъекции начинается проявляться через несколько дней. Однако имеются наблюдения как мгновенного наступления эффекта, так и отсроченного на 3–4 недели .
Через 1–2 месяца после инъекции начинается процесс отрастания новых нервных терминалей от аксонов, где прежде был блокирован транспорт ацетилхолина, с образованием новых функционально активных нервно-мышечных синапсов (спраутинг), что приводит в конечном итоге к восстановлению мышечных сокращений через 3–6 месяцев после инъекции, но иногда длительность эффекта сохраняется до 1 года и более .
Гистологическими исследованиями доказано, что даже после 30 повторных инъекций в одну и ту же мышцу не возникает необратимой деиннервации и атрофий .
Исключительно важной является разработка способов усиления и продления эффекта инъекции, поскольку частые повторные инъекции могут приводить к образованию антител, а также существенно удорожают стоимость лечения. Выявлено, что более стойкие и полные эффекты токсина проявляются при максимальном мышечном сокращении, при достаточной внутриклеточной концентрации ионов кальция (возможно и калия), при воздействии низких температур. Поэтому во время подготовки к лечебной инъекции за 2 недели пациенту рекомендуется назначить прием препаратов кальция и калия с витамином D, непосредственно перед инъекцией и сразу после нее — охлаждать область инъекции, а также интенсивно напрягать инъецируемые мышцы в течение 15–30 минут после процедуры .
Размер поля деиннервации, вызываемой инъекцией токсина, зависит от дозы токсина и объема вводимого раствора. Наилучшие результаты достигаются при равномерном распределении препарата в несколько точек вдоль одной мышцы. Кроме того, более полная блокада нервных терминалей наступает при инъекции токсина вблизи концевых моторных пластинок периферического нерва .
В настоящее время накопились факты, свидетельствующие о том, что эффекты ботулотоксина значительно сложнее и шире, чем временный локальный блок проведения в терминалях альфа-мотонейронов. По-видимому, имеется блокада как интрафузальных, так и экстрафузальных волокон, что может объяснить более широкую зону действия токсина и на терминали чувствительных волокон различной модальности. В частности, это может объяснить быстрый анальгетический эффект инъекции ботулотоксина. За счет механизма деафферентации рецепторов мышечных веретен и других видов чувствительных систем ботулотоксин может оказывать непрямые эффекты на вышележащие отделы центральной нервной системы. При исследовании моторного потенциала выявлено уменьшение латентных периодов его компонентов, снижение активации париетальной коры и каудальной дополнительной моторной области при позитронно-эмиссионной томографии, изменение реципрокного торможения на уровне спинного мозга у больных с постинсультными спастическими парезами .
В настоящее время в России разрешены к использованию следующие препараты ботулинического нейротоксина типа А: Ботокс (США), Диспорт (Великобритания), Ксеомин (Германия), Лантокс (Китай). Содержание токсинов в этих препаратах различно: Ботокс, Ксеомин и Лантокс содержит в 1 единице 0,4 нг нейротоксина, Диспорт — 0,025 нг (одна единица соответствует LD50 (средняя летальная доза ботулотоксина) для самок мышей Swiss-Webster весом 18–20 г). Токсичность (LD50) для обезьян составляет при внутримышечном введении 39 ЕД/кг, при внутривенном введении — 40 ЕД/кг .
Следует избегать назначения более чем 300–400 ЕД в течение одной сессии инъекции. К настоящему времени не выявлено серьезных побочных действий препаратов ботулотоксина при применении его в рекомендуемых дозах. Возможно возникновение чрезмерной мышечной слабости, однако со временем происходит восстановление мышечной силы. Может наблюдаться также вторичная резистентность к препарату, для профилактики которой рекомендуют делать интервал между сессиями инъекций не менее 12 недель. Не выявлено также эффекта взаимодействия ботулотоксина и пероральных миорелаксантов центрального действия .
На сегодняшний день широкое применение ботулинотерапии при постинсультной спастичности в значительной степени ограничивается высокой стоимостью препарата. Однако проведенное в Германии исследование по изучению эффективности трех вариантов лечения постинсультной спастичности: физиотерапия, ботулинотерапия + физиотерапия, баклофен + физиотерапия — показало, что снижение спастичности при сочетании ботулотоксина и физиотерапии было в три раза значительнее, чем при использовании баклофена и физиотерапии, и в десять раз больше, чем при применении одной физиотерапии. Оценка показателя стоимость/эффективность лечения постинсультной спастичности была ниже при использовании ботулотоксина и физиотерапии, чем при других методах лечения .
Для более обоснованного назначения препарата O’Brien С. рекомендует придерживаться следующего алгоритма назначения препаратов ботулотоксина при постинсультной спастичности (рис.).
В данном алгоритме С. O’Brien не рекомендует проведение ботулинотерапии при фиксированных контрактурах в суставах. В ситуации фиксированной контрактуры, вызванной укорочением сухожилий или дистрофическими изменениями в самом суставе, введение ботулотоксина приводит к расслаблению спастических мышц, но объем движения в суставе не увеличивается и двигательные функции остаются прежними. Однако, по мнению Е. Д. Белоусовой , ввиду наличия функционально невыгодной контрактуры (кисти, эквиноварусной деформации стопы), не обеспечивающей работоспособность конечности, выраженного болевого синдрома, введение ботулинического токсина в спастичные мышцы является обоснованным.
В настоящее время расчет дозы препарата ботулотоксина типа А, а также точки его введения в мышцы-мишени при различных проявлениях постинсультной спастичности определяют по рекомендациям Brin M. F. and Spasticity Study Group (табл.) .
По данным рекомендациям, минимальные дозы нейротоксина вводят при легкой степени спастичности, максимальные дозы — при выраженной степени спастичности и больших размерах мышц. Общая доза препарата не должна превышать 400 ЕД.
У всех пациентов с постинсультными спастическими двигательными расстройствами, в связи с повышением тонуса сгибателей запястья и пальцев рекомендуется обязательное введение ботулотоксина в следующие мышцы: лучевой сгибатель запястья по 20–40 ЕД, локтевой сгибатель запястья по 20–40 ЕД, поверхностный сгибатель пальцев по 20–40 ЕД, глубокий сгибатель пальцев по 30–60 ЕД. Общая доза препарата составляет 75–150 ЕД. Инъекции всех этих мышц (в 1–2 точки) осуществляются при введении инъекционной иглы в поперечном по отношению к предплечью направлению с поэтапным введением препарата в каждую мышцу. В остальные мышцы-мишени верхней конечности введение ботулотоксина зависит от клинического паттерна.
В нижней конечности, в связи с повышением мышечного тонуса в задней группе мышц голени, выясняется, какая из мышц задней группы голени (икроножная или камбаловидная) играет ведущую роль в спастичности. Если высокий тонус в голеностопном суставе (при тыльном сгибании стопы) определяется при разогнутом коленном суставе, но существенно ослабевает при сгибании, то это указывает на ведущую роль икроножной мышцы в спастичности, поскольку при сгибании колена происходит расслабление икроножной мышцы, участвующей как в сгибании колена, так и в подошвенном сгибании голеностопного сустава. В этих случаях вводят 100–150 ЕД ботулотоксина в четыре точки икроножной мышцы (по 25–35 ЕД в каждую точку). В тех случаях, когда спастичность в равной мере вызвана как икроножной, так и камбаловидной, дополнительно, в дозе 50–100 ЕД в две точки (по 25–50 ЕД), препарат вводят в камбаловидную мышцу. Выбор остальных мышц-мишеней ноги также зависит от клинического паттерна .
Максимальный эффект после проведения ботулинотерапии отмечается, в среднем, через 2–3 недели после проведения инъекций. Повторное нарастание мышечной спастичности происходит, как правило, через 4–6 месяцев после введения ботулотоксина, что требует повторения процедуры .
В заключение необходимо отметить, что во всех случаях после проведения ботулинотерапии требуется активная физиотерапия и физическая реабилитация. Ботулинотерапия не заменяет физиотерапию и лечебную физкультуру, что составляет основу реабилитационной программы у больных, перенесших мозговой инсульт, а представляет лишь интегральную часть комплексного восстановительного лечения, направленного на улучшения двигательных функций.
Значительное число вопросов, связанных с применением ботулинического токсина при спастичности, требуют дальнейшего изучения . Во-первых, безопасно и эффективно ли использование больших доз ботулотоксина, что часто необходимо при выраженной спастичности во многих мышцах у больных после мозгового инсульта? Во-вторых, в какие сроки с момента инсульта следует проводить ботулинотерапию? В-третьих, каковы оптимальные дозы и точки введения препарата в различные мышцы? В-четвертых, какая комбинация средств медицинской реабилитации и ботулинотерапии оптимальна в различных сроках давности заболевания?
Таким образом, проблема восстановительного лечения постинсультного спастического мышечного гипертонуса с использованием ботулотоксина в течение многих лет занимает одно из важных мест в практической неврологии и нейрореабилитации и требует дальнейшего изучения.
Литература
А. А. Королев, кандидат медицинских наук
ФГБУ «Всероссийский центр экстренной и радиационной медицины им. А. М. Никифорова» МЧС России, Санкт-Петербург
Контактная информация об авторе для переписки: koroland.dok@mail.ru
Гусев В.В.1,2, Львова О.А.2,3, Балуева Т.В.1
1МАУ «Центральная городская клиническая больница № 23», Екатеринбург, Россия; 2ФГАОУ ВО «Уральский федеральный университет им. первого Президента России Б.Н. Ельцина» Минобрнауки России, Екатеринбург, Россия; 3ФГБОУ ВО «Уральский государственный медицинский университет» Минздрава России, Екатеринбург, Россия ‘620017, Екатеринбург, ул. Старых Большевиков, 9; 2620002, Екатеринбург, ул. Мира, 19;
3620028, Екатеринбург, ул. Репина, 3
Опыт использования препарата Релатокс® в комплексной терапии спастичности руки
после инсульта
Цель исследования — оценка безопасности, эффективности и переносимости ботулотоксина А релатокс при спастичности руки после ишемического инсульта в рамках рутинной клинической практики.
Пациенты и методы. В исследование включено 7 пациентов, перенесших ишемический инсульт (давностью до 7лет) с признаками спастичности в верхней конечности. Все пациенты получали комплексное лечение, включавшее ежедневные занятия кинезоте-рапией и электростимуляцию парализованных конечностей. Через 6мес после инсульта или позднее проводилась однократная инъекция Релатокса® в мышцы предплечья парализованной руки. Выбор мышц осуществляли клинически и с помощью данных электромиографии. Оценку состояния пациента проводили до инъекции, через 2 нед и 3 мес.
Определяли изменения мышечного тонуса, двигательных возможностей кисти, степени самообслуживания, наличия субъективных ощущений и выраженности местных и системных реакций. Эффективность терапии оценивали клинически (шкала Эшворта, тест Френчай, индекс Бартел), а также на основании анализа видеомониторинга состояния пациента и учета мнения ухаживающего лица.
Все пациенты до включения в исследование получали лечение различными видами ботулинического нейротоксина типа А других производителей.
Результаты. Во всех случаях отмечена клиническая эффективность применения локального внутримышечного введения препарата ботулотоксина типа А Релатокс® в сочетании с кинезотерапией и электростимуляцией через 14 дней и через 3 мес после инъекции. Констатированы хорошая переносимость, эффективность и длительность действия Релатокса® в течение 3 мес наблюдения, сопоставимые с таковыми других препаратов ботулинического нейротоксина типа А. Не выявлено также побочных эффектов и нежелательных явлений.
Заключение. Накопление данных о дозах и действии препаратов для локальной терапии постинсультной спастичности, полученных разными клиническими центрами, возможность выбора препарата позволят улучшить лечение таких пациентов.
Ключевые слова: ботулотоксин; восстановительное лечение; инсульт; мышечный гипертонус; рефлексотерапия; спастический парез руки.
Контакты: Вадим Венальевич Гусев; gusev_vadim@inbox.ru
Для ссылки: Гусев ВВ, Львова ОА, Балуева ТВ. Опыт использования препарата Релатокс® в комплексной терапии спастичности руки после инсульта. Неврология, нейропсихиатрия, психосоматика. 2017;9(3):59—61.
Yekaterinburg, Russia
19, Starykh Bolshevikov St., Yekaterinburg 620017; 219, Mir St., Yekaterinburg 620002; 33, Repin St., Yekaterinburg 620028
Ежегодно в России регистрируется около 400 тыс. случаев инсульта, при этом почти у 30% выживших пациентов формируются признаки спастичности . По данным Всемирной организации здравоохранения, распространенность постинсультной спастичности достигает 200 на 100 тыс. жителей .
Под термином «спастичность» понимают двигательное нарушение, которое является частью синдрома поражения верхнего мотонейрона и характеризуется скорость-зависимым повышением мышечного тонуса и сухожильных рефлексов в результате гипервозбудимости рецепторов растяжения .
В комплексном лечении спастичности большое значение имеют кинезотерапия, а также использование различных групп миорелаксантов как центрального, так и периферического действия. При этом локальная терапия бо-тулотоксином продемонстрировала ряд несомненных преимуществ: хорошая переносимость, возможность строгого дозирования и введения в четко определенные мышцы-мишени.
В настоящее время в России разрешены к использованию следующие препараты ботулинического нейротоксина типа А: ботокс (США), диспорт (Великобритания), ксеомин (Германия), лантокс (Китай). С 2015 г. зарегистрирован первый отечественный препарат Релатокс®1, а с 2016 г. расширен спектр показаний к его применению, в частности, в показания введена спастичность мышц руки вследствие перенесенного инсульта. Препараты ботулинического нейрото-ксина типа А относятся к биологическим препаратам со сложным строением, индивидуальной рецептурой и трудно предсказуемой взаимозаменяемостью .
Проведенные клинические исследования этих препаратов существенно отличаются по количеству участников и качеству организации. В настоящее время в нашей стране опубликованы результаты только одного исследования, в котором оценивалась эффективность Релатокса® у пациентов с постинсультной спастичностью . Наличие широкого спектра препаратов ботулинического нейротоксина типа А ставит клиницистов перед непростым выбором и фактически приводит к необходимости приобретения собственного навыка работы с каждым из них.
Цель исследования — изучение и сравнение эффективности использования препарата Релатокс® в виде локальных внутримышечных инъекций в составе комплекс-
ной терапии для коррекции постинсультной спастичности и восстановления функции руки.
Пациенты и методы. Дизайн исследования — серия случаев. Исследование проводилось как наблюдательное в рамках повседневной клинической практики. В исследование включено 7 пациентов с постинсультной спастично-стью в верхней конечности. Критериями включения в исследование были наличие ишемического инсульта в анамнезе (срок давности инсульта — от 6 мес до 7 лет), развившийся в результате перенесенного инсульта спастический гемипа-рез, информированное согласие пациента или его законного представителя на лечение.
Все пациенты получали комплексное лечение, включавшее ежедневные занятия кинезотерапией по 45 мин 2 раза в сутки с инструктором, электростимуляцию парализованных конечностей. Все они были обучены методикам самостоятельных занятий, проинформированы о необходимости их регулярного и длительного выполнения.
Для коррекции спастичности пациентам вводили Ре-латокс® в мышцы предплечья парализованной руки. Инъекции проводили в соответствии с инструкцией к препарату Выбор мышц осуществлялся клинически и с помощью данных электромиографии (аппарат «МИСТ», Нейротех). На одну процедуру использовали 140 ед. препарата, разделенных в равной пропорции на 4 или 5 мест инъекций. Эффективность терапии оценивали клинически: по шкале Эшвор-та (допускались оценки в 0,5 балла), тесту Френчай, индексу Бартел, а также на основании анализа видеомониторинга и учета мнения ухаживающего лица.
Все пациенты до включения в исследование получали лечение различными видами ботулинического нейротокси-на типа А других производителей (от 2 до 12 инъекций). Оценку состояния пациента проводили до инъекции, через
2 нед и через 3 мес.
Результаты и обсуждение. У всех пациентов зафиксировано улучшение состояния в виде уменьшения спастич-ности в дистальных отделах руки (шкала Эшворта) и повышения двигательных возможностей кисти (тест Френчай), степени самообслуживания (индекс Бартел) через 2 нед после инъекции и относительная стабильность достигнутых после терапии результатов на протяжении последующих
3 мес (см. таблицу).
Субъективно все пациенты перенесли инъекции хорошо, признаков системных и местных осложнений не зафи-
‘НПО «Микроген» (Россия).
Показатели у пациентов с постинсультной спастичностью в мышцах руки до и после применения релатокса
ксировано. Пациенты оценивали действие препарата в сравнении с опытом предыдущих инъекций: 5 пациентов
указали на хороший эффект, 1 — на отличный и 1 — на удовлетворительный.
Анкетирование ухаживающих за пациентом лиц и анализ видеозаписей состояния пациента до и после исследования также свидетельствовали об улучшении функции спастичной конечности на фоне лечения.
Нами показана клиническая эффективность локального внутримышечного введения препарата ботулиниче-ского нейротоксина типа А Релатокса® в сочетании с кине-зотерапией и электростимуляцией у небольшой группы пациентов с постинсультной мышечной спастичностью верхней конечности. По данным тестов, оценивающих субъективные данные и ощущения пациентов, в течение 3 мес наблюдения Релатокс® характеризовался сопоставимой переносимостью, эффективностью и длительностью действия с препаратами ботулотоксина типа А, которые пациентам назначали ранее. Не зафиксировано побочных эффектов, нежелательных явлений, отмечена хорошая переносимость первого отечественного препарата ботулинического нейро-токсина типа А.
Заключение. Применение препаратов ботулинического нейротоксина типа А в строгом соответствии с рекомендациями производителей, накопление данных об их дозах и действии при локальной терапии постинсультной спастичности, полученных разными клиническими центрами, возможность выбора препарата в зависимости от опыта врача, выполняющего инъекции, и типа финансирования лечебного учреждения, — все это позволяет улучшить результаты лечения и является важным компонентом реабилитации пациентов со спастическим парезом верхней конечности.
№ пациента Исходно Через 14 дней Через 3 мес
Тонус мышц предплечья (шкала Эшворта, баллы)
1. 3,5 2,5 2,5
2. 2 1 2
3. 1,5 1,0 1,0
4. 3,5 1,5 1,5
5. 2,0 2,0 1,0
6. 3,5 3,0 2,0
7. 2,5 2,0 2,5
Двигательные возможности кисти (тест Френчай, баллы)
1. 3 4 4
2. 3 5 5
3. 4 5 5
4. 2 4 3
5. 2 2 2
6. 1 2 1
7. 3 2 2
Степень самообслуживания (индекс Бартел, баллы)
1. 85 90 90
2. 80 80 80
3. 100 100 100
4. 80 90 100
5. 85 85 90
6. 70 80 80
7. 85 95 100
3. Кадыков АС, Черникова ЛА, Шахпароно-ва НВ. Реабилитация неврологических больных. Москва: МЕДпресс-информ; 2009.
ЛИТЕРАТУРА
a handbook of the medical practitioner]. 5th ed. Moscow: MEDpress-inform; 2007. 960 p.]
5. Завалишин ИА, Сгойда НИ, Шитикова ИЕ. Клиническая характеристика синдрома верхнего мотонейрона. В кн.: Завалишин ИА, редактор. Синдром верхнего мотонейрона. Самара: Самарское отделение Литфонда; 2005. С. 11-54. . Samara: Samarskoe otdelenie Litfonda; 2005. P. 11-54.]
6. Артеменко АР, Куренков АЛ, Беломесто-ва КВ. К вопросу об отсутствии взаимоза-
меняемости лекарственных препаратов ботулинического токсина типа А. Медицинский совет. 2015;(5):112-23. . 7. Хатькова СЕ, Костенко ЕВ, Похабов ДВ и др. Оценка безопасности и эффективности российского препарата ботулотоксина А Релатокс® в сравнении с Ботоксом® при спастичности руки после ишемического инсульта (мультицентровое рандомизированное исследование). Неврология, нейропси-хиатрия, психосоматика. 2017;9(1):71-7. . doi:10.14412/2074-2711-2017-1-71-77
Поступила 30.08.2017
Декларация о финансовых и других взаимоотношениях
Исследование проведено при поддержке НПО «Микроген». Авторы несут полную ответственность за предоставление окончательной версии рукописи в печать. Все авторы принимали участие в разработке концепции статьи и написании рукописи. Окончательная версия рукописи была одобрена всеми авторами.
Ботулинотерапия — это направление современной клинической и теоретической медицины, которое изучает механизмы действия ботулотоксина и разрабатывает методы лечения различных заболевания и синдромов. Лечение осуществляется за счет местных инъекций препаратов, оно высокоэффективно и практически не имеет побочных действий. Врачи отделения неврологии Клинического госпиталя на Яузе специализируются на данном виде терапии и накопили большой опыт в области лечения различных заболеваний.
Суть метода
Ботулотоксин — вещество, способное блокировать передачу сигнала между нервами и мышцами за счет блокирования выброса ацетилхолина. Без этого вещества невозможна передача нервного импульса. В результате после введения в организм препаратов ботулотоксина мышцы в том месте, где произведена инъекция, расслабляются. Это важно для лечения спастичности, то есть повышенного мышечного тонуса, и других двигательных расстройств.
Дозировка препарата и место введения определяются индивидуально после осмотра врача. Спустя несколько месяцев после инъекции подвижность мышцы восстанавливается. В зависимости от индивидуальной чувствительности, эффект от инъекции препарата ботулотоксина может сохраняться от 3 месяцев до года.
Показания к применению
В отделении неврологии Клинического госпиталя на Яузе ботулинотерапия применяется для коррекции патологически измененного мышечного тонуса, болевых синдромов, вегетативных расстройств. Основные показания к применению ботулотоксина:
- дистонии — постоянное или спазматическое сокращение мышц (блефароспазм, гемифациальный спазм, спастическая кривошея, писчий спазм, энтропион)
- спастичность (постинсультная, посттравматическая, последствия нейроинфекций, ДЦП)
- тики, тремор головы, треморы конечностей
- гипергидроз — повышенное потоотделение
- болевые синдромы, в том числе хроническая головная боль (мигрень)
- бруксизм — скрежет зубами
- гипертонус жевательных мышц
- локальная хроническая боль (в частности, невралгия)
- слюнотечение и слезотечение (синдром крокодиловых слез, холодовая аллергия)
Как отмечают специалисты, ботулинотерапия расширяет терапевтические возможности врачей: с ее помощью они могут лечить заболевания, которые раньше не поддавались терапии.
Обратите внимание
Опыт клинического применения препаратов ботулотоксина показывает, что эта терапия практически не имеет побочных эффектов (иногда отмечается, например, болезненность в месте инъекции и др.). Как правило, даже те неприятные ощущения, которые могут возникнуть, проходят сами, и пациент не нуждается в дополнительном лечении.
Противопоказаниями к применению препаратов ботулотоксина:
- заболевания с нарушением нервно-мышечной передачи
- повышенная чувствительность к компонентам препарата
- воспалительный процесс или инфекций в месте, где производится инъекция
- острые инфекционные заболевания
- гемофилия