Безопасные статины
Цель обзора. Описать роль ингибиторов гидроксиметилглутарил-КоА-редуктазы в снижении частоты сердечно-сосудистой заболеваемости и смертности с позиций доказательной медицины и возможность применения статинов у больных с неалкогольной жировой болезнью печени в рамках метаболического синдрома.
Сердечно-сосудистые заболевания служат основными причинами инвалидизации и смертности во всём мире. В основе патогенеза этих заболеваний лежит атеросклероз – одна из главнейших проблем современной медицины. В достаточно большом количестве исследований была показана возможность снижения частоты сердечно-сосудистой заболеваемости и смертности вплоть до 42% за счёт снижения уровня липопротеидов низкой плотности. Это стало возможным благодаря применению основного класса гиполипидемических препаратов — статинов. Уникальность статинов заключается не только в способности значимо снижать синтез холестерина, но и в наличии у них целого ряда других свойств, объединенных под названием «плейотропных эффектов». В связи с неуклонным ростом пациентов с метаболическим синдромом, высоким риском сердечно-сосудистых осложнений, назначение статинов неизбежно. Известно, что атерогенная дислипидемия у таких пациентов в большинстве случаев сочетается с неалкогольной жировой болезнью печени. В России приверженность к терапии статинами крайне низкая (в 2001 году только 0,6% больных острым инфарктом миокарда принимали статины). Среди множества возможных причин недостаточного использования статинов в нашей стране сохраняет актуальность вопрос безопасности назначения этого класса препаратов. Результаты проведённых исследований показывают, что у лиц с исходно повышенным уровнем печёночных трансаминаз в силу различных причин приём статинов не вызывает повышенного риска гепатотоксичности (клинически значимое повышение активности печеночных ферментов у 0,8% больных против 0,6% случаев в группе плацебо). Также имеются данные о том, что эффективность комбинации малых доз статинов и урсодезоксихолевой кислоты выше, чем использование удвоенной дозы статинов. В статье рассмотрены вопросы необходимости и безопасности применения статинов у больных с неалкогольной жировой болезнью печени.
Заключение. Назначение статинов для первичной и вторичной профилактики заболеваний сердечно-сосудистой системы сможет предотвратить десятки тысяч преждевременных смертей. Результаты большого числа исследований позволяют говорить об эффективности и безопасности назначения симвастатина пациентам с неалкогольной жировой болезнью печени в рамках комплексной терапии метаболического синдрома Совместное применение статинов и урсодезоксихолевой кислоты обосновано в качестве патогенетической терапии НАЖБП, а также гиполипидемической терапии у больных с метаболическим синдромом.
Сердечно-сосудистые заболевания (ССЗ) (ишемическая болезнь сердца — ИБС, цереброваскулярная болезнь, окклюзивные заболевания периферических артерий) служат основными причинами инвалидизации и смертности во всём мире. В основе патогенеза этих заболеваний лежит атеросклероз – одна из главнейших проблем современной медицины. История пристального изучения сущности процессов, лежащих в основе атеросклероза, длится уже более века. В настоящее время имеется чёткое представление об атеросклерозе как мультифакториальном заболевании, динамичном процессе, прогрессирующем в сосудистой системе десятилетиями и имеющем возможность обратного развития изменений в стенке артерии. Со временем процесс неумолимо прогрессирует, нередко проявляясь внезапно, зачастую фатально (внезапная коронарная смерть или инфаркт миокарда).
Как известно, большинство случаев ИБС возникает на фоне длительного сосуществования факторов риска, среди которых особое значение имеют нарушения липидного обмена. Утверждение «без атерогенных липопротеидов не будет атеросклероза» подтверждают результаты наиболее крупных эпидемиологических исследований (Фремингемское, MRFIT, исследование 7 стран), в которых была показана отчетливая прямая корреляция между концентрацией холестерина в крови и уровнем смертности от ИБС (рис. 1) .
Рисунок 1. Показатели смертности от ИБС в зависимости от уровня ХС.(Данные исследования MRFIT)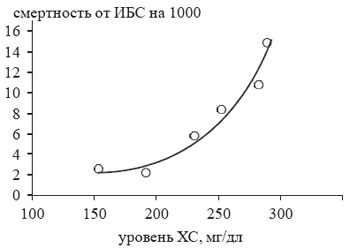
Нарушения липидного обмена играют одну важную роль в патогенезе заболеваний, ассоциированных с атеросклерозом. Наглядным доказательством этому могут служить результаты недавно завершившегося международного исследования INTERHEART, в которое были включены 15152 пациента с острым инфарктом миокарда (случай) и 14820 людей без явных признаков ишемической болезни сердца (контроль) из 52 стран мира . Целью этого исследования было изучение взаимосвязи острого коронарного синдрома и 9 факторов риска (дислипидемия, курение, артериальная гипертензия, ожирение, сахарный диабет, стресс/депрессия, употребление алкоголя, потребление овощей и фруктов и физическая активность). Оказалось, что вне зависимости от пола, национальности и социально-этнических условий в развитии острого инфаркта миокарда дислипидемия занимает первое место среди всех факторов риска .
Во Фремингемском проспективном эпидемиологическом исследовании, которое началось в 50-е годы прошлого столетия и продолжается до сих пор, были определены оптимальные уровни липопротеидов высокой плотности (ЛПНП), общего холестерина (ОХС), триглицеридов (ТГ) и липопротеидов высокой плотности (ЛПВП), как основных липидных факторов риска кардиоваскулярных исходов атеросклероза. Однако результаты исследований последнего десятилетия свидетельствуют о неравнозначном вкладе различных классов липидов в риск ССЗ. Например, во внутрипопуляционном исследовании PROCAM (Prospective Cardiovascular Munster Study) была доказана опасность ассоциации низкого уровня ЛПВП, гипертриглицеридемии и умеренно повышенных значений уровня ЛПНП . В проспективном исследовании AMORIS (Apolipoprotein Mortality Risk Study) получено подтверждение того, что Апo B является более чувствительным маркером риска ССЗ, а размеры и плотность частиц ЛПНП — более сильные предикторы неблагоприятных сосудистых событий, чем ОХС и ЛПНП. Также доказано, что отношение АпоВ/АпоА-1 является наиболее мощным предиктором риска развития ишемического инсульта .
В достаточно большом количестве исследований была показана возможность снижения частоты ССЗ и смертности вплоть до 42% за счёт снижения уровня ЛПНП . Это стало возможным благодаря применению нового класса гиполипидемических препаратов — статинов.
Открытие и внедрение в практику ингибиторов гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоАредуктазы) — основного фермента, регулирующего биосинтез холестерина в гепатоцитах, стало одним из самых ярких достижений второй половины XX века. Создав в 1976 году первый статин, японский исследователь Akira Endo вряд ли мог даже предположить, что спустя 30 лет его назовут «открывателем «пенициллина» для холестерина» (discaverer of a «Penicillin for cholesterol») . Совершенно два разных класса препаратов совершили революционный переворот в медицине: применение антибиотиков предотвратило смертельные исходы миллионов людей от инфекций, а под влиянием статинов стала уязвимой самая распространённая, многоликая опасная болезнь – атеросклероз.
Многочисленные крупнейшие многоцентровые плацебо-контролируемые исследования (4S, CARE, LIPID, WOSCOPS, AF CAPS/TexCAPS, HPS, CARDS и др.) доказали высокую эффективность статинов при атерогенной дислипидемии в аспекте снижения частоты сердечно-сосудистых осложнений, в том числе снижения риска преждевременной смерти у больных с клиническими проявлениями атеросклероза .
Основополагающим среди этих работ следует считать скандинавское исследование 4S (Scandinavian Simvastatin Survival Study). Это было первое длительное (5,4 года) плацебо-контролируемое исследование с использованием симвастатина (использовался препарат «Зокор”) 20–40 мг/сут, в котором участвовало 4444 человека с ИБС. В этой работе впервые изучалось влияние лечения симвастатином на сердечно-сосудистую и общую смертность. Исследуемая популяция – больные ИБС после инфаркта миокарда в анамнезе, в возрасте 35–70 лет, с исходным уровнем общего холестерина 213–309 мг/дл. Снижение уровня ЛПНП за 5 лет наблюдения составило 36%, что привело к снижению общей смертности на 30% (p=0,0003). Количество больших коронарных событий снизилось на 34%, сердечно-сосудистая смертность – на 42%, необходимость в операциях ревакуляризации миокарда – на 37%. Это исследование во многом развеяло сомнения о необходимости гиполипидемической терапии у больных ИБС с целью профилактики ее осложнений и ответило на многие вопросы по безопасности такого лечения. Результаты этого эпохального исследования в значительной мере способствовали развитию препаратов статинов как класса .
Необходимо обратиться и к исследованию HPS (Heart Protection Study) – самому крупному исследованию последнего времени, в котором участвовало 20 536 пациентов: 50% больных принимали симвастатин (использовался препарат «Зокор”), 50% – плацебо. С учетом дизайна исследования половина больных принимали антиоксидантный коктейль: витамин Е (600 мг) + витамин С (250 мг) и ?-каротин (20 мг), половина – витамины-плацебо. По основным результатам HPS прием cимвастатина в дозе 40 мг/сут в течение 5 лет позволил достоверно снизить сердечно-сосудистую смертность на 17%, частоту любого большого сердечно-сосудистого осложнения на 24% (p
Уникальность статинов заключается не только в способности значимо снижать синтез холестерина, но и в наличии у них целого ряда других свойств, объединенных под названием «плейотропных эффектов». Разнообразие плейотропных эффектов статинов вероятно в недалёком будущем позволит использовать этот класс препаратов для лечения не только кардиологических пациентов. Экспериментальные и клинические данные всё больше дают доказательств, свидетельствующих о необходимости расширения «терапевтической ниши» статинов. Наибольшее значение имеют такие плейотропные эффекты статинов, как: улучшение эндотелиальной функции (это свойство статинов проявляется уже при малых дозах и для этого не требуется продолжительных сроков лечения), ингибирование пролиферации и миграции гладкомышечных клеток; снижение агрегации тромбоцитов, противовоспалительное действие, улучшение состояния фибринолитической системы. Появляется всё больше данных об эффективности статинов у лиц с болезнью Альцгеймера, рассеянным склерозом, хронической сердечной недостаточностью, почечной недостаточностью . Корейские ученые на экспериментальных моделях мышей при анализе влияния симвастатина на рост опухоли получили результаты, свидетельствующие о противоопухолевом потенциале симвастатина в отношении рака толстой кишки .
«В лице» статинов врачи получили эффективное и безопасное средство стационарного и амбулаторного применения, которое вошло в фармакопейные списки «обязательных» препаратов многих стран мира. По данным европейского исследования EUROASPIRE, в котором ведётся наблюдение за динамикой факторов риска и ССЗ, в Европе назначение статинов за последнее десятилетие возросло с 32,2% до 88,8%, однако, достижение целевых уровней ЛПНП остаётся на уровне 40%. Одной из основных проблем, как в Западной так и в Восточной Европе, является низкая приверженность пациентов к терапии статинами . Далеко не так радужно обстоят дела в России. По данным USA Food and drug administration от 2005 года Российская Федерация оказалась в числе мировых лидеров по потреблению лекарств (по объемам потребления готовых лекарственных средств — 12-е место в мире и 6-е в Европе). Но статины не вошли даже в десятку наиболее используемых лекарственных средств. Точной статистики, доказывающей частоту использования статинов российскими пациентами нет, однако имеющиеся отдельные данные свидетельствуют о крайне неблагоприятной ситуации, сложившейся вокруг этого класса препаратов. Так, по данным многоцентрового исследования VALIANT, в котором принимала участие и Россия, к 2001 году лишь 0,6% наших соотечественников, перенесших острый инфаркт миокарда, получали статины (рис. 2) .
В связи с неуклонным ростом пациентов с метаболическим синдромом (МС), высоким риском сердечно-сосудистых осложнений, назначение статинов неизбежно. Известно, что атерогенная дислипидемия у таких пациентов в большинстве случаев сочетается с неалкогольной жировой болезнью печени (НАЖБП). НАЖБП является малосимптомной болезнью, не оказывающей существенного влияния на качество жизни вплоть до развития терминальных форм. В то же время основные причины смерти больных с НАЖБП связаны с сердечно-сосудистой патологией. В долговременном исследовании, проведенном в Швеции, показано, что за 15 лет наблюдения из 129 пациентов с морфологически доказанной НАЖБП, сопровождавшейся «хронической гипертрансаминаземией», 12,7% умерли от сердечно-сосудистых заболеваний, и только 1,6% — от печёночной патологии . Поэтому НАЖБП, как одно из проявлений МС, могла бы стать самостоятельной нишей для статинов в гепатологии.
Среди множества возможных причин недостаточного использования статинов в нашей стране сохраняет актуальность вопрос безопасности назначения этого класса препаратов. Исследование Chalasani N. с соавт. продемонстрировало, что у лиц с исходно повышенным уровнем печёночных трансаминаз в силу различных причин приём статинов не вызывает повышенного риска гепатотоксичности . Исследование HPS, проводимое с включением более 20 тыс. человек, длительно получавших симвастатин, показало относительную безопасность их приема — клинически значимое повышение активности печеночных ферментов отмечалось у 0,8% больных (против 0,6% случаев в группе плацебо).
Существует ли риск гепатотоксичности статинов при лечении дислипидемии у пациентов с МС? Известно, что повышение печёночных ферментов – наиболее частый побочный эффект статинов – наблюдается в 0,5-2% случаев и зависит от дозы препарата. Хотя заболевания печени и стоят в перечне противопоказаний для применения статинов, до сих пор не описаны случаи ухудшения течения заболеваний печени на фоне приёма этого класса лекарственных препаратов. Существует ряд исследований, результаты которых показали эффективность и безопасность использования статинов в лечении атерогенной дислипидемии у больных с МС .
Согласно Докладу Комитета по безопасности лечения статинами Национальной Липидной Ассоциации США терапия статинами может быть рекомендована пациентам с хроническими болезнями печени, неалкогольным стеатогепатитом, жировой инфильтрацией печени под тщательным контролем уровня активности печёночных ферментов .
Если больному показан приём статинов, а уровень печёночных трансаминаз превышает 2-3-кратную норму, то на помощь клиницисту может прийти урсодезоксихолевая кислота (УДХК). Назначение УДХК патогенетически обоснованно при НАЖБП . УДХК представляет собой лекарственный препарат плейотропного действия, что выражается в наличии холеретического, цитопротективного, иммуномодулирующего, антиапоптотического, гипохолестеринемического и литолитического механизмов действия. Применение УДХК при НАЖБП с повышенным уровнем трансаминаз в дозе 10-15 мг/кг в сутки, длительностью 6 месяцев и более оказывает положительное влияние на биохимические показатели, ведёт к снижению активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы (ЩФ), гаммаглутамилтранспептидазы (ГГТ) и уменьшению выраженности стеатоза и воспаления по данным гистологического исследования печени . После нормализации уровня АСТ, АЛТ на фоне приёма УДХК больному можно назначать статины.
В литературе также имеются данные о том, что эффективность комбинации малых доз статинов и УДХК выше, чем использование удвоенной дозы статинов. В испанском исследовании при комбинированной терапии симвастатином 20мг/сут и УДХК 300мг/сут в течение 4 месяцев, по сравнению с монотерапией симвастатином 40мг/сут, было достигнуто более выраженное снижение уровня ЛПНП (р=0,0034). Аналогичный результат был получен в этом же исследовании в группе больных, принимавших аторвастатин в дозе 20мг/сут и УДХК 300мг/сут в течение 4 месяцев, по сравнению с монотерапией аторвастатином 40мг/сут (р=0,0037). .
Нужно отметить, что исследования, в которых изучалась комбинированная терапия статинов и УДХК, немногочисленны, но вместе с тем, добавление УДХК в схему гиполипидемической терапии статинами у больных с НАЖБП оправдано.
Приводим клиническое наблюдение .
Больная Д., 73 лет, поступила в отделение реанимации и интенсивной терапии клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии имени В.Х. Василенко (директор клиники – академик РАМН, профессор В.Т. Ивашкин) в декабре 2007 года с жалобами на:
- ощущение тяжести за грудиной;
- выраженную головную боль в затылочной области на фоне повышения АД максимально до 240 и 110мм рт.ст.;
- приступы ночного удушья;
- боли в ногах при ходьбе, похолодание стоп;
- отёки голеней и стоп;
- общую слабость, быструю утомляемость.
Из анамнеза известно, что после вторых родов в 35 лет стала отмечать значительную прибавку в весе. С 44 лет стали беспокоить головные боли на фоне повышения АД до 180 и 90 мм.рт.ст., по поводу чего наблюдалась у врача по месту жительства, лечилась нерегулярно, цифры АД оставались повышенными. В 1998 году в возрасте 63 лет впервые появилось чувство тяжести за грудиной, возникающее при умеренной физической нагрузке и проходящее в покое. Не обследовалась, регулярной терапии не получала. В 2000 году в возрасте 65 лет больная перенесла лапароскопическую холецистэктомию по поводу калькулёзного холецистита, тогда же было выявлено повышение уровня глюкозы, рекомендовано обращение к эндокринологу. Однако больная больше к врачам не обращалась, не лечилась. Значительное ухудшение самочувствия в течение последних 8 месяцев, когда стали нарастать вышеуказанные жалобы. По тяжести состояния больная была госпитализирована в отделение реанимации и интенсивной терапии клиники.
Пациентка не курит, ведёт малоподвижный образ жизни, пищевое поведение – чрезмерное. Семейный анамнез отягощен по ССЗ: мать и отец страдали ГБ и СД 2 типа, умерли в возрасте 67 и 69 лет соответственно.
При поступлении: общее состояние средней тяжести. Сознание ясное. Обращало на себя внимание наличие абдоминального ожирения: масса тела 123кг, ИМТ = 45,2 кг/м2 (морбидное ожирение), Обхват талии (ОТ) =153см, обхват бедер (ОБ) =168см, ОТ/ОБ =0,91. Кожные покровы бледно-розового цвета. Умеренный цианоз губ. Ксантелазмы на верхних веках. Положительный симптом Фрэнка. Отеки голеней и стоп. Пульсация сосудов нижних конечностей резко снижена. При перкуссии грудной клетки ясный лёгочный звук с коробочным оттенком. Дыхание ослабленное везикулярное, ниже угла лопаток с обеих сторон выслушиваются влажные незвонкие мелкопузырчатые хрипы в умеренном количестве. ЧДД 22 в мин. При осмотре область сердца не изменена. Границы относительной тупости сердца смещены влево на 1,5см кнаружи от срединно-ключичной линии. При аускультации I тон ослаблен, акцент II тона над аортой, систолический шум на аорте с проведением на сонные артерии, короткий систолический шум на верхушке. Пульс ритмичный, ЧСС 81 уд. в мин., p. durus, АД 230 и 100 мм. рт. ст. Живот значительно увеличен в размерах за счет избыточного подкожно-жирового слоя, видны множественные стрии белесого цвета, мягкий, безболезненный при пальпации (рис. 3). При перкуссии печень на 2 см ниже края рёберной дуги по правой срединно-ключичной линии. Симптом поколачивания по поясничной области отрицателен с обеих сторон.
Рисунок 3. Абдоминальное ожирение у больной Д., 73 лет.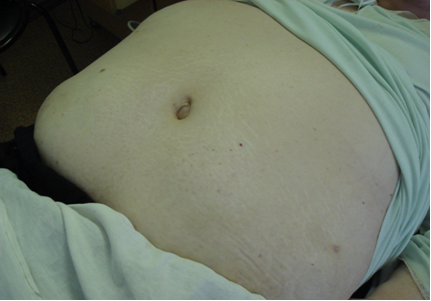
В отделении реанимации и интенсивной терапии при исследовании уровня кардиоспецифических ферментов и ЭКГ в динамике острое очаговое повреждение миокарда было исключено. На фоне проводимой терапии (антиагреганты, антикоагулянты, нитраты, антигипертензивные препараты) тяжесть за грудиной и приступы ночного пароксизмального удушья не рецидивировали, уменьшилась одышка, повысилась толерантность к физическим нагрузкам, уменьшились отёки голеней и стоп. Однако сохранялась артериальная гипертензия на уровне 160-180 и 90мм рт.ст. Для дальнейшего обследования и подбора терапии больная была переведена в отделение кардиологии.
При лабораторно-инструментальном обследовании в отделении кардиологии были выявлены:
- в биохимическом анализе крови признаки атерогенной дислипидемии: ОХС – 284 мг/дл, ТГ – 345 мг/дл, ЛПВП – 45 мг/дл, ЛПНП – 172 мг/дл, ЛПОНП – 67 мг/дл; индекс атерогенности – 5.3, тип дислипидемии – IIb.
- повышен уровень АЛТ (76 ед/л), АСТ (70ед/л), индекс де Ритиса 0,92.
- с целью неинвазивного определения вероятности развития фиброза у больной с метаболическим синдромом, страдающей неалкогольной жировой болезнью печени применяли тест APRI, расчёт которого проводили по формуле: АСТ ? 100 / ((верхний предел АСТ) ? тромбоциты (10^9/л) = 0,58 (вероятность мала).
- показатели инсулинового обмена: глюкоза — 138 мг/дл, ИРИ – 29 МкМЕ/мл, С-пептид – 1680пмоль/л. Рассчитывали количественный контрольный индекс чувствительности к инсулину – QUICKI – тест (QUICKI=1/, где I0 – базальное содержание инсулина в крови, G0 – базальное содержание глюкозы в крови): 0,278, что подтверждало наличие высокой степени инсулинорезистентности. У больной диагностирован СД 2 типа, средней тяжести, в стадии субкомпенсации.
- ЭКГ – синусовый ритм с ЧСС 84 в мин., признаки гипертрофии ЛЖ.
- Эхо-КГ – атеросклероз аорты, гипертрофия миокарда левого желудочка (МЖП – 1,35см, ЗС ЛЖ – 1,2см), ФВ 42%. Стеноз устья аорты атеросклеротического генеза.
- суточное мониторирование АД: тип пациента – non-dipper.
- УЗИ органов брюшной полости: печень не увеличена, контуры ровные, паренхима гиперэхогенная с явлениями выраженной жировой инфильтрации. Желчный пузырь удалён. Поджелудочная железа не увеличена, контуры нечёткие, паренхима повышенной эхогенности. Селезёнка не увеличена. Почки – без особенностей.
На основании жалоб, анамнеза, объективного исследования, данных лабораторно-инструментальных методов обследования был сформулирован следующий клинический диагноз:
Сочетанные заболевания:
Ишемическая болезнь сердца: стенокардия напряжения III Ф.К.
Сахарный диабет 2 типа, средней тяжести, фаза субкомпенсации.
Фоновые заболевания: Гипертоническая болезнь II стадии, очень высокого риска. Атеросклероз аорты, коронарных, мозговых артерий. Атеросклеротический порок сердца: стеноз устья аорты. Атеросклеротический кардиосклероз. Абдоминальное ожирение 3 степени. Дислипидемия IIb типа.
Осложнения основного заболевания: НК 2Б стадии. NYHA III ф.кл.
Сопутствующие заболевания: Желчнокаменная болезнь: лапароскопическая холецистэктомия в 2000 году.
Больной были даны диетические рекомендации, объяснена необходимость дозированной физической нагрузки. Газначена комбинированная антигипертензивная терапия (индапамид 2,5 мг/сут, лизиноприл 10 мг/сут, амлодипин 5 мг/сут), пролонгированные мононитраты (мономак 40 мг/сут), метформин 1000 мг/сут, антиагреганты (аспирин в дозе 100 мг/сут). Кроме того, учитывая наличие у больной атерогенной дислипидемии, а также признаков неалкогольного стеатогепатита, была назначена комбинированная гиполипидемическая терапия (симвастатин 40 мг/сут + препарат урсодезоксихолевой кислоты в дозе 1250 мг/сут). В данной комбинации препарат урсодезоксихолевой кислоты выступил также в роли патогенетического лечения неалкогольного стеатогепатита.
За время наблюдения в клинике на фоне проводимой терапии отмечалась положительная динамика в состоянии больной: ангинозные боли и одышка не беспокоили, повысилась толерантность к физическим нагрузкам, значительно уменьшились отёки голеней и стоп, уменьшилась общая слабость. Пациентка была выписана с рекомендациями продолжения вышеуказанного лечения и регулярного наблюдения в амбулаторных условиях.
При амбулаторном обследовании через 1 месяц: жалоб нет, АД 160 и 90мм рт.ст., АСТ 54 ед/л, АЛТ 61 ед/л, КФК 87 ед/л.
При амбулаторном обследовании через 3 месяца: новых жалоб нет, АД 150/80 мм рт.ст., ангинозные приступы не рецидивировали, показатели липидного обмена несколько улучшились. Учитывая сохраняющуюся выраженную атерогенную дислипидемию, доза симвастатина была увеличена до 60 мг/сут. При контроле сывороточных трансаминаз: АСТ 51 ед/л, АЛТ 55 ед/л.
При проведении повторного обследования ещё через 3 месяца (спустя 6 месяцев от начала лечения): ангинозные приступы не беспокоят, периферических отёков нет, уменьшились боли в ногах при ходьбе, несколько повысилась толерантность к физическим нагрузкам. Пациентка снизила массу тела с 123 до 119кг, ОТ =149см, ОТ/ОБ =0,89, ИМТ =43,7. АД 135 и 80мм рт.ст. Улучшились лабораторные показатели: АСТ 40 ед/л, АЛТ 44 ед/л, КФК 74 ед/л, индекс APRI уменьшился до 0,34. Целевые значения липидов крови пока не достигнуты, однако показатели липидного обмена значительно улучшились: ОХС – 248 мг/дл, ТГ – 210 мг/дл, ЛПВП – 55 мг/дл, ЛПНП – 157 мг/дл, ЛПОНП – 36 мг/дл; индекс атерогенности – 3,5. Нормализовался уровень глюкозы (гликемия натощак = 100 мг/дл), уменьшилась степень инсулинорезистентности (QUICKI – тест =0,296). При контрольном УЗИ органов брюшной полости – уменьшилась степень жировой инфильтрации печени: с выраженной до умеренной. Пациентка продолжает регулярный приём подобранной терапии, наблюдение в нашей клинике.
Данное клиническое наблюдение демонстрирует больную с множественной сочетанной патологией в рамках МС. Обращают на себя внимание следующие клинические особенности, связанные с трудностями подбора терапии:
- пожилой возраст больной;
- наличие морбидного ожирения;
- атерогенная дислипидемия с выраженными клиническими проявлениями;
- выраженная артериальная гипертензия;
- высокая степень инсулинорезистентности;
- наличие сочетанной патологии, в том числе неалкогольная жировая болезнь печени.
Однако улучшение состояния больной и положительная динамика лабораторно-инструментальных показателей на фоне соблюдения немедикаментозных мер и регулярного приёма комбинированной терапии свидетельствует об успехе в лечении МС и у пожилых пациентов. Кроме того, данное наблюдение подчёркивает необходимость (эффективность и безопасность) назначения гиполипидемической терапии (в данной ситуации использовалась комбинация препаратов, влияющих на липидный обмен: симвастатин и УДХК) для лечения атерогенной дислипидемии у пожилых больных.
Увеличение использования статинов для первичной и вторичной профилактики заболеваний сердечно-сосудистой системы ежегодно сможет предотвратить десятки тысяч преждевременных смертей. В настоящее время есть убедительные научные доказательства и клинические данные, подтверждающие необходимость включения статинов (в первую очередь симвастатина) в обязательный список препаратов для активной профилактики и лечения атеросклероза. Результаты большого числа исследований позволяют говорить об эффективности и безопасности назначения симвастатина пациентам с неалкогольной жировой болезнью печени в рамках комплексной терапии метаболического синдрома. Хочется верить, что в скором будущем статины займут достойное место в первой десятке жизненно необходимых препаратов в нашей стране.
Литература
Но назначенный врачом прием статинов отменять нельзя! Их необходимо принимать постоянно, часто — пожизненно. Поэтому встает вопрос: можно ли как-то нейтрализовать их опасные побочные эффекты?
Ученые установили, что одновременно со снижением холестерина статины понижают и уровень коэнзима Q10, который жизненно необходим каждой клетке нашего организма, особенно — сердечно‑сосудистой системе и мышцам; к тому же он замедляет процессы старения. Уже через месяц приема статинов уровень коэнзима Q10 в организме падает на 50-80%2! При таком резком снижении уровня коэнзима организм начинает преждевременно стареть, увядать, ослабевать, становиться немощным. В США при назначении статинов все больше специалистов рекомендуют одновременно со статинами принимать коэнзим Q103.
Как правильно выбрать коэнзим Q10?
На полках аптек можно найти самые разные виды и формы коэнзима – таблетки, капли на водной основе, суспензии и т.д. Но надо помнить, что коэнзим Q10 – вещество жирорастворимое, то есть максимально усваивается в виде масляного раствора. Поэтому внимательно прочтите состав на упаковке — на первом месте должно стоять масло. Чаще всего используется соевое – оно отличается дешевизной и неприятным послевкусием; чуть реже – оливковое. А вот компания «Эвалар» для лучшего усвоения своего Коэнзима Q10 выбрала не какое-нибудь масло, а кокосовое, которое само по себе представляет просто кладезь необходимых нашему организму нутриентов. В каждой капсуле Коэнзима Q10 Эвалар – максимальная4 дозировка коэнзима (100 мг), растворенного в кокосовом масле первого холодного отжима, от ведущего производителя Японии. При этом Коэнзим Q10 Эвалар в 2 раза выгоднее аналога5!
Коэнзим Q10 Эвалар способствует:
- уменьшению побочных действий статинов;
- укреплению сердечной мышцы;
- сохранению молодости и красоты
- замедлению процессов старения.
Где заказать?
Заказать на Аптека.ру
Заказать на Эвалар
Заказать на Фитомаркет
Действие Коэнзима Q10, описанное в статье, находится в рамках корректировки функционального состояния (не является лечебным) и подтверждается СоГР № KZ.16.01.95.003.E.000173.03.17 от 18.03.2017 г.
Основная ниша применения статинов на сегодняшний день – это снижение смертности и улучшение прогноза у пациентов с ишемической болезнью сердца или другими проявлениями атеросклероза, а также для лечения нарушений липидного обмена у больных с наследственными и вторичными дислипидемиями .
Как уже хорошо известно, имеется прямая зависимость между уровнем холестерина и холестерина липопротеинов низкой плотности (ХС ЛПНП) в сыворотке крови и смертностью от ИБС. Поэтому основной целью гиполипидемической терапии является снижение именно ХС ЛПНП. В настоящее время для достижения этой цели наиболее эффективными препаратами являются ингибиторы 3–гидрокси–3–метилглутарил–коэнзим А–редуктазы (ГМГ–КоА–редуктазы) – статины, которые не только эффективно снижают уровень общего ХС и ХС ЛПНП, но и повышают уровень холестерина липопротеинов высокой плотности (ЛПВП) и обладают выраженным антиатеросклеротическим действием.
Механизм действия статинов: ГМГ–КоА–редуктаза – это фермент, катализирующий синтез эндогенного холестерина в печени и дистальных отделах тонкой кишки. В результате по принципу отрицательной обратной связи снижается концентрация холестерина в гепатоцитах, что повышает экспрессию рецепторов к ЛПНП в печени, которые удаляют ЛПНП и его предшественники из циркулирующей крови и повышается содержание ЛПВП .
Также статины обладают рядом плейотропных эффектов: противовоспалительное действие, улучшение функции эндотелия, антиагрегантный эффект, торможение пролиферации гладкомышечных клеток сосудистой стенки, стимуляция фибринолиза и антиоксидантный эффект. Данные эффекты не зависят от гипохолестеринемической активности статинов . Статины снижают содержание в плазме С–реактивного белка, ингибируют экспрессию антигенов главного комплекса гистосовместимости на макрофагах, эндотелиоцитах и гладкомышечных клетках сосудистой стенки, стимулированных интерфероном g . Они подавляют также синтез важных провоспалительных цитокинов: фактора некроза опухоли–a (ФНО–a), интерлейкина 1 (ИЛ–1), ИЛ–6 и ИЛ–8 . Важно отметить, что эпидемиологические данные свидетельствуют о тесной связи повышенного содержания маркеров воспаления и риска серьезных сердечно–сосудистых осложнений . Улучшение местного сосудистого гомеостаза происходит на уровне выработки оксида азота (NO–зависимая вазодилатация) . Антиоксидантный эффект статинов ассоциируют с редукцией синтеза свободных кислородных радикалов . Это приводит к снижению образования окисленных ЛПНП, а следовательно, замедляет аккумуляцию холестерина в макрофагах, тормозит образование пенистых клеток, снижает их цитотоксичность, уменьшает уровень активности воспалительных процессов, что также тормозит атерогенез .
Исследования in vitro показали, что большинство статинов уменьшают пролиферацию гладкомышечных клеток и их миграцию, которые являются ключевыми процессами в атерогенезе, патогенезе рестеноза после ангиопластики коронарных артерий, окклюзии венозных шунтов после операции коронарного шунтирования и васкулопатии трансплантанта у больных после пересадки сердца .
Побочные эффекты статинов: препараты хорошо переносятся, среди побочных эффектов могут отмечаться боли в животе, метеоризм, запоры. Асимптомное повышение уровня печеночных трансаминаз более чем в 3 раза по сравнению с верхней границей нормы на фоне терапии статинами встречается у 3 больных из 1000. Если уровень хотя бы одного из ферментов при двух последовательных измерениях превышает в 3 раза верхние пределы нормальных значений, прием статинов следует прекратить. В случаях умеренного повышения ферментов достаточно снизить дозу препарата. Обычно в течение короткого времени уровни ферментов возвращаются к норме и лечение возобновляют с меньшей дозы либо с назначением другого статина. Печеночная недостаточность на фоне терапии статинами отмечается у 1 пациента из 1 млн.; с такой же частотой печеночная недостаточность встречается у больных, не принимающих статины. Эксперты NLA считают, что нет необходимости мониторировать уровень печеночных трансаминаз у больных, получающих статины . Довольно редко (0,1–0,5%) при приеме статинов наблюдаются миопатия и миалгия, которые проявляются болью и слабостью в мышцах и повышением уровня креатинкиназы (КК) более чем в 5 раз. Крайне опасным осложнением терапии статинами следует считать рабдомиолиз (распад мышечной ткани). Осложнение сопровождается повышением уровня КК более чем в 10 раз и потемнением цвета мочи из–за миоглобинурии. При появлении симптомов рабдомиолиза прием статинов необходимо срочно прекратить. Для лечения осложнения применяют экстракорпоральные методы очистки крови – плазмаферез и гемодиализ. Данное осложнение чаще наблюдается при сочетании статинов с фибратами, цитостатиками, антибиотиками – макролидами. Причина более частого развития осложнений при таком сочетании обусловлена тем, что метаболизм ловастатина, симвастатина, аторвастатина происходит через систему цитохрома Р–450 и ее изоформы 3А4. Конкурентное связывание фермента ведет к повышению концентрации статинов в плазме крови и к повышению их токсических свойств. При необходимости сочетанного применения этих препаратов со статинами следует назначать минимальную дозу статинов и контролировать уровни печеночных ферментов и КК не реже 1 раза в месяц.
Более чем 20–летний опыт применения статинов показал, что преобладающим большинством пациентов эти препараты хорошо переносятся. Так, в 2006 году был опубликован отчет NLA (National Lipid Association), в котором рассматривался вопрос безопасности применения статинов. Этот отчет включал в себя результаты нескольких недавно завершившихся клинических исследований, информацию из базы данных системы здравоохранения США (более 470 тыс. пациентов), а также сообщения о побочных эффектах статинов в реальной клинической практике и медицинские публикации. Данный отчет еще раз подтвердил, что все статины, имеющиеся на фармацевтическом рынке, обладают сходным профилем безопасности с хорошей переносимостью и низкой вероятностью побочных эффектов .
Проведено большое количество многоцентровых клинических исследований, в которых участвовало в общей сложности более 100 тыс. пациентов (длительность наблюдения – 5 лет и более).
Одним из первых крупных исследований, направленных на изучение вопроса об увеличении продолжительности жизни кардиологических больных на фоне приема статинов, стало двойное слепое плацебо–контролируемое исследование 4S (Scandinavian Simvastatin Survival Study), в котором была изучена частота осложнений и смертность у больных ИБС. В исследование было включено 4444 пациентов со стабильной стенокардией, перенесенным инфарктом миокарда, уровнем холестерина 5,5–8,0 ммоль/л, которых рандомизировали на группы, получающие симвастатин или плацебо. Все больные также получали липид–снижающую диету. Через 5,4 лет оказалось, что в отличие от пациентов группы контроля на фоне приема симвастатина уровень общего холестерина снизился на 25%, ЛПНП – на 35%, а уровень ЛПВП повысился на 8%. Выживаемость пациентов в группе симвастатина оказалась достоверно большей и составила 91,3%, причем особенно высоким данный показатель был в подгруппе больных старше 65 лет. Снижение общей смертности в группе симвастатина составило 42%, риска осложнений ИБС – 34% .
Недавно проведенный дополнительный анализ исследования 4S показал, что симвастатин достоверно снижает риск кардиоваскулярных событий у больных с умеренной хронической почечной недостаточностью, в т.ч. инфаркта миокарда и коронарной реваскуляризации, при этом достоверного влияния на вероятность развития инсульта выявлено не было . Несмотря на то, что дислипидемия – потенциально модифицируемый фактор риска у больных с сердечно–сосудистой патологией и сниженной скоростью клубочковой фильтрации, до последнего времени имеется мало исследований, демонстрирующих способность статинов увеличивать продолжительность жизни этой категории больных. Большой интерес представляют данные исследования 4S о влиянии симвастатина на больных с сочетанием ишемической болезни сердца и сахарного диабета 2 типа (n=202). Положительный эффект лечения симвастатином у этой группы больных был более выраженным, чем у больных с ишемической болезнью сердца без диабета: общая смертность снизилась на 43%, смертность от ишемической болезни сердца на 36%, риск основных коронарных событий на 55% (p=0,002), инсульта на 54%.
Сегодня довольно активно обсуждается вопрос о способности статинов снижать частоту развития инсультов. Согласно данным многих мета–анализов, включавших в общей сложности около 20 тыс. пациентов, частота развития инсульта на фоне приема статинов уменьшается на 2–30%, причем остается неясным, является ли это прямым следствием только гиполипидемических свойств или же дополнительным результатом плейотропных эффектов препаратов. Так, известно, что важная роль при повреждении нервной ткани в условиях гипоксии принадлежит провоспалительным цитокинам, в т.ч. ФНО–a. Симвастатин, назначенный в течение 24 часов от начала развития симптоматики инсульта, достоверно снижает концентрацию ФНО .
Важной стороной применения статинов является вторичная профилактика сердечно–сосудистых осложнений после интервеционных вмешательств на коронарных артериях. Так, в международном многоцентровом рандомизированном двойном слепом плацебо–контролируемом исследовании LIPS (Lescol Intervention Prevention Study) было оценено длительное применение флувастатина, назначаемого с профилактической целью после выполнения первичной коронарной ангиопластики со стентированием. Известно, что после чрескожной коронарной ангиопластики удается получить отличное кратковременное улучшение у больных, проявляющееся в снижении ишемических симптомов. Однако только у немногих пациентов в отдаленном периоде не отмечается серьезных нежелательных сердечных осложнений . Целью исследования LIPS было изучить, может ли снижение уровня холестерина при лечении флувастатином в сравнении с плацебо, начатом вскоре после успешной ангиопластики (как со стентированием так и без), увеличивать время до наступления сердечно–сосудистых осложнений. В исследование было включено 1677 пациентов мужского и женского пола в возрасте от 18 до 80 лет, перенесших первую успешную коронарную ангиопластику по поводу одной и более бляшек в коронарных артериях. Для включения в исследование у пациентов уровень общего ХС в крови должен был быть в интервале от 135 до 270 мг/дл (от 3,5 до 7,0 ммоль/л), уровень триглицеридов, определяемый натощак менее чем 400 мг/дл (4,5 ммоль/л) до проведения процедуры. Пациенты были разделены на 2 группы: получения флувастатина 80 мг/сут. и плацебо. Время, свободное от серьезных нежелательных сердечных событий (СНСС) (первичная конечная точка), было значимо больше в группе больных, получавших лечение флувастатином в сравнении с плацебо (p=0,01). 181 (21,4%) из 844 пациентов в группе, леченной флувастатином, и 222 (26,7%) из 833 пациентов, получавших плацебо, перенесли как минимум одно СНСС (относительный риск 0,78; 95% доверительный интервал 0,64–0,95; р=0,01). При этом результат не зависел от исходных уровней холестерина. Наиболее выраженным снижение частоты СНСС было отмечено у больных с исходно более высоким риском осложнений, т.е. при множественном поражении коронарных артерий, при наличии сахарного диабета, нестабильной стенокардии. Так, у больных с сопутствующим сахарным дибетом лечение флувастатином привело к снижению риска СНСС на 47% (р=0,04); у больных с нестабильной стенокардией – на 28% (р=0,03) в сравнении с плацебо.
Другим наиболее важным исследованием явилось крупнейшее плацебо–контролируемое исследование HPS (Heart Protection Study) (n=20536), , куда включили пациентов с ИБС и высоким риском сердечно–сосудистых осложнений (страдающих диабетом, перенесших инфаркт миокарда, инвазивные сердечно–сосудистые вмешательства, инсульт и др.). Уровень общего холестерина исходно должен был быть не ниже 3,5 ммоль/л. В результате было достигнуто достоверное снижение уровня липидов в крови. В течение периода наблюдения среднее различие между группами симвастатина и плацебо в уровне холестерина составило 1,2 ммоль/л, в уровне ЛПНП – 1 ммоль/л. Несмотря на то что в течение первого года не было выявлено отличий между группами рандомизированных больных, в дальнейшем была четко продемонстрирована эффективность симвастатина в дозе 40 мг/сут. как препарата, достоверно снижающего сердечно–сосудистую смертность у больных высокого риска. Исследование подтвердило, что на фоне приема симвастатина снижается смертность от любых причин (12,9% в группе симвастатина против 14,7% в группе плацебо, p=0,0003), коронарной смерти (5,7% против 6,9%, p=0,0005), нефатального инфаркта миокарда (8,7% против 11,8%, p<0,0001), нефатального инсульта (4,3% против 5,7%, p<0,0001). Также уменьшалась потребность в коронарной (р<0,0001) и некоронарной (р=0,006) реваскуляризации. Многолетний прием симвастатина оказался безопасным. Так, риск развития миопатии составил 0,01%. Было подтверждено, что симвастатин не повышает риск развития злокачественных новообразований и госпитализаций по некардиологическим причинам. Исследование HPS имело огромное значение для клинической практики . Основываясь на полученных в ходе него результатах, было предложено использовать дозу симвастатина 40 мг, как стартовую для данного препарата с целью избежать необходимости в постепенном подборе дозы и обеспечения более быстрого и значимого снижения липидных фракций. Проведенный ретроспективный фармакоэкономический анализ результатов HPS продемонстрировал, что прием симвастатина ассоциируется с уменьшением расходов, связанных с госпитализацией по поводу любых сердечно–сосудистых осложнений, на 22%. Оказалось, что чем больший высокий коронарный риск имелся у пациента изначально, тем более фармакоэкономически обоснованным было использование симвастатина .
Симвастатин остается одним из наиболее изученных препаратов, который активно используется в клинической практике с 1988 г. и имеет довольно внушительную доказательную базу в плане эффективности и хорошей переносимости. Симвастатин оценивался в крупнейших исследованиях, именно этот препарат использовался в качестве гиполипидемического средства и большинство свойств статинов изучены именно на примере симвастатина, как эталонного представителя группы . На российском фармацевтическом рынке с успехом используется генерический аналог оригинального симвастатина – препарат Симвастол (Гедеон Рихтер), что делает применение статинов более доступным с экономической точки зрения для широкого круга пациентов.
Литература
1. Российские рекомендации «Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза», Секция атеросклероза ВНОК // Кардиоваскулярная терапия и профилактика. 2004. № 2 (приложение). 36 с.
2. Tonkin A.M. Clinical relevance of statins: their role in secondary prevention. Atheroscler Suppl. 2001 Feb;2(1):21–5.
3. Courville K.A., Lavie C.J., Milani R.V. Lipid–lowering therapy for elderly patients at risk for coronary events and stroke. Am Heart Hosp J. 2005 Fall;3(4):256–62.
4. Law M., Wald N.J. Efficacy and safety of cholesterol–lowering treatment // Lancet 2006 Feb 11;367(9509):469–70.
5. Чазов Е.И., Беленков Ю.Н., Борисова Е.О., Гогин Е.Е. и др. Рациональная фармакотерапия сердечно–сосудистых заболеваний: руководство для практикующих врачей / под общ. ред. Е.И. Чазова, Ю.Н. Беленкова. М.: Литтерра, 2004. 972 с.
6. Kleemann R., Kooistra T. HMG–CoA Reductase Inhibitors: Effects on Chronic Subacute Inflammation and Onset of Atherosclerosis Induced by Dietary Cholesterol. Curr Drug Targets Cardiovasc Haematol Disord. 2005 Dec;5(6):441–53.
7. Liao J.K. Clinical implications for statin pleiotropy. Curr Opin Lipidol. 2005 Dec;16(6):624–9.
8. Halcox J.P., Deanfield J.E. Beyond the laboratory: clinical implications for statin pleiotropy. Circulation. 2004 Jun 1;109(21 Suppl 1):II42–8.
9. Crisby M. Modulation of the inflammatory process by statins. Timely Top Med Cardiovasc Dis. 2005 Mar 1;9:E3.
10. Sorrentino S., Landmesser U. Nonlipid–lowering Effects of Statins. Curr Treat Options Cardiovasc Med. 2005 Dec;7(6):459–66.
11. Callahan A.S. 3rd. Vascular pleiotropy of statins: clinical evidence and biochemical mechanisms. Curr Atheroscler Rep. 2003 Jan;5(1):33–7.
12. Leu H.B., Chen J.W., Wu T.C. et al. Effects of fluvastatin, an HMG–CoA reductase inhibitor, on serum levels of interleukin–18 and matrix metalloproteinase–9 in patients with hypercholesterolemia. Clin Cardiol. 2005 Sep;28(9):423–8.
13. Mora S., Ridker P.M. Justification for the Use of Statins in Primary Prevention: an Intervention Trial Evaluating Rosuvastatin (JUPITER) – can C–reactive protein be used to target statin therapy in primary prevention? Am J Cardiol. 2006 Jan 16;97(2A):33A–41A.
14. Clearfield M.B. C–reactive protein: a new risk assessment tool for cardiovascular disease. J Am Osteopath Assoc. 2005 Sep;105(9):409–16.
15. Patti G., Melfi R., Di Sciascio G. The role of endothelial dysfunction in the pathogenesis and in clinical practice of atherosclerosis. Current evidences. Recenti Prog Med. 2005 Oct;96(10):499–507.
16. Ng D.S. The role of statins in oxidative stress and cardiovascular disease. Curr Drug Targets Cardiovasc Haematol Disord. 2005 Apr;5(2):165–75.
17. Hassan H.H., Denis M., Krimbou L. Cellular cholesterol homeostasis in vascular endothelial cells. Can J Cardiol. 2006 Feb;22 Suppl B:35B–40B.
18. Conti CR. Updated pathophysiologic concepts in unstable coronary artery disease. Am Heart J 2001; 141 (2 Suppl): S12–4.
19. Dupuis J. Mechanisms of acute coronary syndromes and the potential role of statins. Atheroscler Suppl 2001; 2:9–14.
20. James McKenney The Report of the National Lipid Association Statin Safety Task Forse Am J Cardiol. 2006: 97:Sup.
21. The Scandinavian Simvastatin Survival Study group. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S) // Lancet 1994;344:1383–89.
22. Chonchol M., Cook T., Kjekshus J. et al. Simvastatin for secondary prevention of all–cause mortality and major coronary events in patients with mild chronic renal insufficiency // Am J Kidney Dis. 2007 Mar;49(3):373–82.
23. Szczepanska–Szerej A., Kurzepa J., Wojczal J., Stelmasiak Z. Simvastatin–induced prevention of the increase in TNF–alpha level in the acute phase of ischemic stroke // Pharmacol Rep. 2007 Jan–Feb;59(1):94–7.
24. Ruygrok PN, de Jaegere PT, van Domburg RT et al. Clinical outcome 10 years after attempted percutaneous transluminal coronary angioplasty in 856 patients. J Am Coll Cardiol. 1996;27:1669–1677.
25. Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20,536 high–risk individuals: a randomised placebo–controlled trial // Lancet. 2002 Jul 6;360(9326):7–22.
26. Minhas R. Statins in primary care: bridging the treatment gap // Br J Cardiol 2004;11(6):487–91.
27. Heart Protection Study Collaborative Group. Cost effectiveness of simvastatin in people at different levels of vascular disease risk: economic analysis of a randomised trial in 20 536 individuals // Lancet 2005;365: 1779–85.
28. Pedersen T.R., Tobert J.A. Simvastatin: a review // Expert Opin Pharmacother. 2004 Dec;5(12):2583–96.
Наши приоритеты
Считается, что первым её выдвинул русский и советский учёный Николай Николаевич Аничков. В 1913 г. он опубликовал работу, в которой доказал, что у кроликов, которых кормили холестерином, развиваются атеросклеротические бляшки. В мире исследование Аничкова считают одним из самых главных открытий в кардиологии ХХ века. Это редкий случай, когда на Западе признали приоритет руского медика. Но тогда эти исследования на Западе не заметили. О них вспомнили только 40 лет спустя, когда в 1950-е «переоткрыли» холестерин и начали его изучать. Самое главное случилось в 1961 г., когда вышло Фрамингемское исследование. В нём много лет наблюдали несколько тысяч американцев и выявили три главных фактора риска атеросклероза – высокое давление, курение и повышенный холестерин в крови. Чем он выше, тем выше был риск атеросклероза и инфаркта.
После этого, когда главного врага открыли вновь, процесс пошёл. Интенсивные исследования привели в 1976 г. к открытию первого статина. В отличие от других препаратов он реально снижал холестерин в крови. Ещё через 5 лет первый статин появился в продаже.
Фармкомпании поняли, что это золотая жила, и новые статины, один сильнее другого, начали валиться как из рога изобилия. Они стали самыми употребляемыми препаратами в мире, их продавали на десятки миллиардов долларов каждый год. На фоне эйфории критический взгляд на них был потерян, и они, по сути, спровоцировали создание фармацевтической утопии. Статины провозгласили лекарством для всех, кто перешагнул 50–55-летний рубеж. Совершенно серьёзно обсуждалось, что их нужно назначать всем, кто имеет хоть какие-нибудь факторы риска атеросклероза (а у кого их нет?), чтобы предотвратить развитие бляшек в сосудах, а значит, избежать инфарктов и инсультов. Для этого предлагали статины продавать свободно, без рецепта. И даже запустили на здоровых людях в Индии масштабные исследования суперпилюли, содержащей сразу статин, аспирин и несколько компонентов для снижения давления.
Но в прошлом году пузырь лопнул. 16 учёных из разных стран с доказательствами на руках обвинили «статиновых адвокатов» в том, что они искажали результаты исследований, чтобы назначать эти лекарства всё больше и больше – даже людям без болезней сердца и бляшек, которым они могут быть вредны (см. «АиФ» № 42 за 2018 г.). После этого отношение к статинам становится всё более взвешенным. Переоценивается и роль холестерина. Значение в развитии атеросклероза не отрицается, но к его снижению подходят более взвешенно.
Утопия отменяется
«Снижение холестерина статинами не является самоцелью, – объясняет врач-кардиолог, кандидат медицинских наук Ярослав Ашихмин. – Главный эффект этих препаратов – стабилизация покрышки холестериновых бляшек в сосудах. Благодаря действию статинов, она становится более плотной и менее подверженной разрыву (в месте разрыва бляшки образуется тромб, приводящий к инфаркту или инсульту). Поэтому применение статинов у людей с бляшками обязательно для профилактики таких состояний. Например, у тех, кто уже перенёс инфаркт и инсульт, такие бляшки есть наверняка. И чтобы они не возникали повторно, им статины нужно принимать обязательно, даже не проверяя уровень холестерина, – это называется вторичной профилактикой. К сожалению, у нас в стране таким пациентам их часто не назначают. А вот людям без бляшек в сосудах статины обычно, наоборот, не нужны. Но им их часто назначали для так называемой первичной профилактики инфарктов и инсультов. Хотя нет достаточных оснований полагать, что статины будут эффективны у пациентов, не имеющих болезней сосудов и сердца.
 Вопрос-ответ Как определить, повышен ли холестерин в крови? Но есть проблема в том, что бляшки могут существовать скрытно. В таких случаях назначение статинов лучше делать индивидуально. Для этого у пациентов с высоким риском формирования бляшек, но без явных поражений сердца и сосудов, возможно провести низкодозовую компьютерную томографию сердца. Это поможет определить в сосудах бляшки, если они есть, и решить вопрос, нужны статины в лечении или нет».
Вопрос-ответ Как определить, повышен ли холестерин в крови? Но есть проблема в том, что бляшки могут существовать скрытно. В таких случаях назначение статинов лучше делать индивидуально. Для этого у пациентов с высоким риском формирования бляшек, но без явных поражений сердца и сосудов, возможно провести низкодозовую компьютерную томографию сердца. Это поможет определить в сосудах бляшки, если они есть, и решить вопрос, нужны статины в лечении или нет».
Сегодня на одной из медицинских страничек нашла запутанную статью про то, что сейчас уже совсем по-другому назначают статины. И в коментах к статье — закономерный вопрос «а кто же все таки должен принимать статины?». Вопрос действительно правильный и непростой. Поэтому по горячим следам решила объяснить своим читателям, кому показан прием статинов.
Для начала давайте разберем, а что за зверь такой эти статины. Статины — группа препаратов, которые снижают синтез печенью холестерина. Как они это делают? А просто блокируют фермент, необходимый для реакции синтеза холестерина. Статины не имеют эффекта привыкания, накопительного эффекта. Тут все просто — принимаешь статины — холестерин не синтезируется, перестал принимать — снова налаживается «массовое производство». О том, для чего и почему печень синтезирует холестерин можно напомнить себе, прочитав статью «Откуда берется холестерин?» (см. выше). Препараты этой группы принимаются постоянно, назначать их на короткий курс (часто вижу в рекомендациях) не имеет смысла, так как после прекращения приема все быстро возвращается на свои места — и высокий уровень холестерина, и высокий риск атеросклероза и его последствий (инфарктов, инсультов и тд.). Основными представителями группы статинов, которые назначаются и используются на сегодняшний день, являются розувастатин и аторвастатин. Они самые безопасные и эффективные.
Подписывайтесь на новости «КиевVласть”
А теперь давайте перечислим все группы пациентов, которым показан постоянный прием этих препаратов:
1. Пациенты с уровнями холестерина и «тяжелых» липопротеидов выше нормы, у которых правильно назначенные врачом и правильно выполняемые пациентом немедикаментозные методы снижения не дали результата. Обычно своим пациентам с повышенными показателями (нормы еще раз напомню в конце статьи) я разрабатываю индивидуальную схему снижения холестерина, которая включает диету, физ нагрузки и т.д. на 4 месяца. Если через 4 месяца мы не получаем эффекта — начинается прием лекарств.
2. Пациенты с сахарным диабетом 2 типа, независимо от уровней холестерина и фракций.
3. Пациенты с доказанным атеросклерозом, независимо от уровней холестерина и фракций. Например, на УЗД сосудов шеи были обнаружены бляшки или доказана ишемическая болезнь сердца.
4. Пациенты, перенесшие в прошлом инфаркт или инсульт, независимо от уровней холестерина и фракций.
5. Пациенты после постановки стентов или аорто-коронарного шунтирования, независимо от уровней холестерина и фракций
Для того, чтобы понимать, какой холестерин считается повышенным, еще раз напомню цифры.
-уровень общего холестерина должен составлять менее 5,2 ммоль/л
-уровень ХС липопротеидов низкой плотности (ЛПНП) менее 3,0 ммоль/л
— уровень ХС липопротеидов высокой плотности (ЛПВП) у женщин должен быть не ниже 1,2 ммоль/л, у мужчин – не ниже 1,0 ммоль/л,
— уровень триглицеридов – не выше 1,7 ммоль/л.
Желаю всем не оказываться в группе риска, заботиться о себе и своем здоровье.
Вопросы можно прислать на электронную почту
Читайте:
Как «увидеть” атеросклероз
Откуда берется холестерин (часть2)
Откуда берется холестерин (часть1)
Анализ, который спасает жизнь
Как узнать, есть ли бляшки в сосудах сердца (часть2)
Как узнать, есть ли бляшки в сосудах сердца (часть1)
Анна Солощенко, врач-кардиолог высшей категории в Александровской клинической больнице и клинике «Инго»
КиевVласть

